Навигация
Вызывают глюгонеогенез, обеспечивая тем самым легко доступный источник энергии для реакции адаптации
1. Вызывают глюгонеогенез, обеспечивая тем самым легко доступный источник энергии для реакции адаптации.
2. Облегчают осуществление различных других регулируемых ферментами адаптивных обменных реакций.
3. Подавляют иммунные реакции, воспаление. Подавление выработки антител под влиянием АКТГ и кортизона может играть защитную роль в иммунологических реакциях неспецифической природы. Известно, что в пораженных тканях происходит изменение их антигенных свойств, поэтому они могут быть источником аутосенсибилизации организма. Гормоны, уменьшая образование антител, тем самым предотвращают явление аутоагрессии тканей.
4. Обуславливают тимиколимфатическую инволюцию, эозинопению и лимфопению, характерные для острого стресса. Инволюция тимиколимфатической система и лимфопения, с одной стороны, связаны с разрушением лимфоидных клеток (катотоксическое действие глюкокортикоидов, в результате которого образующиеся при распаде аминокислоты используются в глюконеогенезе), а с другой стороны, лимфоидные клетки мигрируют в костный мозг, что приводит к активации гранулоцитопоэза и развитию нейтрафилеза, т.е. в крови нарастает количество микрофагов.
5. Понижают проницаемость сосудов. Они предупреждают повышение проницаемости сосудистой стенки, вызванное гиалуронидазой, лейкотоксином, экссудином.
6. АКТГ и глюкокортикоиды понижают проницаемость гематоэнцефалического барьера, вследствие этого повышается устойчивость к действию нейротропных веществ (морфины, наркотики).
Таким образом. Вызванный любым фактором среды стресс выглядит, как генерализованная реакция мобилизации энергетических ресурсов, охватывающая весь организм, но и происходит перераспределение энергетических и структурных ресурсов или передача их из систем, не участвующих в адаптации к данному стрессору, в системы, специфически ответственные за эту адаптацию. Благодаря такому перераспределению кислород, субстраты окисления, а также предшественники, используемые для синтеза нуклеиновых кислот и белков, направленно поступают в системы, осуществляющие специфическую защиту. Это положение иллюстрируют следующие примеры. Катаболический эффект глюкокортикоидов при стрессе состоит в том, что в мышечной, соединительной, лимфоидной и жировой тканях и коже эти гормоны тормозят синтез белка и нуклеиновых кислот и активируют распад белка; в результате в крови значительно возрастает количество свободных аминокислот. Но на фоне этого эффекта глюкокортикоиды реализуют в печени анаболический эффект, а именно активируют синтез системы белков-ферментов, специфически ответственных за неоглюкогенез, трансформирование и синтез альбумина плазмы крови. При этом для активации синтеза белка в печени используются аминокислоты, освободившиеся при разрушении структур других органов и в избытке имеющиеся в крови. Другой пример: состояние готовности к борьбе и сама борьба характеризуется у животных не только общей мобилизацией дыхания, кровообращения, но также значительным сужением сосудов органов брюшной полости и неактивных мышц. Это свидетельствует, что возникший в результате реакции мобилизации избыток кислорода, глюкозы и жирных кислот избирательно направляются в системы, осуществляющие увеличенную функцию.
Для ГАС характерны несколько групп адаптивных реакций:
1. Процессы, направленные на обеспечение двигательных реакций (борьбы или убегания): повышение уровня сахара в крови для энергообеспечения, расширение зрачка (увеличение поля зрения), повышение АД и учащение сердечного ритма, улучшение кровоснабжения мышц, повышение деятельности ЦНС, повышение выпотевания жидкости в суставные полости.
2. Процессы, направленные на подготовку к получению механического повреждения тканей: повышение свертываемости крови (предотвращение кровотечения), повышение пролиферативной активности клеток соединительной ткани (для дефекта ткани).
3. Процессы, направленные на активацию физиологических барьеров, препятствующих проникновению патогенного агента в организм: понижение проницаемости гематоэнцефалического барьера, активация дезинтоксикационной функции печени и т.д.
4. Процессы, направленные на подготовку к встрече с инфекционным агентом: активация гранулоцитопоэза (повышение образования микрофагов), предотвращение аутосенсибилизации организма и т.д.
Местный адаптационный синдром (МАС).
Для МАС характерны выраженные изменения в месте действия стрессора. Эта область получила название – область «мишени». Механизм его формирования аналогичен ГАС. Первый медиатор адаптации, образовавшийся в области «мишени» действует через гипоталамус на переднюю долю гипофиза, стимулируя освобождение АКТГ и СТГ. АКТГ, действуя на надпочечники, приводит к повышению в крови уровня глюко- и минералокортикоидов. СТГ сенсибилизирует ткань области «мишени» к действию провоспалительных гормонов, следствием чего будет развитие воспалительного процесса, локализующего патогенный агент в месте его внедрении.
На МАС, как правило, накладывается ГАС, образованный развивающимися общими явлениями. Наоборот, ГАС вторично влияет на МАС с помощью нейрогуморальных механизмов (например, антивоспалительных гормонов).
Шок (англ. shock – удар) – патологический процесс, возникающий при действии на организм сверхсильных патогенных раздражителей и характеризующийся фазным нарушением деятельности ЦНС, висцеральных функций и обмена веществ. Инициальным патогенетическим механизмом шока является массивный поток отрицательной афферентации, поступающей в ЦНС из зоны повреждения. Число состояний, относимых к шоку (постгеморрагический, инфекционно-токсический, гистаминовый и др.), нередко значительно расширяют. Это связано с тем, что шок не дифференцируют от такого явления, как коллапс (лат. сollapsus – ослабевший, упавший) – первично гемодинамического расстройства, которое развивается в результате возникшего несоответствия между объемом циркулирующей крови и сосудистого русла. Трудность разделения указанных состояний вполне объяснима, поскольку при шоке в его торпидной стадии может возникать острая сосудистая недостаточность, т.е. коллапс и гиперфузия тканей, в том числе мозга. Следовательно, и при шоке, и при коллапсе имеет место циркуляторная гипоксия. Некоторые (особенно зарубежные) исследователи в основе патогенеза шока видят расстройства микроциркуляциии, прежде всего в виде так называемых шоковых органах (почки и легкие), которые определяют тяжесть и исход шоковых состояний. Аналогичные по существу нарушения микроциркуляции, в том числе в почках и легких, могут быть при коллапсе.
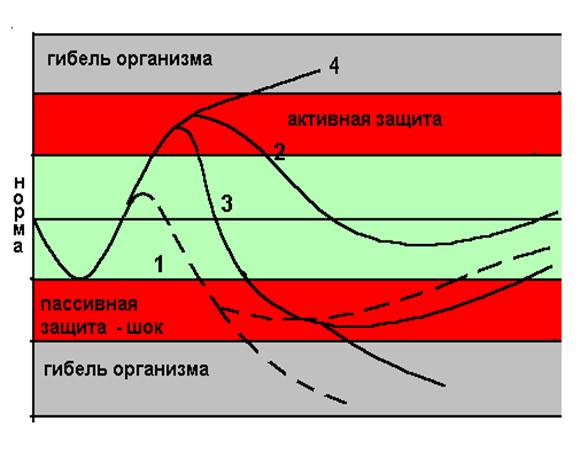
Шок – общая, т.е. полисистемная, двухфазная реакция организма на воздействие сверхсильных, угрожающих жизни раздражителей. По существу шок представляет собой стресс, при котором вследствие чрезмерной силы воздействия и/или низкой устойчивости организма характерные для стресса «реакция тревоги» и «стадия истощения» в своеобразной форме (эректильная и торпидная стадии) сохраняются, но «стадия резистентности» отсутствует. Коллапс – первично моносистемный процесс, связанный с острой сосудистой недостаточностью, хотя может также возникать при действии сверхсильных раздражителей. В основе патогенеза любого шока лежит массивное распространенное повреждение тканей, нередко включая рецепторный и проводниковый аппарат нервной системы (травматический, ожоговый, операционный и др.). Следствием этого является избыточная афферентация разных по модальности (в том числе болевых) сигналов в ЦНС. При коллапсе увеличение объема сосудистого русла вследствие падения сосудистого тонуса может возникать в результате «паралича» миоцитов резистивных сосудов, падения их адренореактивности, накопления в крови депрессорных агентов и т.п. Помимо отмеченных различий в патогенезе шока и коллапса следует отметить, что при шоке и в первую, и во вторую стадии сознание пациента сохранено, оно может быть затемненным с инертным мышлением, но полностью не утрачивается, и контакт пациента с врачом сохраняется. Напротив, при коллапсе может возникать полная утрата сознания.
Таким образом, шок является по патогенезу состоянием, первично связанным с изменением деятельности ЦНС, имеет две стадии развития и две стадии изменения регуляции жизнедеятельности, в соответствии, с чем регистрируются две последовательно сменяющие друг друга формы изменения кровообращения – гипер- и гиподинамическая. В отличие от этого коллапс по патогенезу является первично гемодинамическим расстройством, протекающим монофазно в виде нарастающего падения артериального и венозного давления.
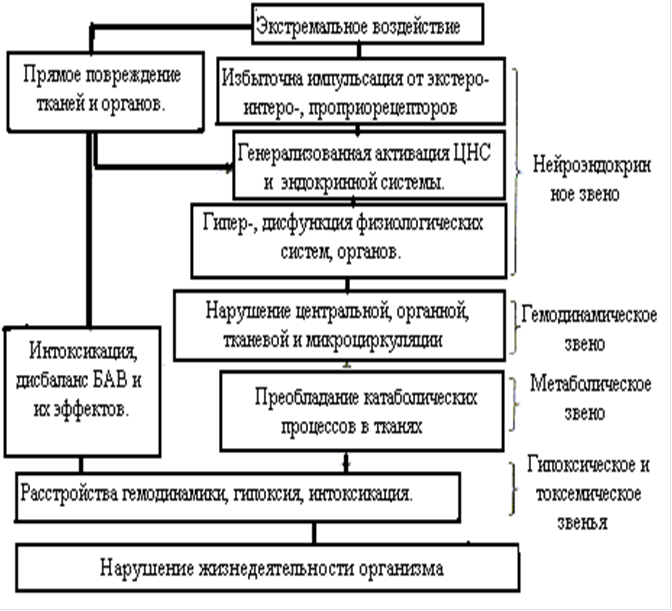
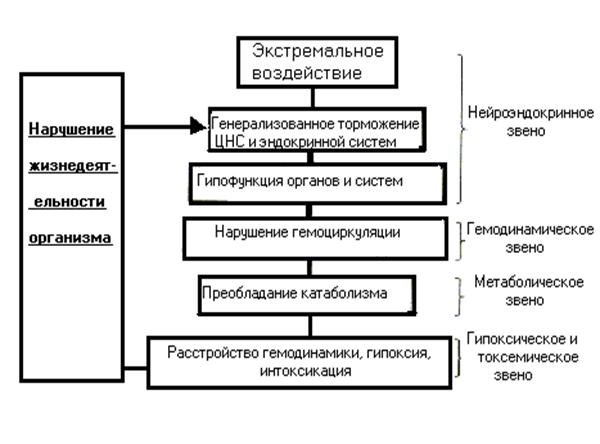
Для шока характерно двухфазное изменение деятельности ЦНС: первоначальное распространенное возбуждение нейронов (эректильная стадия), в дальнейшем сменяемое распространенным угнетением их активности (торпидная стадия). Фазные изменения активности нейронов ЦНС обусловлены избыточной афферентацией различного происхождения: неадекватным раздражением разнообразных экстро-, интеро- или проприорецепторов, повреждением нервных проводников, сплетений и мозговой ткани. Для шока характерно сохранение сознания в обе фазы развития, что существенно отличает его от комы. Сознание может быть несколько затемнено, однако оно не утрачивается полностью. Некоторые авторы выделяют третью, терминальную, стадию шока. Она по существу не отличается от коматозного состояния, при котором происходит утрата сознания.
В соответствии с фазными изменениями активности ЦНС при шоке наблюдаются фазные изменения нейроэндокринных влияний. В эректильной стадии шока усиливаются симпатико-адреналовые и гипофизарно-надпочечниковые влияния, которые перестраивают обмен веществ и повышают активность многих органов и систем. В торпидной стадии концентрация катехоламинов и кортикостероидов в крови обычно сохраняется повышенной, однако эффективность действия этих гормонов на различные органы-мишени снижается. В дальнейшем развивается недостаточность симпатико-адреналовой и гипофизарно-надпочечниковой систем, вследствие чего количество нейрогормоном в крови может снижаться. Возникающие вторично нарушения деятельности органов и систем приводят к существенным отклонениям от нормы жизненно важных параметров гомеостаза. В эректильной стадии функции центрального кровообращения и дыхания усиливаются (тахикардия, артериальная гипертензия, перераспределение крови, тахипноэ и др.). Могут повышаться число эритроцитов за счет выброса их из депо, а также свертываемость крови. В торпидной стадии угнетаются центральное кровообращение (брадикардия, артериальная гипотензия, депонирование крови) и дыхания (брадипноэ). В торпидной стадии шока возникающая недостаточность кровообращения и дыхания приводит к развитию тяжелой гипоксии, и именно гипоксия в дальнейшем определяет тяжесть шокового состояния.
Для шока характерны расстройства микроциркуляции, которые могут возникать уже в эректильной стадии вследствие перераспределения крови, редукции кровообращения в ряде органов (почки, печень, кишечник и др.). Нарушения микроциркуляции проявляется не только снижением перфузии крови через микрососуды, но и нарушением ее реологических свойств, повышением проницаемости стенок капилляров. Возрастание проницаемости гистогематических барьеров также является обычным компонентом шока и приводит к появлению в крови разнообразных токсических продуктов.
Обязательным процессом при шоках разной этиологии является интоксикация – токсемия. В зависимости от вида шока скорость возникновения и значение токсемии в патогенезе шока неодинаковы. При шоке токсическое действие оказывают многочисленные физиологически активные вещества, в избытке высвобождающиеся в гуморальную среду организма, например, гистамин, ацетилхолин, катехоламины, серотонин, кинины и др. В крови появляются денатурированные белки и продукты их гидролиза, лизосомные ферменты и другие компоненты распавшихся клеток, токсические продукты кишечника, микробы и их токсины. В развитии токсемии немаловажное значение имеют метаболиты, усиленно образующиеся в клетках вследствие нарушения обмена веществ и поступающие в кровь (молочная и пировиноградная кислоты, кетокислоты, аденозин, калий и др.). Возникающие в результате гипоксии и расстройств микроциркуляции нарушения функции почек и печени приводит к еще большим изменениям состава крови – накоплению производных аммония, ацидозу, ионному и белковому дисбалансу, изменению осмотического и онкотического давления.
В процессе развития шока первоначально возникающие нарушения деятельности органов и систем могут значительно усугубляться в результате включения «порочных кругов». Например, расстройства деятельности ЦНС приводит к нарушению регуляции кровообращения и дыхания. Угнетение этих жизненно важных функций вызывает гипоксию, а последняя усугубляет нарушения деятельности ЦНС.
Обычно шоковое состояние разделяют в зависимости от причинного фактора или от того процесса, который лежит в основе развития шока. Наиболее полно изучен травматический шок. Вместе с тем травматический шок – понятие собирательное. В него включают собственно травматический, ожоговый, турникетный, операционный шок, шок от ударной волны и синдром длительного раздавливания (краш-синдром). Различают также анафилактический и гемотрансфузионный шоки. Своеобразную и тяжелую форму шока представляет так называемый кардиогенный шок.
Травматический шок возникает при обширном механическом повреждении костей и мышц, внутренних органов, что обычно сопровождается травмой нервных окончаний, стволов и сплетений. Травматический шок часто усугубляется кровотечением и инфицированием ран.
Во время эректильной стадии у больного возникает речевое и двигательное возбуждение; больной мечется, даже на обычное прикосновение бурно реагирует распространенной локомоторной активностью вследствие повышения рефлекторной возбудимости. Кожные покровы бледные из-за спазма микрососудов кожи. Характерно расширение зрачков, обусловленное активацией симпатико-адреналовой системы. Показатели центрального кровообращения и внешнего дыхания повышены. Эректильная стадия сменяется торпидной. В торпидной стадии шока центральное кровообращение угнетается: артериальное давление, особенно систолическое снижается, уменьшается сердечный выброс. Характерна редукция кровообращения, которая начинает возникать уже в эректильной стадии; кровообращение в миокарде и мозге поддерживается на высоком уровне, а в почках, печени, скелетных мышцах и коже – понижается. Наблюдается нарушение микроциркуляции: вследствие повышения проницаемости капилляров и выхода из сосудов жидкости возникают сгущение крови и стазы. Нередко развиваются микротромбы, и даже диссеминированное внутрисосудистое свертывание крови. Объем циркулирующей крови уменьшается, кровь депонируется в органах брюшной полости, вследствие чего снижается венозный возврат крови к сердцу и еще более уменьшается сердечный выброс. Внешнее дыхание изменяется непостоянно: иногда оно частое и поверхностное, иногда – редкое глубокое. С увеличением тяжести шока может возникать дыхание Куссмауля, Чейна-Стокса и др.
В состоянии травматического шока больные могут погибнуть от прогрессирующей легочной или почечной недостаточности. В легких возникает нарушение микроперфузии и возрастает шунтирование крови, изменяются диффузионные свойства альвеолярно-капиллярных мембран вследствие их набухания и развития интерстициального отека. Снижение газообменной функции легких при травматическом шоке является грозным симптомом, требующим экстренного вмешательства врача («шоковое легкое»). Редукция кровообращения и микроциркуляторные расстройства в почках приводят к почечной недостаточности, которая проявляется азотемией и олигурией. На поздних стадиях шока в почках возможно нарушение канальцевых процессов вследствие образования гиалиновых и миоглобиновых цилиндров («шоковая почка»). Нарушение кровообращения в печени может приводить к недостаточности ее функции, что существенно отражается на составе крови и общем состоянии больных. В тяжелых случаях при травматическом шоке развивается кишечная аутоинтоксикация.
Обычным для травматического шока является лактат-ацидоз, а при легочной недостаточности – и респираторный ацидоз, гиперкалиемия, диспротеинемия и другие отклонения в составе крови. В крови могут появляться активные лизосомные ферменты, миозин, продукты протеолиза. Токсемия еще больше нарушает деятельность ЦНС, дыхание, кровообращение и функцию почек.
Ожоговый шок. Возникновение ожогового шока зависит от многих факторов, но, прежде всего от обширности и глубины поражения кожных покровов. Шок развивается в случае поражения 25 – 30 % всей поверхности тела (у детей – 8%) при II – III степени ожога. При наличии общих с травматическим шоком механизмов развития ожоговый шок имеет свои существенные особенности.
При ожоговом шоке болевая афферентация поступает от обожженной поверхности кожи. Для этого вида шока характерна тяжелая и быстро развивающаяся интоксикация. При ожоговом шоке эректильная стадия сравнительно короткая и быстро переходит в торпидную стадию. Несмотря на прекращение действия термического фактора, при шоке больной как бы продолжает подвергаться действию ожога. Это связано с тем, что на ожоговой поверхности и по ее краям вследствие выхода из лизосом активных ферментов продолжает развиваться и даже нарастает протеолиз, в результате чего токсемия и выход на ожоговую поверхность жидкости нарастает. Еще одной важной особенностью ожогового шока является нарушение барьерной функции кожи, инфицирование обожженной поверхности бактериями, грибами и вирусами, что приводит к интоксикации организма продуктами их жизнедеятельности. Таким образом, токсемия при ожоговом шоке обусловлена денатурированными белками, продуктами их распада – полипептидами, физиологически активными веществами, высво-бождающимися из тучных клеток и нервных окончаний, или соединениями, образующимися во время протеолиза, - гистамином, катехоламинами, ацетилхолином, кининами и др. Немаловажное значение в развитии интоксикации имеют избыток калия, который выходит из гибнущих клеток, токсины микроорганизмов. Все эти вещества вследствие повышения проницаемости микрососудов резорбцируются с ожоговой поверхности в кровь.
Важное значение в развитии ожогового шока имеют нарушения деятельности висцеральных органов и систем и отклонения разных параметров гомеостаза. Вслед за кратковременной стимуляцией центрального кровообращения возникает его угнетение. Наряду с нарушением центральной регуляции в расстройстве кровообращения при ожоговом шоке существенное значение имеют перегрузка сердца вследствие сгущения крови, а также снижение возбудимости миокарда в результате гиперкалиемии. Одно из важных мест в развитии ожогового шока занимают микроциркуляторные нарушения: ухудшаются реологические свойства крови, повышается проницаемость мембран микрососудов. Сгущение крови и увеличение ее вязкости происходят вследствие выхода плазмы на ожоговую поверхность (плазморея). Изменения физико-химических свойств крови приводит к усиленному гемолизу эритроцитов. Наряду с этим при ожоговом шоке создаются условия для развития микротромбов. Резкое повышение проницаемости микрососудов обусловлено действием физиологически активных веществ, сначала местным, а затем их резорбцией в общий кровоток, т.е. распространенным действием. В более поздних стадиях ожогового процесса вследствие появления измененных белков, обладающих аутоантигенными свойствами, возможно развитие аутоаллергических поражений микрососудов и паренхиматозных клеток разных органов. Аутосенсибилизация и аутоаллергия могут играть весьма существенную роль в качестве патогенетических факторов ожоговой болезни, отягощающих ее течение. Тяжесть ожогового шока значительно повышается в случае поражения почек. Нарушение микроциркуляции в почках, появление в канальцах белка и гемоглобина, который легко проходит через мембраны клубочков, приводят к снижению азотовыделительной функции почечных клубочков и явлениям почечной недостаточности.
Нарушения состава внутренней среды организма связаны не только с появлением названных выше токсических агентов, но и с общими расстройствами обмена веществ. Для ожогового шока особенно характерны нарушения водного баланса, проявляющиеся внеклеточной дегидратацией вследствие потери жидкости. Помимо этого, возникает внутриклеточная гипергидратация, которая обусловлена задержкой натрия в тканях и их гипоксией, приводящей к усилению внутриклеточного протеолиза. Наряду с гипонатриемией для ожогового шока характерна гиперкалиемия. На ранних стадиях шока вследствие гипервентиляции развивается респираторный алкалоз, а позднее – метаболический ацидоз. Снижение концентрации альбуминов и натрия в крови приводит к изменению онкотических и осмотических ее свойств.
Кардиогенный шок. По мнению некоторых авторов, к кардиогенному шоку следует относить все состояния, при которых вследствие инфаркта миокарда или других острых нарушений насосной функции сердца резко падают ударный и минутный объемы сердца, возникают артериальная гипотония, расстройства микроциркуляции и характерные нарушения функции почек и легких («шоковая почка» и «шоковое легкое»). Кардиогенный шок возникает в 12 – 15% случаев инфаркта миокарда. Возникновение кардиогенного шока зависит от обширности зоны поражения миокарда, исходного состояния миокарда и состояния центрального кровообращения, а также от исходного состояния всего организма. При выключении 50 – 65% массы миокарда возникает либо фибрилляция сердца, либо острая сердечно-сосудистая недостаточность. При этом шок может не возникнуть. Кардиогенный шок чаще развивается при поражении меньшей массы миокарда (до 50%) на фоне резких болевых ощущений, сопровождающихся возбуждением определенных зон гипоталамуса и нарушением регуляции кровообращения.
При кардиогенном шоке эректильная стадия обычно непродолжительная. Вместе с тем сразу после острого нарушения коронарного кровообращения болевая афферентация может оказывать решающее влияние на развитие процесса. Кардиогенный шок отличается от других видов шока отсутствием выраженного повышения АД, столь характерного для шока в эректильной стадии. Это может быть связано с тем, что при инфаркте миокарда резко снижается ударный объем сердца. Возникающее при этом увеличение периферического сопротивления обычно не стабилизирует системное артериальное давление. Однако в ряде случаев вслед за нарушением коронарного кровообращения на фоне речевого и двигательного возбуждения у больного удается зарегистрировать кратковременную артериальную гипертонию. Торпидная стадия шока является продол-жительной (многие часы), если лечебные мероприятия малоэффективны. В этой стадии наблюдается снижение двигательной активности и рефлекторных реакций. Артериальная гипотония нарастает на фоне тахикардии и довольно часто возникающих аритмий. Снижение минутного объема кровообращения сопровождается депонированием и уменьшением объема циркулирующей крови. Падение сердечного выброса и циркулятор-ная гипоксия вызывают гипоперфузии, нарушение реологических свойств крови и транскапиллярного обмена. Выход жидкости из сосудов в ткани вследствие повышения проницаемости сосудистых мембран вызывает сгущение крови и увеличение ее вязкости. Возникающие при кардиогенном шоке лактат-ацидоз и изменения реологических свойств крови приводит к стазу и образованию тромбов в микрососудах разных органов.
В тяжелых случаях шока развивается почечная и легочная недостаточность. Почечная недостаточность («шоковая почка») возникает вследствие перераспределения крови и редукции кровообращения, а также нарушения микроциркуляции в почках. Появление анурии или даже олигурии при кардиогенном шоке – крайне неблагоприятный прогностический признак. Нарушения микроциркуляции в легких вследствие возникновения микротромбов сопровождаются шунтированием крови на уровне легких; развиваются набухание альвеолярно-капиллярных мембран и интерстициальный отек («шоковое легкое»). Все это приводит к гипоксемии и повышению степени тяжести гипоксии. Указанные выше расстройства еще более нарушают функцию сердца, что проявляется снижением сократительной функции околоинфарктной зоны. В условиях нарастающей циркуляторной и респираторной гипоксии и ацидоза появляется ареактивность сосудов к прессорным агентам (катехоламинам, ангиотонину- II и др.).
Анафилактический шок. Данный вид шока является одной из наиболее тяжелых и опасных форм гиперчувствительности немедленного типа. Анафилактический шок может возникнуть при введении вакцин или лечебных сывороток, попадание в организм яда насекомых, действии ряда лекарственных препаратов. При появлении в организме аллергенов образуются антитела, после чего происходит взаимодействие между ними. Образовавшиеся комплексы аллерген – антитело при участии комплемента вызывают высвобождение или образование медиаторов аллергии, которые имеют важное значение в возникновении функциональных и морфологических проявлений аллергии.
Анафилактический шок развивается очень быстро. Для него характерна короткая эректильная фаза, проявляющаяся чувством страха, беспокойством и двигательным возбуждением. Часто возникают сильная головная боль, зуд кожи и потливость. Отчетливо, хотя и кратковременно, регистрируются артериальная гипертония и усиление внешнего дыхания. Уже в этом периоде возможно появление нарастающего чувства удушья с преимущественным затруднением выдоха (экспираторная одышка) вследствие бронхиолоспазма и гиперсекреции желез слизистой оболочки дыхательных путей. Возбуждение ЦНС при анафилактическом шоке может быть связано с гиперафферентацией, возникающей в результате раздражения разнообразных рецепторов сосудистого русла макромолекулами комплексов антиген – антитело, рецепторов кожи и слизистых оболочек, а также других тканей при действии на них медиаторов аллергии (гистамина, кининов, МРВ-А и др.). В торпидной стадии анафилактического шока наблюдается спутанность сознания, возможны судороги. Вследствие тяжелого бронхиолоспазма, возникающего под влиянием медиаторов аллергии, развиваются острая дыхательная недостаточность и асфиксия. Те же медиаторы, но особенно анафилатоксин (С3-, С5-компоненты комплемента), вызывают вазодилатацию и падение системного артериального давления. Наблюдаются депонирование крови, снижение венозного возврата к сердцу и ослабление его сократительной функции. Тяжелые нарушение возникают в микроциркуляторном отделе кровообращения. Снижение микроперфузии обусловлено падением тонуса и резким расширением артериол и снижением насосной функции сердца. В дальнейшем к этому присоединяется ухудшение реологических свойств крови: вследствие повышения проницаемости стенок микрососудов плазма выходит во внеклеточную среду, происходит сгущение крови и увеличение ее вязкости. Возникают сладжирование крови и микротромбозы. Наряду с этим в результате активации фибринолитической системы довольно часто развиваются висцеральные кровотечения. Все это в целом характерно для диссеминированного внутрисосудистого свертывания. Помимо респираторных и гемодинамических расстройств, при анафилактическом шоке довольно часто возникают тяжелые нарушения функций желудочно-кишечного тракта: спастические боли в области живота, парез кишечника и метеоризм, рвота и понос. Шок может усугубляться аллергическим отеком гортани, крапивницей, отеком Квинке и др.
Использованная литература
1. Патофизиология. Курс лекций./Под ред. П.Ф.Литвицкого. – М: Медицина, 1997. – 752 с.
2. Патологическая физиология. Учебник для студентов медицинских вузов./Под ред. Н.Н.Зайко. – Киев: Вища школа, 1985 – 575 с.
3. Саркисов Д.С., Пальцев М.А., Хитров Н.К. Общая патология. – М: Медицина, 1997 – 608 с.
4. Патологическая физиология. Сборник лекций в трех томах. /Под ред. А.П.Ястребова. – Екатеринбург, 1996.
5. Павлов А.Д., Глобиш В.И. Патофизиология обменных процессов. – Рязань, 1985. – 82 с.
6. Селье Г. Стресс без дистресса. – М: изд. «Прогресс», 1979. – 120 с.
7. Тигранян Р.А. Стресс и его значение для организма. – М: Наука, 1988. – 176 с.
РАЗДЕЛ 3. ПАТОЛОГИЯ ОРГАНОВ И СИСТЕМ
Тема 6. Патология системы внешнего дыхания
Острый бронхит — диффузное острое воспаление трахеобронхиального дерева.
Этиология острого бронхита: заболевание вызывают вирусы, бактерии, физические и химические факторы.
Предрасполагают к заболеванию охлаждение, курение табака, употребление алкоголя, хроническая очаговая инфекция в казофарингеальной области, нарушение носового дыхания, деформация грудной клетки.
Патогенез острого бронхита.
Повреждающий агент проникает в трахею и бронхи с вдыхаемым воздухом, гематогенным или лимфогенным путем. Острое воспаление может сопровождаться нарушением бронхиальной проходимости отечно-воспалительного или бронхоспастического механизма. Характерны набухание и гиперемия слизистой оболочки; на стенках бронхов и в их просвете слизистый, слизисто-гнойный или гнойный секрет; дегенеративные изменения реснитчатого эпителия. При тяжелых формах воспалительный процесс захватывает не только слизистую оболочку, но и глубокие ткани стенки бронхов.
Клиническая картина острого бронхита.
Бронхит инфекционной этиологии нередко начинается на фоне острого ринита, ларингита. При легком течении заболевания возникают саднение за грудиной, сухой, реже влажный кашель, чувство разбитости, слабость. Физикальные признаки отсутствуют или над легкими выслушиваются сухие хрипы на фоне жесткого дыхания. Температура тела субфебрильная или нормальная. Состав периферической крови не меняется. При среднетяжелом течении значительно выражены общее недомогание, слабость, характерны сильный, сухой кашель с затруднением дыхания и одышкой, боль в нижних отделах грудной клетки. Кашель постепенно становится влажным, мокрота приобретает слизисто-гнойный характер. Аускультативно выслушиваются жесткое дыхание, сухие и влажные мелкопузырчатые хрипы. Температура тела остается в течение нескольких дней субфебрильной. Выраженных изменений состава периферической крови нет. Тяжелое течение болезни наблюдается при поражении бронхиол (бронхиолит). Начало болезни острое. Лихорадка (38—39 °С), выраженная одышка (до 40 в 1 минуту), дыхание поверхностное. Лицо одутловатое, цианотичное. Мучительный кашель со скудной слизистой мокротой. Перкуторный звук с коробочным оттенком, дыхание ослабленное или жесткое, обильные мелкопузырчатые хрипы. Нарастают симптомы обструктивной эмфиземы. Отмечается лейкоцитоз, повышение СОЭ. Рентгенологически определяется усиление легочного рисунка в нижних отделах и в области корней легких.
Хронический бронхит — диффузное прогрессирующее поражение бронхов, связанное с длительным раздражением дыхательных путей вредными агентами, характеризующееся воспалительными и склеротическими изменениями в бронхиальной стенке и перибронхиальной ткани, сопровождающимися перестройкой секреторного аппарата и гиперсекрецией слизи, проявляющееся постоянным или периферическим кашлем с мокротой на протяжении не менее 3 месяцев в году в течение 2 и более лет, а при поражении мелких бронхов — одышкой, ведущей к обструктивным нарушениям вентиляции и формированию хронического легочного сердца.
Классификация хронических бронхитов
I. Клинические формы:
• хронический простой (необструктивный) бронхит, протекающий с постоянным или периодическим выделением слизистой мокроты и без вентиляционных нарушений;
• хронический гнойный (необструктивный) бронхит, протекающий с постоянным или периодическим выделением гнойной мокроты и без вентиляционных нарушений;
• хронический обструктивный бронхит, протекающий с выделением слизистой мокроты и стойкими обструктивными нарушениями вентиляции;
• хронический гнойно-обструктивный бронхит, сопровождающийся выделением гнойной мокроты со стойкими обструктивными нарушениями вентиляции;
• особые формы: геморрагический; фибринозный.
II. Уровень поражения:
• бронхит с преимущественным поражением крупных бронхов (проксимальный);
• бронхит с преимущественным поражением мелких бронхов (дистальный).
III. Течение:
• патентное;
• с редкими обострениями;
• с частыми обострениями;
• непрерывно рецидивирующее.
IV. Наличие бронхоспастического (астматического) синдрома.
V. Фаза процесса:
• обострение;
• ремиссия.
VI. Осложнения:
• эмфизема легких;
• кровохарканье;
• дыхательная недостаточность (с указанием степени);
• хроническое легочное сердце (компенсированное, декомпенсированное).
Этиология хронических бронхитов.
• Вдыхание поллютантов — содержащихся в воздухе примесей различной природы и химического строения, оказывающих вредное раздражающее действие на слизистую оболочку бронхов (табачный дым, пыль, токсические пары, газы и т. д.).
• Инфекция (бактерии, вирусы, микоплазмы, грибки).
• Эндогенные факторы — застойные явления в легких при недостаточности кровообращения, выделение слизистой оболочкой бронхов продуктов азотистого метаболизма при хронической почечной недостаточности.
• Неизлеченный острый бронхит.
Предрасполагающие факторы:
• нарушение носового дыхания;
• заболевания носоглотки — хронические тонзиллиты, синуситы, риниты;
• охлаждение;
• злоупотребление алкоголем;
• проживание в местности, где атмосфера загрязнена поллютантами (газами, пылью, парами кислот, щелочей и т. д.).
Патогенез хронических бронхитов.
Нарушение функции системы местной бронхопульмональной защиты. Развитие классической патогенетической триады — гиперкриния (гиперфункционирование бронхиальных слизистых желез, гиперпродукция слизи), дискриния (повышенная вязкость мокроты вследствие изменения ее физико-химических свойств и снижения ее реологии), мукостаз (застой в бронхах густой вязкой мокроты). Благоприятные условия для внедрения в бронхи инфекционных агентов. Развитие сенсибилизации к микробной флоре и аутосенсибилизации.
Основные механизмы бронхообструкции:
• бронхоспазм;
• воспалительный отек и инфильтрация бронхиальной стенки;
• гипер- и дискриния;
• гипотоническая дискинезия крупных бронхов и трахеи;
• коллапс мелких бронхов на выдохе;
• гиперпластические изменения слизистого и подслизистого слоев бронхов.
Клинические симптомы хронических бронхитов
I. Клинические проявления хронического необструктивного бронхита:
• Кашель с отделением слизисто-гнойной мокроты до 100—150 мл в сутки, преимущественно утром.
• В фазе обострения — слабость, потливость, при гнойном бронхите — повышение температуры тела.
• При гнойном многолетнем хроническом бронхите возможно развитие утолщений концевых фаланг («барабанные палочки») и утолщение ногтей («часовые стекла»).
• При перкуссии легких в случае развития эмфиземы перкуторный звук «коробочный» и ограничение дыхательной подвижности легких.
• При аускультации определяется жесткое дыхание с удлиненным выдохом, сухие свистящие и жужжащие хрипы, разнокалиберные влажные хрипы в зависимости от калибра бронхов.
II. Клинические проявления хронического обструктивного бронхита:
• Одышка, преимущественно экспираторного типа.
• Меняющийся характер одышки в зависимости от погоды, времени суток, обострения легочной инфекции.
• Затрудненный и удлиненный выдох по сравнению с фазой вдоха.
• Набухание шейных вен во время выдоха и спадение при вдохе.
• Затяжной малопродуктивный кашель.
• При перкуссии легких: «коробочный» звук, опущение нижней границы легких (эмфизема).
• При аускультации: дыхание жесткое с удлиненным выдохом, жужжащие, свистящие хрипы, которые могут быть слышны на расстоянии. Иногда прослушиваются лишь в положении лежа.
• Пальпация выдоха по Вотчану: удлинение выдоха и снижение его силы.
• Положительная проба со спичкой по Вотчану: больной не может погасить зажженную спичку на расстоянии 8 см от рта.
• При выраженном обструктивном синдроме возникают симптомы гиперкапнии: нарушения сна, головная боль, повышенная потливость, анорексия, мышечные подергивания, крупный тремор, в более тяжелых случаях — спутанность сознания, судороги и кома.
• Синдром дискинезии трахеи и крупных бронхов проявляется приступами мучительного битонального кашля с трудно отделяемой мокротой, сопровождающимися удушьем, иногда потерей сознания, рвотой.
Пневмония – острый воспалительный процесс в легких, вызванный первично или вторично неспецифической патогенной или условно патогенной микрофлорой с прорывом иммунных механизмов защиты и сопровождающийся поражением респираторных отделов паренхимы и интерстициальной ткани с обязательным накоплением в альвеолах экссудата, содержащего нейтрофилы.
Классификация пневмоний.
I. По этиологии (с указанием возбудителя):
• бактериальная;
• микоплазменная;
• вирусная;
• грибковая;
• смешанная.
II. По патогенезу:
• первичная;
• вторичная.
III. По наличию осложнений:
• неосложненная;
• осложненная (плеврит, абсцесс, бактериальный токсический шок, миокардит и т. д.).
Деление пневмоний на очаговую и паренхиматозную правомочно лишь при воспалительном процессе в легких, вызванном пневмококком. Затяжное течение пневмонии целесообразно отражать только при пневмококковой этиологии заболевания или при наличии в очаге поражения ассоциации микроорганизмов. При других формах пневмонии (стафилококковой, микоплазменной и др.) разрешение воспалительного процесса в легких нередко продолжается более 4 недель. Вторичной называют пневмонию, развитие которой последовало за заболеванием, патогенез которого непосредственно или опосредованно связан с бронхолегочной системой (ателектатическая, посттравматическая, аспирационная) или возникает на фоне иммунодефицитного состояния (СПИД, иммуносупрессорная терапия).
Особого внимания заслуживает выделение так называемых атипичных пневмоний, вызванных внутриклеточными возбудителями (микоплазмой, легионеллой, хламидией). Их особенность состоит в преобладании симптомов общей интоксикации, которые отодвигают на второй план легочные проявления, отсутствие инфильтративных изменений на рентгенограмме легких в первые дни болезни (интерстициальный тип). Течение таких пневмоний непредсказуемо: они могут протекать как малосимптомно, так и тяжело с развитием опасных для жизни осложнений. По локализации пневмонии подразделяют на одно- и двухсторонние, верхне-, средне- или нижнедолевые (или в соответствующих сегментах), а также прикорневые или центральные. Целесообразно отражать также степень тяжести острой пневмонии.
Этиология пневмоний.
Наиболее частыми возбудителями пневмонии являются пневмококки (от 30 % до 40 %), вирусы (около 10 %) и микоплазма (15—20 %). До настоящего времени почти у половины больных причина заболевания остается неизвестной.
Патогенез пневмоний.
Основные факторы:
• внедрение инфекции в легочную ткань чаще бронхогенным, реже гематогенным или лимфогенным путем;
• снижение функции системы местной бронхопульмональной защиты;
• развитие под влиянием инфекции воспаления в альвеолах и распространение его через межальвеолярные поры на другие отделы легких;
• развитие сенсибилизации к инфекционным агентам, формирование иммунных комплексов, взаимодействие их с комплементом, выделение медиаторов воспаления;
• повышение агрегации тромбоцитов, нарушения в системе микроциркуляции;
• активация перекисного окисления липидов, выделение свободных радикалов, дестабилизирующих лизосомы и повреждающих легкие;
• нервно-трофические расстройства бронхов и легких.
Клиника острой пневмонии, кроме общих симптомов данного заболевания, имеют отличительные черты, обусловленные этиологией воспалительного процесса в легких.
Пневмококковая пневмония протекает в двух морфологических формах: крупозной и очаговой.
I. Крупозная пневмония проявляется внезапным началом (больной называет день и час), потрясающим ознобом с повышением температуры тела до фебрильных цифр, кашлем (вначале сухим, а затем с вязкой ржавой мокротой), выраженной одышкой, болью в грудной клетке, сердцебиением. При осмотре: герпес на губах, подбородке, в области крыльев носа, одышка, отставание при дыхании грудной клетки на стороне поражения. В левом легком пристеночно и в междолевой щели сохраняются небольшие плевральные наложения, сосудистый рисунок в обоих легких нормальный. В начальной фазе (фаза накопления экссудата) — притупленно-тимпанический звук над очагом поражения, жесткое дыхание с удлиненным выдохом, начальная (необильная) крепитация, иногда на ограниченном участке — сухие и влажные хрипы. В фазе уплотнения — резкое усиление голосового дрожания, появление бронхофонии, дыхание не прослушивается, крепитация исчезает, нередко — шум трения плевры. В фазе разрешения — голосовое дрожание постепенно нормализуется, бронхофония исчезает, появляется crepetato redux (обильная, звучная на большом протяжении), звучные мелкопузырчатые хрипы, бронхиальное дыхание постепенно сменяется жестким, затем везикулярным. При исследовании сердечно-сосудистой системы — частый пульс, при тяжелом течении — слабого наполнения, аритмия, снижение артериального давления, глухость тонов сердца.
II. Очаговая пневмония характеризуется постепенным началом после предшествующей острой вирусной инфекции верхних дыхательных путей или трахеобронхита. Кашель с отделением слизисто-гнойной мокроты, слабость, потливость, иногда одышка, боли в грудной клетке при дыхании, повышение температуры тела. При перкуссии легких в случае крупноочаговой или сливной пневмонии — укорочение перкуторного звука, расширение корня легких на стороне поражения, при аускультации — жесткое дыхание с удлиненным выдохом, мелкопузырчатые хрипы, крепитация на ограниченном участке, сухие хрипы.
Стафилококковая пневмония.
Стафилококковая пневмония как самостоятельная нозологическая единица возникает только при бронхогенном характере инфицирования обычно после перенесенной вирусной инфекции. При гематогенном пути инфицирования стафилококковое поражение легких становится составной частью картины более тяжелого заболевания — сепсиса. Клиническая симптоматика стафилококковой пневмонии характеризуется особо тяжелым течением с признаками выраженной интоксикации (кашель со скудной мокротой типа «малинового желе», резкая общая слабость, нередко спутанное сознание). Физикальная картина характеризуется несоответствием объема поражения и тяжести состояния больного. Клинико-рентгенологически стафилококковая пневмония протекает в виде двух вариантов: стафилококковой деструкции легких и стафилококковой инфильтрации. В подавляющем большинстве случаев встречается стафилококковая деструкция легких. При рентгенологическом исследовании легких на фоне негомогенной инфильтрации легких определяются сухие полости деструкции с тонкими стенками (стафилококковые буллы). При динамическом рентгенологическом исследовании легких полости быстро возникают и быстро исчезают. При стафилококковой инфильтрации отмечается выраженная интоксикация и длительно сохраняющееся затемнение в легких при рентгенологическом исследовании (до 4—6 недель).
Фридлендеровская пневмония.
Фридлендеровская пневмония вызывается клебсиеллой и возникает у очень ослабленных больных. Заболевание развивается постепенно, с длительным продромальным периодом, характеризующимся лихорадкой, глухим кашлем и общим недомоганием. Спустя 3—4 дня в зоне инфильтрации появляются множественные полости распада с жидким содержимым.
Легионеллезная пневмония.
Болезнь легионеров (легионеллезная пневмония). Возникает как эпидемическая вспышка у лиц, имеющих постоянный контакт с землей, проживающих или работающих в помещениях с кондиционерами. Болезнь проявляется остро, высокой температурой тела, кожным и диарейным синдромами, артромегалией, выявляются очаговые инфильтраты с постоянно сохраняющейся тенденцией к нагноению и образованию эмпиемы.
Микоплазменная пневмония.
Клиническая картина характеризуется фебрильной температурой, мучительным сухим кашлем, переходящим во влажный, с отделением скудной слизисто-гнойной мокроты, ломотой в теле. Физикальная симптоматика очень скудная. При аускультации выслушиваются жесткое дыхание и локальные сухие или влажные звучные мелкопузырчатые хрипы. При рентгенологическом исследовании обнаруживается перибронхиальная и периваскулярная инфильтрация. В анализах крови выявляется значительное увеличение СОЭ при нормальном содержании лейкоцитов. Улучшение самочувствия отмечается при назначении антибиотиков тетрациклинового ряда.
Осложнениями пневмонии могут быть:
1 – легочными: плевральный выпот, эмпиемы плевры, деструкция легочной ткани, острый респираторный дистресс-синдром, острая дыхательная недостаточность;
2 – внелегочными: инфекционно-токсический шок, вторичная бактериемия, сепсис, перикардит, миокардит, нефрит.
Абсцесс легкого – гнойное расплавление легочной ткани в виде ограниченного очага (полости), окруженного воспалительным валиком (инфильтратом).
Специфического возбудителя легочных нагноений нет. Этиологическим фактором в развитии нагноительного процесса в легких является смешанная флора с преобладанием стрептококков. В ряде случаев заболевание бывает связано с аутоинфекцией микробами, являющимися сапрофитами верхних дыхательных путей. Эти микроорганизмы, попадая в легкие, становятся патогенными и могут вызвать нагноение различного характера и распространенности. Развитие нагноительного процесса в легких и его интенсивность зависят от реактивности легочной ткани и реакции всего организма. Пути проникновения инфекции в легкие различные. Чаще всего гнойный процесс развивается как исход пневмонии, а также при наличии бронхоэктазов – это группа так называемых вторичных абсцессов легких, когда преобладает бронхогенный путь распространения инфекции. Первичные абсцессы легких возникают остро при ранениях грудной клетки, аспирации инородных тел, после операции на верхних дыхательных путях, тонзилэктомии и др. Возможно развитие абсцесса гематогенным или лимфогенным путем, когда инфекция заносится в легкие из отдаленного гнойного очага в организме. Расплавление легочной ткани может быть и без участия микробов. Например, при распадающихся опухолях или инфарктах легкого может образоваться полость в результате нарушения кровообращения в определенном участке; в таких случаях омертвение легочной ткани предшествует нагноению.
По особенностям клинического течения заболевание разделяется:
1) по происхождению: острый абсцесс легкого и хронический абсцесс легкого (течение процесса свыше 2 месяцев);
2) по локализации: сегмент, сегменты, право- или левосторонние;
3) по осложнениям.
В остром абсцессе легкого выделяют период организации (до вскрытия полости – до 7 дней), который характеризуется острым началом (сухой надсадный кашель, озноб), сменой озноба на проливной пот (гектическая лихорадка), психическими нарушениями, одутловатостью лица, гиперемией щек, отставанием пораженной стороны грудной клетки при дыхании, локальным уплотнением перкуторного звука, жестким дыханием с бронхиальным оттенком. Период после вскрытия полости характеризуется внезапным отхождением гнойной зловонной мокроты полным ртом, падением температуры, уменьшением интоксикации, перкуторно над пораженным участком легкого определяется тимпанита, при аускультации дыхание амфорическое, влажные средне- и крупнопузырчатые звучные хрипы.
При хроническом абсцессе легкого у больных отмечается кашель со зловонной мокротой, кровохарканье, ознобы, потливость, одутловатость лица, диффузный цианоз, запах изо рта, пальцы в виде барабанных палочек, ногти в виде часовых стекол (признак гипоксии), при аускультации над пораженным участком выслушивается амфорическое дыхание, влажные мелкопузырчатые звучные хрипы.
Осложнениями абсцесса легкого являются:
· сепсис,
· пиопневмоторакс,
· медиастинальная и подкожная эмфизема,
· эмпиема плевры,
· легочное кровотечение,
· метастатический абсцесс головного мозга,
· легочное сердце.
Гангрена легкого – прогрессирующий некроз и ипохорозный (гнилостный) распад легочной ткани, не склонный к ограничению.
Возбудителями заболевания являются неклостридиальные анаэробы. Анаэробные бактерии проникают в легочную ткань, происходит активизация бактериальных экзотоксинов и их непосредственное воздействие на легочную ткань, прогрессирующий некроз легочной ткани, тромбоз сосудов в зоне поражения, нарушение формирования грануляционной ткани.
Основным проявлениями заболевания являются кашель со зловонной мокротой и фрагментами легочной ткани, гектический характер лихорадки, боль в грудной клетке, одышка, перкуторно в начале заболевания определяется расширяющаяся тупость; в период разгара – появление участков тимпанита вследствие образования полостей. При пальпации определяется болезненность над зоной поражения (симптом Кисслинга) и перкуссии (синдром Зауэрбруха), вследствие вовлечения в процесс плевры; пальпаторно – вначале усиление голосового дрожания, затем ослабление. Аускультативно выслушивается вначале бронхиальное дыхание, затем резкое ослабление дыхания.
Деструктивные заболевания легких
Эмфизема легких — заболевание, характеризующееся расширением воздушных пространств, расположенных дистальнее терминальных бронхиол, и сопровождающееся деструктивными изменениями альвеолярных стенок.
Классификация эмфиземы легких (Н. В. Путов, Г. П. Хлопотова, 1984 г.):
I. По патогенезу:
• первичная (идиопатическая, эссенциальная);
• вторичная (развивающаяся на фоне заболеваний легких).
II. По распространенности:
• диффузная;
• локализованная.
III. По морфологическим признакам:
• панацинарная — с поражением всего ацинуса;
• центрилобулярная — с поражением центральной части ацинуса;
• периацинарная — с поражением периферии ацинуса;
• иррегулярная (околорубцовая);
• буллезная.
IV. Особые формы:
• врожденная долевая эмфизема легких;
• синдром Макмода (эмфизема неясной этиологии, поражающая одно легкое).
Этиология эмфиземы легких.
В развитии первичной эмфиземы легких играет роль ряд факторов: вдыхание агрессивных токсичных аэрозолей, табачного дыма, нарушения легочной микроциркуляции, нарушение продукции и активности сурфактанта, нарушения обмена мукополисахаридов и генетический дефект эластина и коллагена в легких, нарушение физиологического равновесия в системе протеаз-ингибиторов, андрогенов — эстрогенов. Вторичную диффузную эмфизему легких связывают с хроническим бронхитом. При локализованных формах эмфиземы важную роль играет формирующийся в мелких бронхах клапанный механизм, ведущий к вздутию и перерастяжению участков легочной ткани и формированию булл.
Патогенез эмфиземы легких.
Основные патогенетические механизмы:
а) прогрессирующее уменьшение общей функционирующей поверхности легкого в результате деструкции межальвеолярных перегородок, что ведет к снижению диффузной способности легких и развитию дыхательной недостаточности;
б) изменение механических свойств легочной ткани, в результате чего мелкие бесхрящевые бронхи, лишенные эластической поддержки, спадаются во время выдоха с формированием характерного для эмфиземы механизма вторичной бронхиальной обструкции. Крупные буллы сдавливают и нарушают вентиляцию еще функционирующей легочной ткани и тем самым усугубляют дыхательные расстройства.
Клинические симптомы эмфиземы легких:
• Одышка, выраженность которой отражает степень дыхательной недостаточности.
• Кашель со слизистой или слизисто-гнойной мокротой (при хроническом бронхите).
• Расширенная бочкообразная грудная клетка, увеличенная в переднезаднем размере; поверхностное дыхание и участие в дыхании вспомогательной мускулатуры; у мужчин — уменьшение расстояния между щитовидным хрящом и рукояткой грудины; расширение межреберных промежутков и эпигастрального угла (больше 90 °С); опущение нижней границы легких и снижение дыхательной подвижности, «коробочный» перкуторный звук; ослабление везикулярного дыхания («ватное дыхание»), уменьшение абсолютной тупости сердца; глухость сердечных тонов.
• Надключичные ямки выпячены и заполнены расширенными верхушками легких.
• Больные выдыхают при сомкнутых губах, надувая щеки; при выраженной дыхательной недостаточности — цианоз, одутловатость лица.
Лабораторные данные при эмфиземе легких.
ОАК: при выраженной дыхательной недостаточности — эритроцитоз, увеличение содержания гемоглобина.
Инструментальные исследования при эмфиземе легких.
Рентгенологическое исследование — признаки эмфиземы легких, ЭКГ — отклонение электрической оси вправо, поворот сердца вокруг продольной оси по часовой стрелке, синдром трех S (выраженный зубец S в отведениях I—III); спирограмма — уменьшение ЖЕЛ, при хроническом обструктивном процессе — снижение РЖЕЛ и индекса Тиффно.
Бронхоэктатическая болезнь — приобретенное заболевание, характеризующееся, как правило, локализованным хроническим нагноительным процессом в необратимо измененных (расширенных, деформированных) и функционально неполноценных бронхах, преимущественно нижних отделов легких.
Классификация бронхоэктатической болезни (Н. В. Пустов, 1984 г.):
I. Формы расширения бронхов:
• цилиндрические;
• мешотчатые;
• веретенообразные;
• смешанные.
II. Состояние паренхимы пораженного отдела легкого:
• ателектатические;
• не связанные с ателектазом.
III. Клиническое течение:
• легкое;
• выраженное;
• тяжелое;
• осложненное.
IV. Распространенность процесса:
• односторонние,
• двусторонние. С указанием точной локализации изменений по сегментам.
Этиология бронхоэктатической болезни:
• Генетически обусловленная неполноценность бронхиального дерева.
• Условный этиологический фактор — микроорганизмы, вызывающие острые респираторные процессы у детей (пневмонии, коклюш).
Патогенез бронхоэктатической болезни.
Патогенез включает факторы, приводящие к развитию бронхоэктазий, и факторы, ведущие к их инфицированию.
К развитию бронхоэктазий приводят:
• обтурационный ателектаз;
• снижение устойчивости стенок бронхов к действию бронходилатирующих сил;
• развитие воспалительного процесса в бронхах в случае его прогрессирования ведет к дегенерации хрящевых пластинок, гладкой мышечной ткани с заменой фиброзной тканью и снижением устойчивости бронхов.
К инфицированию бронхоэктазов ведут следующие механизмы:
• нарушение откашливания;
• застой и инфицирование секрета в расширенных бронхах способствует дальнейшему расширению бронхов.
Клинические симптомы бронхоэктатической болезни.
Основные жалобы: кашель с отхождением гнойной мокроты неприятного запаха, особенно утром («полным ртом»), а также при принятии дренажного положения в количестве от 20 до нескольких сотен миллиметров; возможно кровохарканье, общая слабость, анорексия; повышение температуры тела.
При осмотре: бледность кожи, видимых слизистых оболочек, при развитии дыхательной недостаточности — цианоз, одышка; утолщение ногтевых фаланг («барабанные палочки») и ногтей («часовые стекла»); отставание детей в физическом и половом развитии. Физикальное исследование легких: отставание подвижности легких на стороне поражения; аускультативно-жесткое дыхание и притупление перкуторного звука, крупно- и среднепузырчатые хрипы над очагом поражения.
Лабораторные данные при бронхоэктатической болезни:
• ОАК: признаки анемии, лейкоцитоз, сдвиг лейкоцитарной формулы влево и увеличение СОЭ (в фазе обострения).
• Общий анализ мочи: протеинурия.
• Снижение содержания альбуминов, увеличение альфа-2- и гамма-глобулинов, а также сиановых кислот, фибрина, серомукоида в сыворотке крови в фазе обострения.
• Общий анализ мокроты: гнойная, при отставании — два или три слоя; в мокроте много нейтрофилов, эластических волокон, могут встречаться эритроциты.
Инструментальные исследования при бронхоэктатической болезни
Рентгенография легких: уменьшение объема пораженной части легкого, смещение средостения в сторону поражения, высокое стояние диафрагмы, усиление, деформация, ячеистость легочного рисунка, иногда интенсивное затемнение резко уменьшенной доли.
Бронхография: расширение бронхов IV, V порядка, их сближение, деформация.
Бронхоскопия: выявляется гнойный бронхит, уточняется источник кровотечения.
Спирография: рестриктивный или смешанный тип дыхательной недостаточности.
Пневмосклероз – избыточное разрастание соединительной ткани в легких, нарушающее их функцию.
К возникновению пневмосклероза могут привести как острые (очаговые и крупозные), так и хронические пневмонии, хронические бронхиты с частыми обострениями, бронхоэктатическая болезнь, а также абсцессы легких и пневмокониозы. Иногда пневмосклероз может быть самостоятельным, первичным заболеванием (синдром Хаммена – Рича). Наблюдается разрастание соединительной ткани как диффузного, так и очагового характера на месте пневмонии, а также по ходу бронха. Одновременно обнаруживаются эмфизема, бронхоэктазы и т.д.
Больные, страдающие пневмосклерозом, в анамнезе указывают на повторные пневмонии или частые обострения хронического бронхита. Очаговые пневмосклерозы диагностируются аускультативно и рентгенологически. Важными признаками являются наличие свистящих хрипов, значительное удлинение фазы выдоха и появление вен над ключицами. Могут быть и влажные звучные короткие хрипы. Перкуторно чаще всего определяется коробочный перкуторный звук. Очаговый пневмосклероз, если он не прогрессирует, не представляет непосредственной угрозы здоровья. Диффузный пневмосклероз аускультативно установить очень трудно, лишь иногда выслушиваются жестковатое дыхание и жужжащие сухие хрипы. К этому состоянию может присоединиться повышенная секреция слизистой бронхов. В связи с тем, что мокрота скапливается в участках пневмосклероза, кашля может и не быть; образуется стаз мокроты, развиваются бронхоэктазы. Легко развивается воспаление стенки бронха, переходящее на легочную ткань (перифокальное воспаление). Мокрота приобретает гнойный характер, обычно обладает запахом плесени, в ней обнаруживаются эластические волокна. Единственной возможностью освободиться от мокроты у больного пневмосклерозом является поиск оптимального положения тела, способствующего выделению мокроты и вызывающего кашель. При застое мокроты пневмосклероз будет давать частые обострения и по существу превратится в хроническую пневмонию Рентгенологически характерны усиление легочного рисунка и деформация бронхиального дерева за счет перибронхита и бронхоэктазов.
Прогноз при пневмосклерозе определяется прогрессированием процесса, дыхательной и сердечной недостаточностью.
Аллергические заболевания легких
Бронхиальная астма — хроническое рецидивирующее заболевание с преимущественным поражением бронхов, которое характеризуется их гиперреактивностью, обусловленной специфическими (иммунологическими) и (или) неспецифическими (неиммунологическими), врожденными или приобретенными механизмами, а основным (обязательным) признаком которого является приступ удушья и (или) астматический статус вследствие спазма гладких мышц бронхов, гиперсекреции, дискринии и отека слизистой оболочки бронхов.
Классификация бронхиальной астмы.
Традиционно выделяют:
• атопическую (экзогенную, аллергическую, иммунологическую);
• неатопическую (эндогенную, неиммуннологическую) бронхиальную астму.
По степени тяжести:
• легкое течение;
• течение средней тяжести;
• тяжелое течение.
Легкая степень характеризуется отсутствием классических приступов удушья. Симптомы затрудненного дыхания возникают менее 1—2 раз в неделю, носят кратковременный характер; медикаментозной терапии, как правило, не требуется. Ночной сон больного в этой стадии заболевания характеризуется пробуждением от респираторного дискомфорта менее 1—2 раз в год. Вне приступов состояние больного стабильное. При бронхиальной астме средней тяжести приступы купируются симпатомиметиками. Приступы по ночам регистрируются чаще двух раз в месяц. Приступы астмы тяжелого течения характеризуются частыми длительными обострениями с наличием осложнений, опасных для жизни, частыми ночными симптомами, снижением физической активности, наличием сохраняющихся симптомов в межприступный период.
Фазы течения бронхиальной астмы: обострение, ремиссия.
Этапы развития бронхиальной астмы.
I. Наличие у практически здоровых людей врожденных и (или) приобретенных биологических дефектов и нарушений:
а) местного и общего иммунитета;
б) системы «быстрого реагирования» (тучные клетки, макрофаги, эозинофилы, тромбоциты);
в) мукоцилиарного клиренса;
г) эндокринной системы и т. д.
Клиническая реализация биологических дефектов ведет к развитию бронхиальной астмы.
II. Состояние предастмы. Это признак угрозы возникновения клинически выраженной бронхиальной астмы.
III. Клинически оформленная бронхиальная астма — после первого приступа астмы или астматического статуса.
Этиология и патогенез бронхиальной астмы.
Общим патогенетическим механизмом, присущим разным формам бронхиальной астмы, является изменение чувствительности и реактивности бронхов, определяемое по реакции проходимости бронхов в ответ на воздействие физических и фармакологических факторов. Считают, что у 1/3 больных астма имеет аутоиммунное происхождение. В возникновении аллергических форм астмы играют роль небактериальные и бактериальные аллергены. Наиболее изучены аллергические механизмы возникновения астмы, в основе которых лежат IgE и IgG обусловленные реакции. Центральное место в патогенезе «аспириновой» астмы отводят лейкотриенам. При астме физического усилия нарушается процесс теплоотдачи с поверхности дыхательных путей.
Клинические симптомы бронхиальной астмы.
Предастма.
Первая группа симптомов предастмы — острые, рецидивирующие или хронические бронхиты и пневмонии с явлениями обструкции бронхов. Вторая группа — наличие внелегочных проявлений аллергии: вазомоторного ринита, крапивницы, отека Квинке. Третья группа — наследственное предрасположение к различным аллергическим заболеваниям, что выявляется при сборе семейного анамнеза. Четвертая группа — эозинофилия крови и мокроты.
Бронхиальная астма.
В развитии приступа бронхиальной астмы различают три периода:
1 – Период предвестников наступает за несколько минут, часов, иногда дней до приступа и проявляется следующими симптомами: вазомоторными реакциями со стороны слизистой носа, чиханием, зудом глаз, кожи, приступообразным кашлем, головной болью, нередко изменениями настроения.
2 – Период разгара (удушья) имеет следующую симптоматику. Появляется чувство нехватки воздуха, сдавления в груди, выраженная экспираторная одышка. Вдох становится коротким, выдох — медленным, сопровождается громкими, продолжительными, свистящими хрипами, слышными на расстоянии. Больной принимает вынужденное положение, сидит, наклонившись вперед, опираясь локтями на колени, ловя ртом воздух. Лицо бледное, с синюшным оттенком. Крылья носа раздуваются при вдохе. Грудная клетка в положении максимального вдоха, в дыхании участвуют мышцы плечевого пояса, спины, брюшной стенки. Межреберные промежутки и надключичные ямки втягиваются при вдохе. Шейные вены набухшие. Во время приступа наблюдается кашель с очень трудно отделяемой мокротой, над легкими определяется перкуторный звук с тимпаническим оттенком, нижние границы легких опущены, подвижность легочных краев ограничена, на фоне ослабленного дыхания, особенно на выдохе, слышно много сухих свистящих хрипов. Пульс учащен, слабого наполнения, тоны сердца приглушены. Приступ удушья может перейти в астматический статус.
3 – Период обратного развития имеет разную продолжительность. После приступа больные хотят отдохнуть, некоторые из них испытывают голод, жажду.
Осложнения бронхиальной астмы:
• легочные — эмфизема легких, легочная недостаточность, ателектаз, пневмоторакс;
• внелегочные — дистрофия миокарда, легочное сердце, сердечная недостаточность.
Рак легкого.
Рак — это группа опухолей, произрастающих только из клеток эпителиальной ткани (слизистые оболочки, кожа). Из покровного эпителия чаще раки локализуются на коже, на губах, в бронхах, в пищеводе, во влагалищной порции шейки матки, в мочевом пузыре. Из железистого эпителия наиболее частая локализация рака в желудке, кишечнике, молочной железе, поджелудочной железе, печени, теле матки, бронхах, слюнной железе. Любая злокачественная опухоль обладает рядом особенностей:
• способность к автономному (самостоятельному), быстрому нерегулируемому организмом росту;
• способность к метастазированию (по лимфатическим и кровеносным сосудам);
• местно отмечается разрушающий инфильтрирующий рост.
Классификация рака легкого.
I. По локализации:
- прикорневой (центральный);
- периферический.
II. По характеру роста:
- экзофитный (эндобронхиальный);
- эндофитный (экзо- и перибронхиальный).
III. По макроскопической картине:
- массивный узловой;
- полипообразный;
- разветвленный;
- маленький рак Пенкоста;
- пневмониеподобный.
IV. По гистологическому строению:
- плоскоклеточный (эпидермоидный) рак;
- недифференцированный анапластический рак (мелкоклеточный, крупноклеточный);
- аденокарцинома.
К факторам риска возникновения онкологических заболеваний относятся следующие:
• хронические стрессы, отрицательные эмоции, депрессия, которые способствуют возникновению рака. Стрессорным гормоном является кортизол;
• курение является причинным фактором около 30 % всех форм злокачественных опухолей. Хотя не у каждого курильщика развивается рак легкого, но частота возникновения составляет 90 %. Пассивные курильщики за один час поглощают 2,3 мг золы. Курение повышает частоту рака гортани, глотки, пищевода. У курящих отцов и матерей дети в 4 раза чаще болеют раком;
• употребление алкоголя способствует возникновению рака пищевода, желудка, толстой и прямой кишки. Он увеличивает риск возникновения рака и цирроза печени;
• нарушения питания. Чрезмерное употребление продуктов, содержащих большое количество насыщенных жирных кислот (сало, жирное мясо, сливки, сливочное масло), увеличивает риск возникновения рака кишечника, молочной железы, поджелудочной железы, яичников и прямой кишки. Ограничение жира может замедлять развитие опухолевого процесса;
• к канцерогенам относятся мышьяк, асбест, тяжелые металлы, полихлорвинил. Сильные канцерогены обнаружены в выхлопных газах автомобилей. Недостаток витаминов усиливает действие канцерогенов.
Все эти факторы называют канцерогенными. Под действием канцерогенов происходит экзофитно-эндобронхиальное поражение железистого эпителия крупных бронхов (1-го, 2-го, реже 3-го порядка), переходит на легочную ткань (чаще справа, с локализацией в верхних долях, реже в нижних и средних долях), органы средостения, регионарные лимфатические узлы. Просвет бронхов закрывается, происходит нарушение его проходимости (обтурация бронха). Уменьшается соответствующая доля легкого, происходит смещение органов средостения в сторону поражения. Развивается вторичный воспалительный процесс в зоне поражения, идет разрушение легочных кровеносных сосудов с развитием кровоизлияния и внелегочное метастазирование с поражением печени, кости, головной мозг. Раком легкого мужчины заболевают в 7—10 раз чаще, чем женщины, главным образом, за счет курения. Предрасполагающими факторами являются перенесенный ранее туберкулез, очаги пневмосклероза.
Рак, поражающий главные, долевые и сегментарные бронхи, называется центральным, опухоль, возникшая в бронхах меньшего калибра, — периферическим раком (шаровидный, пневмониеподобный, рак верхушки легкого (Пенкоста). Встречаются атипические формы (медиастенальная, мозговая, костная и т. д.).
Для центрального рака характерны следующие симптомы:
· кашель, связан с развитием реактивного бронхита, затем ателектаза легких, перифокальной пневмонии, распадом легочной ткани, характер кашля приступообразный, коклюшеподобный, вначале сухой, впоследствии со слизисто-гнойной мокротой, с примесью крови (сгустки, легочное кровотечение)
· одышка нарастает постепенно, отмечается при развитии ателектаза легких, массивном выпоте в плевру, сдавлении органов средостения;
· лихорадка, связана с воспалительным процессом, раковой интоксикацией, развитием осложнений;
· боль в грудной клетке с поврежденной стороны, интенсивность болей нарастает при прорастании опухоли в стенку грудной клетки, поражении ребер, позвонков метастазами;
· кожные проявления в виде дерматита, зуда кожи;
· развивается слабость, быстрая утомляемость;
· похудение;
· западение грудной стенки на стороне поражения.
При периферическом раке легкого симптоматика скудна.
В анализе крови: повышение СОЭ, гипохромная анемия. При исследовании мокроты можно обнаружить клетки опухоли.
Для раннего выявления большое значение имеет флюорография, рентгенография легких, бронхоскопия.
Метастазирование.
Первые лимфогенные метастазы возникают в перибронхиальных и бифуркационных лимфатических узлах, затем - шейных, забрюшинных. Среди гематогенных метастазов для рака легкого характерны метастазы в печень, головной мозг, кости (особенно в позвонки) и надпочечники.
Осложнения:
- ателектазы легких;
- кровотечение;
- абсцедирующая пневмония;
- гангрена легкого.
Основы предупреждения болезней органов внешнего дыхания.
1. Профилактика острого бронхита:
· устранение возможного этиологического фактора острого бронхита: запыленность, загазованность рабочих помещений, переохлаждение, курение, злоупотребление алкоголя, хроническая и очаговая инфекция в дыхательных путях;
· меры, направленные на повышение сопротивляемости организма к инфекции: закаливание, витаминная пища.
2. Профилактика острой пневмонии заключается в:
· санации очагов хронической инфекции,
· закаливании организма,
· избегании переохлаждения,
· диспансерное наблюдение (пневмониям наиболее подвержены лица детского и пожилого возраста, страдающие хроническими заболеваниями сердца, легких, почек, желудочно-кишечного тракта, с иммунодефицитом, постоянно контактирующие с птицами, грызунами).
Основные задачи диспансеризации:
• Ранняя диагностика болезни.
• Максимально раннее исключение внешних причинных факторов — прекращение курения, исключение вредных производственных факторов, санация хронических очагов инфекции, восстановление носового дыхания.
• Подбор индивидуальной поддерживающей терапии на фоне немедикаментозных методов лечения.
• Организация специальных методов лечения в амбулаторных условиях (аэрозольтерапия, эндобронхиальная санация). Диагностика функциональных нарушений дыхания, в том числе ранняя диагностика бронхиальной обструкции. Меры по предупреждению рецидива хронического бронхита предполагают закаливание организма (регламентированные занятия спортом), предупреждение возникновения вирусной инфекции (прием аскорбиновой кислоты, ремантадина, интерферона).
3. Профилактика бронхиальной астмы основана на:
· мероприятиях социального характера: улучшение условий труда и быта, уменьшение степени загрязнения воздуха, отказ от курения и использования аллергенных веществ, относящихся к предметам бытовой химии,
· медицинского характера: своевременное лечение острых и хронических заболеваний органов дыхания, разумное назначение лекарственных препаратов.
Комплексная программа профилактики бронхиальной астмой включает в себя:
• образовательную программу пациентов;
• динамический контроль тяжести заболевания и адекватности проводимой терапии с помощью клинических и функциональных исследований;
• мероприятия, исключающие воздействие на организм больного «виновного аллергена», или контроль причинных факторов;
• разработку плана медикаментозной терапии;
• профилактику обострения и разработку плана его лечения;
• динамическое наблюдение за больным.
4. Основные принципы профилактики эмфиземы:
• раннее выявление и непрерывное лечение больных с хроническим бронхитом;
• применение средств и методов, улучшающих бронхиальную проходимость, предупреждающих метаболические осложнения, респираторный ацидоз, улучшающих артериализацию крови.
Основы лечения болезней органов внешнего дыхания.
1. Восстановление проходимости дыхательных путей:
1.1. Выбор отхаркивающих препаратов зависит от типа кашля:
· при сильном сухом изнуряющем кашле назначают препараты, угнетающие кашлевой рефлекс (кодеин, текодин, дионин, глауцин);
· при продуктивном кашле с хорошим отхождением мокроты показаны вещества, усиливающие ее выделение: отхаркивающие (термопсис, терпингидрат и т.д.) и бронхолитические средства (эуфиллин, теофиллин);
· при неизмененных реологических свойствах мокроты, но сниженном мукоцилиарном транспорте используют производные теофиллина и симпатомиметиков (теолонг, теопек, синекод);
· при высоких вязкоэластических свойствах мокроты применяют производные тиолов (ацетил-цистеин или мукосольвин), протеолитические ферменты (трипсин, химотрипсин),
· при значительных адгезивных показателях назначают вещества, стимулирующие образование сурфактанта (бромгексин-бисольван, лазолван-амброксол) и регидратата секрета (минеральные соли, эфирное масло).
1.2. Купирование бронхоспазма достигается назначением препаратов с бронходилатирующим эффектом:
· симпатомиметиков селективного или преимущественно селективного действия (изадрин, сальбутамол, беротек, вентолин);
· ингибиторов фосфодиэстеразы (производные теофиллина);
· холинолитиков (платифиллин, атропин);
· глюкокортикостероидов, в основном ингаляционного действия (бекотид, бекломет, пульмикорт), не подавляющих функцию коры надпочечников.
1.3. Улучшение дренажной функции легких:
· бронхолитики в сочетании с муколитиками (амброксол, мукодин, бромгексин, бронхикум и др.);
· дренажный массаж;
· лечебная дыхательная гимнастика.
2. Рациональная антибактериальная терапия.
Антибиотики могут вводиться внутрь, парентерально и в виде аэрозолей. Выбор антибиотикотерапии был бы проще, если бы была возможность сразу установить характер возбудителя. Принимая во внимание, что основными возбудителями острой первичной пневмонии считаются вирусы, пневмококки, микоплазма и легионелла, ее терапию начинают с пенициллина (суточная доза — 3,0—6,0 млн ЕД внутримышечно) или полусинтетических его препаратов (ампициллина по 4,0—6,0 г). При лечении больного в амбулаторных условиях предпочтение отдают пероральным цефалоспоринам 2-го поколения (цефаклор, цефуроксим натрия), которые активны в отношении большинства грамположительных и грамотрицательных палочек.
Эмпирическая антибактериальная терапия внебольничных пневмоний (рекомендации Европейского респираторного общества):
· нетяжелая «пневмококковая пневмония»»: амоксициллин по 1,0 г внутрь каждые 8 ч в течение 8 дней, прокаин-пенициллин по 1,2 млн ЕД внутримышечно каждые 12 ч в течение 8 дней;
· нетяжелая атипичная пневмония: макролиды внутрь в течение 2-х недель;
· тяжелая пневмония, вероятно, пневмококковой этиологии: пенициллин С (бензил-пенициллин) по 2 млн ЕД внутривенно каждые 4 ч;
· тяжелая пневмония неизвестной этиологии: цефалоспорины III поколения + эритромицин (рифампицин);
· аспирационная «анаэробная» пневмония: клиндамицин по 600 мг внутривенно каждые 6 ч, амоксициллин + клавуланат (амокисклав) по 2,0 г внутривенно каждые 8 ч.
Похожие работы
... новые возможности, которые возникали с появлением новых методов исследования, позволяли делать открытия, радикально менявшие взгляды на патологию, начинать качественно новые этапы её развития. Патологическая анатомия использует три основных метода исследования — вскрытие трупов людей, умерших от болезней (1); микроскопические методы изучения тканей (2); эксперимент, позволяющий моделировать на ...
... , а не просто отсутствие болезни или физических дефектов. Здоровье- оптимум функционирования организма как целостной системы. Определение ключевых понятий общей патологии: Нозология - учение о болезни. Болезнь - качественно новое по отношению к здоровью состояние организма, возникающее при нарушении генетической программы или действии болезнетворных факторов среды, характеризующееся нарушением ...
... и Sadov четко и ясно обозначили имеющееся противоречие во взглядах на исследуемые экстремальные состояния, в мире так и не существует единой позиции по этому вопросу. Например, российские ученые склонны считать острую массивную кровопотерю геморрагическим шоком, а не коллапсом, в то время как за рубежом понятия «шок» и «коллапс» не разграничиваются. Этому способствует и тот факт, что в настоящее ...
... что и пневмосклероз, и приобретенные бронхоэктазы развиваются вследствие дискретного (разового, однократного) патологического процесса, не противоречит тому, что больные с хронической бронхолегочной патологией предрасположены к такому течению. Закономерной стадийности нет. Осложнения. Вздутие легких - следствие обструктивного процесса в мелких бронхах. Самыми характерными признаками хронической ...

0 комментариев