Навигация
Запись данных
3. Запись данных.
Для начала записи данных в меню Регистратор выберите команду Пуск.
2.2 Анкетирование
Для реализации цели работы – исследования возможностей цифровой лаборатории «Архимед» для применения в урочной и внеурочной деятельности по химии нами был применен метод анкетирования. Анкетирование – метод сбора первичного материала в виде письменного опроса респондентов с целью сбора информации с помощью анкеты о состоянии тех или иных сторон воспитательного процесса, отношения к тем или другим явлениям [12].
Мы использовали сплошное (опрос всех представителей выборки) анкетирование. По числу респондентов и типов контактов респондентов анкетирование‚ проводимое нами следует отнести к групповому (несколько респондентов) и очному (в присутствии исследователя-анкетёра) соответственно. Вопросы, предложенные учащимся были составлены в закрытой (содержит полный набор возможных ответов) и открытой (ответ целиком и полностью формулирует сам респондент) форме (Приложение 7, 8). В закрытых вопросах респонденту предлагалось выбрать один или несколько из данных ему вариантов (количество выборов оговаривалось после формулировки вопроса). В наших анкетах для закрытых вопросов предъявлялись поливариантная (предусматривает список ответов) или шкальная (с ранжированием степени убеждения, отношения, впечатления и т.д.) форма вариантов ответов.
Глава 3. Результаты и их обсуждение
Проект «Информатизация системы образования» (2004-2009 гг.), подготавливаемый сегодня Министерством образования РФ, направлен на реализацию принятой Правительством РФ «Концепции модернизации российского образования».
Анализ состояния дел в области информатизации, проведенный в ходе подготовки проекта, выявил острую нехватку специалистов, способных грамотно и эффективно использовать цифровые образовательные ресурсы на практике.
В связи с этим в рамках проекта планируется: создание новых моделей подготовки будущих учителей и переподготовка уже практикующих.
Результатом такой масштабной подготовки должен стать специалист – учитель, которой сможет эффективно применять возможности цифровых учебно-методических материалов, в частности, цифровой лаборатории «Архимед» в урочной и внеурочной деятельности.
Целью нашей работы было исследование возможностей цифровой лаборатории «Архимед» для применения в урочной и внеурочной деятельности по химии. В последующих частях работы мы предлагаем разработанные нами или модифицированные с пособия разработчика опыты для учителей, использующих в своей работе (планирующих использование) цифровую лабораторию «Архимед».
3.1 Методические разработки опытов, с использованием цифровой лаборатории «Архимед», для урочной деятельности
В предлагаемых работах используется, входящие в состав цифровой лаборатории «Архимед» карманный компьютер (КПК), устройство NOVA5000, TriLink, датчик рН и датчик температуры.
Тема: Растворение как физико-химический процесс. Растворимость.
Типы растворов
Тема «Растворение как физико-химический процесс. Растворимость. Типы растворов» изучается учащимися, обучающимися по УМК О. С. Габриеляна в 8 классе, в разделе 7. «Растворение. Растворы. Свойства растворов электролитов» (Приложение 1,2). Одним из элементов физико-химического аспекта процесса растворения является поглощение или выделение тепла при растворении.
Опыт № 1. Экзотермические реакции. Растворение гидроксида натрия и безводного сульфата меди в воде [26, 38]
Цель работы: Проследить за изменением температуры при растворении твёрдого гидроксида натрия и безводного сульфата меди в воде.
Форма работы: фронтальная (демонстрационный эксперимент).
Оборудование и реактивы: химический стакан на 250 мл, магнитная мешалка, ёмкость из пенопласта (без дна), крышка к стакану из пенопласта, едкий натр (10 г), датчик температуры, цифровая лаборатория «Архимед».
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 500
Ход опыта: Налейте в химический стакан, погружённый в емкость (без дна) из пенопласта, 25 мл воды и поставьте на магнитную мешалку. Закройте ёмкость крышкой, с вставленной воронкой и датчиком температуры
Включите магнитную мешалку. Опустите в химический стакан, через воронку 10 г едкого натра (или 10 г безводного сульфата меди). Начните измерения. Повторите опыт 3 раза.
Результаты измерений: зарисовать полученные графики зависимости температуры от времени при растворении гидроксида натрия и безводного сульфата меди в воде в тетрадь.
Опыт № 2. Эндотермические реакции. Растворение нитрата аммония в воде [38]
Цель работы: Проследить за изменением температуры в процессе растворения кристаллов нитрата аммония в воде.
Форма работы: фронтальная (демонстрационный эксперимент).
Оборудование и реактивы: химический стакан на 250 мл, магнитная мешалка, ёмкость из пенопласта (без дна), крышка к стакану из пенопласта, 2,5 г твёрдого нитрата аммония, 25 мл водопроводной воды, датчик температуры, цифровая лаборатория «Архимед».
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 500
Ход опыта: Налейте в химический стакан, погружённый в емкость (без дна) из пенопласта 25 мл воды и поставьте на магнитную мешалку. Закройте ёмкость крышкой, с вставленной воронкой и датчиком температуры (рис. 2). Включите магнитную мешалку. Начинайте регистрацию данных. Опустите в химический стакан 2,5 г нитрата аммония при включённой мешалке. Следите за изменением температуры. Повторите опыт 3 раза.
Результаты измерений: зарисовать полученный график зависимости температуры от времени при растворении нитрата аммония в воде в тетрадь (рис. 3).
Тема: Тепловой эффект химической реакции
Тема «Тепловой эффект химической реакции» изучается учащимися, обучающимися по УМК О. С. Габриеляна в 11 классе, в разделе 2. «Строение веществ и их свойства» (Приложение 3).
Опыт № 1. Эндотермические реакции. Понижение температуры раствора при растворении некоторых солей в воде [39]
Цель работы: Проследить за изменением температуры при растворении ряда солей в воде. Отметить, какая соль даст наибольшее понижение температуры.
Форма работы: фронтальная (демонстрационный эксперимент).
Оборудование и реактивы: химический стакан на 250 мл, ёмкость из пенопласта (без дна), крышка к стакану из пенопласта, нитрат калия, нитрат аммония, тиосульфат натрия, дистиллированная вода, датчик температуры, цифровая лаборатория «Архимед».
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 500
Ход опыта: Налейте в химический стакан, погружённый в емкость (без дна) из пенопласта 50 мл воды и поставьте на магнитную мешалку. Закройте ёмкость крышкой, с вставленной воронкой и датчиком температуры (рис.2). Включите магнитную мешалку, начинайте растворять в воде 20-25 г соли, включив при этом регистратор данных. Опыт с каждой солью повторяют 3 раза. Отметьте, какая соль даст наибольшее понижение температуры.
Результаты измерений: зарисовать полученные графики зависимости температуры от времени при растворении нитрата аммония в воде в тетрадь.
Опыт № 2. Аддитивность теплоты реакции. Закон Гесса [38]
Цель работы: Проверить на практике выполнение закона Гесса (Формулировка закона: сумма энтальпий отдельных этапов реакции должна равняться полному изменению энтальпии всей реакции), используя возможности цифровой лаборатории «Архимед».
Форма работы: фронтальная (демонстрационный эксперимент).
Оборудование и реактивы: химический стакан на 250 мл, ёмкость из пенопласта (без дна), крышка к стакану из пенопласта, магнитная мешалка, 1 М раствор едкого натра, 1 М раствор соляной кислоты, 0,5 М раствор соляной кислоты, дистиллированная вода, датчик температуры, цифровая лаборатория «Архимед».
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 500
Ход опыта: Налейте в химический стакан, погружённый в емкость (без дна) из пенопласта 100 мл воды и поставьте на магнитную мешалку. Закройте ёмкость крышкой, с вставленной воронкой и датчиком температуры (рис. 2). Включите магнитную мешалку и перемешивайте воду до тех пор, пока во всём объёме химического стакана не установится температура, приблизительно равная комнатной. Начинайте регистрацию данных.
Реакция №1. Добавьте в химический стакан 2 г кристаллического гидроксида натрия и сразу закройте крышкой. Включите магнитную мешалку. Следите на экране за температурой до прекращения её изменения. Остановите регистрацию, нажав кнопку «Стоп» на панели инструментов. Повторите эксперимент 3 раза. Высчитайте среднее. Полученный результат (температура в конце опыта) занесите в тетрадь.
Реакция №2. Повторите реакция растворения, используя вместо воды 100 мл 0,5 М раствора соляной кислоты. Повторите эксперимент 3 раза. Высчитайте среднее. Полученный результат (температура в конце опыта) занесите в тетрадь.
Реакция №3. Налейте в химический стакан, погружённый в емкость (без дна) из пенопласта 50 мл 1 М раствора соляной кислоты и поставьте на магнитную мешалку. Закройте ёмкость крышкой, с вставленной воронкой и датчиком температуры (рис.2). Включите мешалку и перемешивайте 1 М раствор соляной кислоты до тех пор, пока во всём объёме химического стакана не установится температура, приблизительно равная комнатной. Начинайте регистрацию данных. Добавьте в химический стакан 50 мл 1 М раствора едкого натра. Включите магнитную мешалку. Следите на экране за температурой до прекращения её изменения. Остановите регистрацию, нажав кнопку «Стоп» на панели инструментов. Повторите эксперимент 3 раза. Высчитайте среднее. Полученный результат (температура в конце опыта) занесите в тетрадь.
Результаты измерений: высчитайте тепловой эффект каждой из трёх реакций и проверьте соответствие полученного вами результата закону Гесса (сумма энтальпий отдельных этапов реакции должна равняться полному изменению энтальпии всей реакции)
Опыт № 3. Теплота сгорания [38]
Цель работы: Определить теплоту сгорания магниевой стружки.
Форма работы: фронтальная (демонстрационный эксперимент).
Оборудование и реактивы: химический стакан на 250 мл, ёмкость из пенопласта (без дна), крышка к стакану из пенопласта, магниевая стружка (1,5 г), оксид магния (3 г), 1М раствор соляной кислоты (500 мл ), магнитная мешалка, датчик температуры, цифровая лаборатория «Архимед».
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 500
Ход опыта: Налейте в химический стакан, погружённый в емкость (без дна) из пенопласта 100 мл 1 М раствора соляной кислоты и поставьте на магнитную мешалку. Закройте ёмкость крышкой, с вставленной воронкой и датчиком температуры (рис. 2). Начинайте регистрацию данных.
Реакция №1: начните перемешивать в чашке раствор соляной кислоты (до достижения постоянной температуры). Добавьте в химический стакан 1 г порошка оксида магния. Следите по графику за температурой до прекращения её изменения. Остановите регистрацию, нажав кнопку «Стоп», на панели инструментов. Повторите эксперимент 3 раза. Высчитайте среднее. Полученный результат (температура в конце опыта) занесите в тетрадь.
Реакция №2: повторите предыдущее исследование, используя 0,5 г магниевой стружки вместо порошка оксида магния. Повторите эксперимент 3 раза. Высчитайте среднее. Полученный результат (температура в конце опыта) занесите в тетрадь.
Опыт № 4. Тепловой эффект сгорания топлива [38]
Цель работы: Определить и сравнить между собой тепловые эффекты сгорания различных видов топлива: парафин и этанол, используя возможности цифровой лаборатории «Архимед».
Форма работы: фронтальная (демонстрационный эксперимент).
Оборудование и реактивы: химический стакан из термостойкого стекла, весы, мерный цилиндр, вода, стеклянная палочка для перемешивания, свеча, спиртовка, спички, датчик температуры, цифровая лаборатория «Архимед».
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 200
Ход опыта: Определите массу химического стакана для воды. Добавьте в него 100 мл воды. Определите массу свечи до начала эксперимента. Закрепите сосуд с водой в кольцевом кронштейне. Поместите температурный датчик в воду так, чтобы он не касался дна сосуда. Перемешайте воду в сосуде и добейтесь постоянной температуры во всём объёме сосуда. Начинайте регистрацию данных. Зажгите свечу. В процессе нагревания воды продолжайте её перемешивать. Погасите свечу, когда температура достигнет 40 0С. После того, как температура перестанет расти, остановите регистрацию. По окончании эксперимента определите массу свечи. Замените свечу спиртовкой и повторите эксперимент с 200 мл воды. Не забудьте определить массу спиртовки до её заполнения этанолом. Закройте спиртовку металлической пластинкой перед тем, как потушить её, и остудите её до комнатной температуры. Определите массу горелки с остатками этанола. Эксперимент повторяют 3 раза.
Тема: Среда водных растворов. Водородный показатель
Тема «Среда водных растворов. Водородный показатель» изучается учащимися, обучающимися по УМК О. С. Габриеляна в 11 классе, в разделе 2. «Строение веществ и их свойства» (Приложение 3).
Опыт № 1. Растворение гидроксида натрия в воде [38]
Цель работы: Проследить за изменением изменением рН при растворении твёрдого гидроксида натрия в воде.
Форма работы: фронтальная (демонстрационный эксперимент).
Оборудование и реактивы: химический стакан на 250 мл, магнитная мешалка, крышка к стакану из пенопласта, едкий натр (10 г), датчик рН, цифровая лаборатория «Архимед».
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 500
Ход опыта: Налейте в химический стакан, погружённый в емкость (без дна) из пенопласта, 25 мл воды и поставьте на магнитную мешалку. Закройте ёмкость крышкой, с вставленной воронкой и датчиком рН (рис.2). Включите магнитную мешалку. Опустите в химический стакан, через воронку 10 г едкого натра. Начните измерения рН. Повторите опыт 3 раза.
Результаты измерений: зарисовать полученный график зависимости рН от времени при растворении гидроксида натрия в воде в тетрадь( рис. 4).
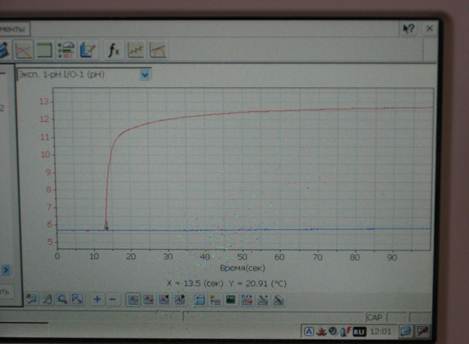
Рис. 4 - Пример графика зависимости рН от времени при растворении гидроксида натрия в воде
Тема: Реакции ионного обмена
Тема «Реакции ионного обмена» изучается учащимися, обучающимися по УМК О. С. Габриеляна в 11 классе, в разделе 2. «Строение веществ и их свойства» (Приложение 3).
Опыт № 1. Реакции нейтрализации. Взаимодействие гидроксида натрия с соляной кислотой [38]
Цель работы: проследить за изменением рН и температуры при прохождении реакции нейтрализации, используя возможности цифровой лаборатории «Архимед».
Форма работы: фронтальная (демонстрационный эксперимент).
Оборудование и реактивы: химический стакан на 250 мл, бюретка на 25 мл, магнитная мешалка, штатив, крышка к стакану из пенопласта, цифровая лаборатория «Архимед»; раствор фенолфталеина, 0,1 М раствор едкого натра, 0,1 М раствор соляной кислоты, датчик температуры, датчик рН.
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 500
Ход опыта: В химический стакан наливают 25 мл 0,1н. раствора соляной кислоты, добавляют 2-3 капли раствора фенолфталеина. Закрывают стакан крышкой из пенопласта. В стакан, через отверстие в крышке, помещают рН- метр и датчик температур, а также носик бюретки, предварительно заправленной 0,1 М раствором едкого натра. Стакан помещают на магнитную мешалку
Далее одновременно начинают добавлять по каплям 0,1 М раствор едкого натра и включают магнитную мешалку. Отмечаем момент изменения окраски раствора в стакане (до розовой). Опыт повторяют 3 раза.
Результаты: зарисовать график зависимости рН и температуры от времени при прохождении реакции нейтрализации в тетрадь
Тема: Окислительно-восстановительные реакции
Тема «Окислительно-восстановительные реакции» изучается учащимися, обучающимися по УМК О. С. Габриеляна в 11 классе, в разделе 2. «Строение веществ и их свойства» (Приложение 3).
Опыт №1. Изменение температуры при окислительно-восстановительных реакциях. Взаимодействие хлорида меди с алюминием [38]
Цель работы: Проследить за изменением температуры в процессе окислительно-восстановительной реакции, используя возможности цифровой лаборатории «Архимед».
Форма работы: фронтальная (демонстрационный эксперимент).
Оборудование и реактивы: химический стакан на 250 мл, магнитная мешалка, крышка к стакану из пенопласта, хлорид меди (крист.) массой 2,5г, алюминиевая фольга, 25 мл водопроводной воды, датчик температуры, цифровая лаборатория «Архимед».
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 500
Ход опыта: Налейте в химический стакан, погружённый в емкость (без дна) из пенопласта, 25 мл воды и поставьте на магнитную мешалку. Закройте ёмкость крышкой, с вставленной воронкой и датчиком температуры (рис.2).
Включите магнитную мешалку Опустите в химический стакан 2,5 г. хлорида меди. Добавьте алюминиевой фольги. Начинайте регистрацию данных. Повторите опыт 3 раза.
Результаты измерений: зарисовать график зависимости температуры от времени при окислительно-восстановительной реакции в тетрадь.
Тема: Гидролиз неорганических веществ
Тема «Гидролиз. Гидролиз неорганических веществ» изучается учащимися, обучающимися по УМК О. С. Габриеляна в 11 классе, в разделе 2. «Строение веществ и их свойства» (Приложение 3).
Опыт № 1. Влияние температуры на степень гидролиза ацетата натрия [26]
Цель работы: Проследить за изменением степени гидролиза ацетата натрия и реакции среды в зависимости от изменения температуры, используя возможности цифровой лаборатории «Архимед».
Форма работы: фронтальная (демонстрационный эксперимент).
Оборудование и реактивы: химический стакан на 250 мл, ёмкость для стакана из пенопласта (без дна), крышка к стакану из пенопласта, раствор фенолфталеина, 0,1 н. раствор ацетата натрия, электроплитка, датчик температуры, датчик рН, цифровая лаборатория «Архимед».
Настройка параметров измерения:
1) частота измерений – каждую секунду;
2) число замеров – 1500
Ход опыта: В химический стакан налейте 25 мл 0,1 М раствора ацетата натрия и добавьте несколько капель раствора фенолфталеина (из расчёта, что на 1-2 мл раствора ацетата натрия необходимо 1-2 капли фенолфталеина). Закройте химический стакан крышкой с вставленными датчиками температуры и рН. Поставьте химический стакан на электроплитку. Начинайте регистрацию данных и наблюдайте за изменением окраски раствора. Раствор будет становиться малиновым (рН будет расти) по мере повышения температуры, так как при нагревании гидролиз усиливается. Опыт повторяется 3 раза.
Результаты измерений: построить график зависимости рН и температуры от времени при прохождении реакции гидролиза. Сделать вывод об изменении степени гидролиза ацетата натрия в зависимости от температуры.
Похожие работы
... литературе, студентам, изучающим русскую литературу в вузах. 2) Лингафонный кабинет предназначен для активного обучения иностранным языкам под наблюдением преподавателя с применением современных технических средств. Мультимедийные лингафонные кабинеты, которыми оснащаются современные школы, представляют собой последнее слово в технике и технологиях. Тип оборудования – встраиваемое или настольное ...
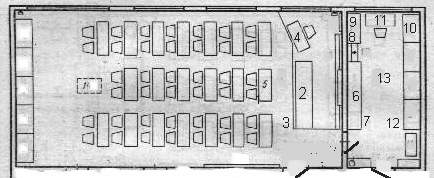
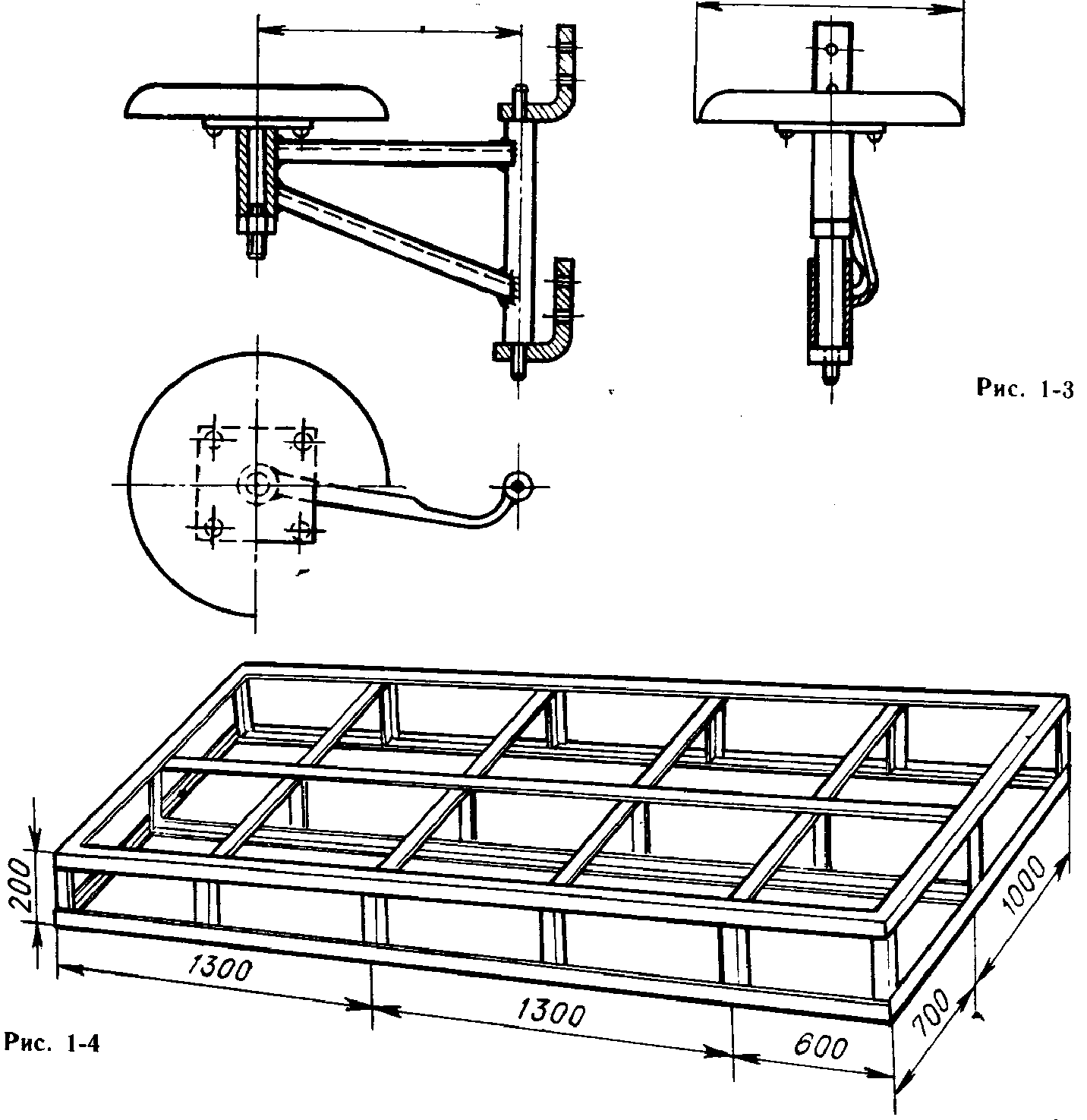
... школы. Мебель кабинета физики. Особенности оснащения и оборудования кабинета физики сельской школы. Рабочее место ученика и учителя в кабинете физики сельской школы. Кабинет физики в условиях разноуровневого обучения. Системы освещения и затемнения кабинета. Экскурсия в кабинет физики городской школы. 4. Работа заведующего кабинетом физики (5ч.) Права и обязанности заведующего кабинетом физики. ...
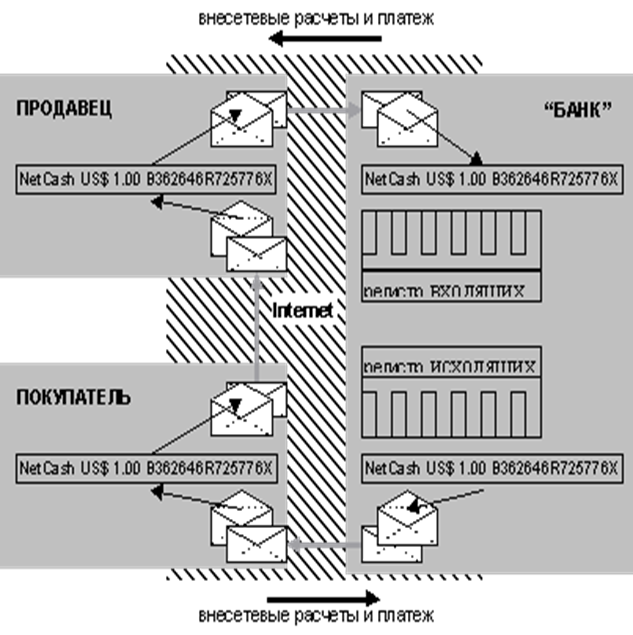
... " и т.п.), продвинутые платежные средства (такие, как цифровая наличность или цифровые чеки) фактически, с технологической точки зрения и есть реализация сложных криптографических протоколов. До недавнего времени (точнее, до середины 70-х гг.) вопроса об использовании фирмами и гражданами криптографии обычно не возникало. Однако, распространение быстродействующей вычислительной техники, с одной ...
... приборы (рычажные весы, электроскоп и др.); -работы, выполняемые на приборах, выпускаемых промышленностью. Классификация взята из [1]. В своей книге [2] С.Ф. Покровский показал, что домашние опыты и наблюдения по физике, проводимые самими учащимися: 1)дают возможность нашей школе расширить область связи теории с практикой; 2)развивают у учащихся интерес к физике и технике; 3)будят ...




0 комментариев