Навигация
Кг Cu входят в х кг CuFeS2
23 кг Cu входят в х кг CuFeS2
Х = 66,32 кг
Зная количество и состав халькопирита, найдем сколько серы и железа связано в халькопирите
183,4 кг CuFeS2 содержат 64 кг S
66,32 кг CuFeS2 содержат х кг S
Х = 23,14 кг
Количество железа в халькопирите
183,4 кг CuFeS2 содержат 64 кг Fe
66,32 кг CuFeS2 содержат х кг Fe
Х = 20,18 кг
Количество железа в пирите
25,5 – 20,18 = 5,32 кг
С этим количеством железа связано серы
55,8 кг Fe – 64 кг S
5,32 кг Fe – х кг S
Х = 6,10 кг
Количество пирита
5,32 + 6,10 = 11,42 кг
Остальная серы находится в элементарном состоянии
33 – 23,14 – 6,10 = 3,76 кг
По данным расчета составляем таблицу 1 рационального состава медного сырья.
Таблица 1 - Рациональный состав медного сырья, % CuFeS2
| Минералы | Cu | Fe | S | SiO2 | CaO | MgO | Al2O3 | прочие | всего |
| CuFeS2 | 23 | 20,18 | 23,14 | 66,32 | |||||
| FeS2 | 5,32 | 6,10 | 11,42 | ||||||
| S2 | 3,76 | 3,76 | |||||||
| Пустая порода | 2,0 | 0,5 | 0,5 | 5,2 | 10,3 | 18,5 | |||
| всего | 23 | 25,5 | 33,0 | 2,0 | 0,5 | 0,5 | 5,2 | 10,3 | 100 |
3.2. Обжиг медных концентратов в кипящем слое
Обжиг ведем на дутье, обогащенным кислородом до 35%. Степень десульфуризации при обжиге принимаем 55%, температуру обжига 8500С. Расчет ведем на 100 кг шихты.
Определим количество серы, диссоциирующей при обжиге.
По реакции
2CuFeS2 => Cu2S + 2 FeS + S образуется
S своб 66,32.32 / 366,7 = 5,79 кг
FeS 66,32.175,7 / 366,7 = 31,78 кг
Cu2S 66,32.159 / 366,7 = 28,75 кг
По реакции
FeS2 => FeS + S образуется
S своб 11,42.32 / 119,85 = 3,05 кг
FeS 11,42.87,85 / 119,85 = 8,37 кг
Всего выделится свободной серы
5,79 + 3,05 = 8,84 кг
При 55% десульфуризации в газы перейдет серы
33,0.0,55 = 18,15 кг
В том числе 3,76 кг за счет окисления свободной серы концентрата и за счет окисления FeS
18,15 – 8,84 – 3,76 = 5,55 кг
Образуется сернистого ангидрида
18,15.2 = 36,3 кг
Принимаем, что в процессе обжига сернистое железо окисляется до Fe3O4 по реакции
3FeS + 5 O2 = Fe3O4 + 3 SO2
На практике наряду с образованием Fe3O4 может происходить образование FeO и Fe2O3
Количество окислившегося FeS
5,55.263,5 / 96 = 15,23 кг
В огарке останется сернистого железа
31,78 + 8,37 – 15,23 = 24,92 кг
Для окисления FeS потребуется кислорода
15,23.160 / 263,5 = 9,25 кг
Результаты расчетов сводим в таблицу 2.
Таблица 2 – Рациональный состав огарка
| Соединение | Cu2S | FeS | Fe3O4 | Всего | ||||
| кг | % | кг | % | кг | % | кг | % | |
| Cu Fe S SiO2 CaO MgO Al2O3 О2 Прочие | 23 5,75 | 79,9 20,1 | 15,84 9,08 | 63,56 36,44 | 9,66 3,72 | 72,2 27,8 | 23 25,5 14,83 2,0 0,5 0,5 5,2 3,72 10,3 | 26,88 29,81 17,33 2,34 0,58 0,58 6,08 4,35 12,05 |
| Итого | 28,75 | 100 | 24,92 | 100 | 13,38 | 100 | 85,55 | 100 |
Выход огарка 85,55%.
Для определения материального баланса обжига рассчитаем количество серы и состав отходящих газов. Для окисления элементарной серы по реакции
S + О2 = SО2
Потребуется кислорода
(8,84 + 3,76).32 / 32 = 12,6 кг
Образуется при этом сернистого ангидрида
12,6.2 = 25,2 кг
Всего кислорода с учетом окисления сернистого железа потребуется
12,6 + 9,25 = 21,85 кг
Количество дутья при содержании кислорода 35% составит
22,4.21,85.100 / (35.32) = 43,7 м3
Азота в этом дутье будет
43,7.65 / 100 = 28,41 м3
Состав отходящих газов
кг м3 % (об)
SO2 36,3 12,7130,91
N2 40,5828,4169,09
Для проверки проделанных расчетов составляем материальный баланс обжига (таблица 3).
Таблица 3 - Материальный баланс обжига
| Статьи баланса | Всего, кг | В том числе | ||||||
| Cu | Fe | S | породы | прочие | О2 | N2 | ||
| Загружено Шихты Воздуха | 100 62,43 | 23 | 25,5 | 33 | 8,2 | 10,3 | 21,85 | 40,58 |
| Итого | 162,43 | 23 | 25,5 | 33 | 8,2 | 10,3 | 21,85 | 40,58 |
| Получено Огарка Газов | 85,55 76,86 | 23 | 25,5 | 14,83 18,17 | 8,2 | 10,3 | 3,72 18,13 | 40,58 |
| Итого | 162,43 | 23 | 25,5 | 33 | 8,2 | 10,3 | 21,85 | 40,58 |
Похожие работы
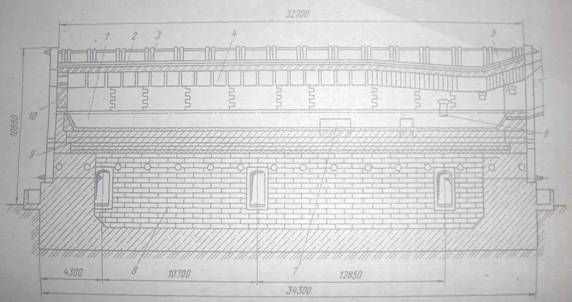
... возможность их очистки и использования в сернокислотном производстве из за низкого содержания в них сернистого ангидрида (2,5 /о). 2.2 Тепловой и температурный режимы работы Отражательная печь для плавки на штейн является агрегатом непрерывного действия с относительно постоянными во времени тепловым и температурным режимами работы. В ней осуществляется технологический процесс, состоящий из ...
... в сульфидных расплавах, где активность платиновых металлов очень невелика. Поэтому в процессе конвертирования в шлаковую фазу в очень незначительных количествах переходит платина (<0.5%), палладий (<0.5%), родий (<1.0%), иридий (<1.0%). Более того, конвертные шлаки перерабатываются в обеднительных печах, поэтому общие потери благородных металлов при конвертировании сравнительно малы ...
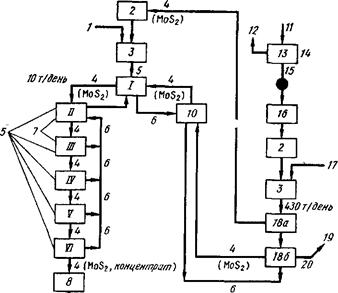
... из отработанных катализаторов и химических остатков [16]. 3.3 Молибден из колошниковой пыли плавильных печей Этот процесс, разработанный X. Кастанья, предназначен для выделения молибдена в виде молибденовой кислоты из отходов, в частности, из отработанных катализаторов, содержащих носитель - у-оксид алюминия и молибден в виде оксида или сульфида. Процесс включает обработку отходов ...
... . Благодаря неуклонному росту цен никель, он стал более привлекательным для инвесторов – еще одна из причин, по которой государство очень заинтересовано в поддержке развития сырьевой базы медно-никелевой промышленности. Но, есть и другая сторона, возможно, теперь основные покупатели никеля – производители нержавеющей стали – посчитают, что текущая цена слишком высока, и перейдут на его заменители ...




0 комментариев