Навигация
7. Напряжение разложения
Напряжение разложения – это наименьшая величина внешней электродвижущей силы, приложенной к электродам электролизера, при которой начинается длительный электролиз. При инертном аноде напряжение разложения глинозема по реакции:
Al2O3 ↔ 2Al + 1 1/2O2
составляет 2,19 В. При угольном аноде напряжение разложения Аl2O3 по реакции:
2Al2O3 + 3C ↔ 4Al + 3CO2, составляет1,167 В и по реакции: Al2O3 + 3C ↔ 2Al + 3CO
напряжение разложения составляет 1,034 В.
Экспериментальные значения напряжения разложения, полученные на промышленных электролизерах в результате изменения обратной электродвижущей силы составляют 1,37-1,78 В.
При промышленных анодных плотностях тока около 1 А/см2 о. э. д. с. находятся в пределах 1,4-1,8 В. Величина о. э. д. с. и перенапряжение растет с увеличение плотности тока и уменьшается с повышение температуры и увеличением активности углеродистого материала анода. Величины обратимых напряжений разложения других компонентов электролита – AlF3, NaF, MgF2, CaF2 – значительно выше напряжения разложения глинозема и соответственно равны 3,97; 4,37; 4,61; и 5,16 В.
8. Механизм электролиза криолито-глинозенмых расплавов (КГР)
В расплаве электролита присутствуют ионы (+) и (-).
Na+; AlF3(-3) AlF4(-); Al+3,
F(-) Ca+2 Mg+2; O2-2,
Al2O3 ↔ 2Al++1 ½ О2 –
Со и СО2
В то же время при взаимодействии Со и СО2
При электролизе ток переносит всеми ионами, но в соответствии с величиной разряда потенциалов на электроде будут разряжаться
ионы Al и O2
катод Al+3 + 3e → Al
анод 2O-2 4e + C → CO2 60%
анод C + CO2 = 2CO 40%
Катодный процесс представляется разрушением оксифторидных анионов с выделением алюминия и обогащением прикатодного слоя ионами. В прикатодном слое накапливаются ионы, необходимые для образования фтористого натрия и алюминия натрия.
В нормально работающем промышленном электролизе электролит постоянно находится в движении. Он циркулирует за счет конвективных потоков, движения анодных газов и катодного металла. В этом движении электролит перемешивается, и избыток фтористого натрия и алюминия натрия в прикатодном слое и фтористого алюминия в прикатодном слое исчезает, восстанавливается первоначальный состав электролита:
6NaF + Na3AlO3 + 4AlF3 ↔ 3Na3AlF6 + Al2O3.
Однако электролит постепенно обедняется глиноземом. Конечным результатом процесса является расходование 1 моля глинозема.
При электролизе алюминия параллельно с основным процессом идут побочные (на катоде, на аноде), которые осложняют нормальный ход электролиза, снижается выход алюминия, повышается расход электроэнергии, снижается стойкость футеровочных материалов и другое.
Побочный процесс на катоде осложняется двумя явлениями: растворением алюминия и выделением на катоде натрия. Растворимость алюминия в электролите увеличивается с повышением температуры электролита и содержания в нем фтористого натрия. Растворенный алюминий в процессе электролиза переносится к аноду и к поверхности электролита, где он окисляется анодными газами и кислородом воздуха:
3AlF+3CO2=AlF3+3CO+Al2O3;
3AlF+3CO=AlF3+C=Al2O3.
Эти реакции обуславливают потерю алюминия при электролизе, обогащение анодных газов окисью углерода и появления в электролите очень мелких частиц углерода.
Другое осложнение катодного процесса – это разряд катионов Na+, который всегда содержится в алюминии при его производстве. Количество выделившегося натрия зависит от криолитового отношения (КО) электролита. При снижении КО с 3 до 2,5 содержание натрия снижается в 2,5 раза. При температуре электролита выше 10000С каждые 100С приводят к росту содержания натрия на 0,001%. Содержание натрия увеличивается также во время анодных эффектов.
Таким образом, чтобы обеспечить минимальный разряд натрия и наибольший выход алюминия, необходимо поддерживать низкую температуру электролита (955-9600С),- КО=2,6-2,8 и не допускать большего числа анодных эффектов.
Существуют и другие побочные процессы: анодный эффект, образование в ванне карбонада алюминия Al4C3, также различные примеси, которые попадают с сырьем в электролизер (окислы железа, кремния, кальция, титана, сульфаты, фосфаты и т.д.).
9. Анодный эффект положительные и отрицательные действия
Периодически возникающий искровой анодный разряд, наблюдаемый на аноде при электролизе криолито-глиноземного расплава, называется анодным эффектом. На практике называют - «вспышками». Вспышки возникают при снижении концентрации глинозема в электролизе от 1 – 1,5%. При этом рабочее напряжение на электролизе резко поднимается – с 4,2-4,3 до 25-30 В.
Поскольку анодный эффект связан с обеднением электролита глиноземом, то добавка новой порции глинозема и перемешивание электролита быстро устраняет анодный эффект и восстанавливается нормальный ход электролиза в пределах нормы 4,3-4,5V.
Возникновение анодного эффекта происходит из-за ухудшения смачиваемость подошвы анода расплавленным электролитом вследствие уменьшения содержания глинозема:
Al2O3 в электролите до 1-1,5%.
Когда электролит хорошо смачивает анод, газообразные продукты электролиза не могут удержаться на подошве анода и выделяются из электролиза в виде пузырьков. С уменьшением содержания глинозема в электролите отрыв пузырьков от подошвы затруднен, что увеличивает сопротивление и на электролизере И- увеличивается с 4,5 V до 25-30 V. Мелкие пузырьки сливаются в большие и оттесняют электролит от подошвы анода, постепенно образуя сплошную газовую прослойку между анодом и электролитом. В результате этого плотность тока на тех участках, где еще идет ток, резко возрастает, увеличивается сопротивление прохождению электрического тока, возрастает напряжение на ванне и возникает анодный эффект.
Анодный эффект бывает:
тусклые – до 15V
средние – до 15-25V
ясные – 25 и вышеV
Анодный эффект играет положительную и отрицательную роль в электролизе Al.
Положительная роль анодного эффекта – дает возможность контролировать нормальную работу электролизера.
Допустимая чистота (А.Э.) – 0,8-1,0 а.э. в сутки. Считается я, что при возникновении анодного эффекта полируется подошва анода, очищается от неровностей, от пены, растворяется осадок на подине.
Отрицательная роль анодного эффекта – это потери Al. При каждом анодном эффекте сгорает 1кг. наработанного металла, перерасход электроэнергии при А.Э. расходуется 150-160 кВч., дополнительный расход фторсырья, дополнительный расход анодной массы. Несет ущерб – 5,2$. Происходит перегрев электролита, увеличиваются потери фторсолей в результате испарения.
С увеличением плотности тока возможность возникновения анодного эффекта возрастает. Анодную плотность тока, при повышении которой наступает анодный эффект называют критической (d кр).
Величина критической плотности тока зависит от многих факторов: фтористый натрий улучшает смачиваемость, поэтому с увеличением содержания его в электролите критическая плотность тока возрастает. Также, плотность тока возрастает при увеличении содержания глинозема. При повышении температуры электролита смачиваемость анода также улучшается. Добавки в электролит фтористого кальция и фтористого магния понижают критическую плотность тока, способствуют учащению вспышек.
Анодные эффекты, которые не удается ликвидировать обычными способами, и которые продолжаются до нескольких часов, называются негаснущими. Они возникают из-за появления, не растворенного глинозема в электролите, которые ухудшают смачиваемость угольного анода. Негаснущие эффекты возникают чаще всего во время выливки или сразу после выливки алюминия из ванн, работающих на сильно кислом электролите и с низким его уровнем, с большими глиноземистыми осадками на подине и длинными подовыми настылями, уходящими под анод.
10. Расчет производительности электролизера. Расчет выхода по току. Расчет выхода по энергии. Расчет удельного расхода электроэнергии. Влияние различных факторов на выход по току
Как известно, количество алюминия (обозначим Рт), которое теоретически может быть получено в процессе электролиза за определенный промежуток времени t, определяется по закону Фарадея.
Рт = 0,336 гр * I * t
0,336 гр – электрохимический эквивалент равен количеству граммов алюминия полученного на катоде при прохождении силы тока в 1А в течении одного часа.
На практике же вследствие некоторых утечек тока и вторичных процессов (в частности, растворения алюминия в электролите и последующего взаимодействия растворения алюминия с анодными газами) количество получаемого алюминия (обозначим Рп) всегда меньше этой величины.
Отношение количества металла, фактически полученного при электролизе, к его теоретически ожидаемому количества за то же время называют выходом по току. Выход по току обозначают
ήт =Рф / Рт * 100%.
Выход по току при получении алюминия на мощных электролизерах с верхних токоподводом обычно составляет 0,82-0,85 (82-85%). Зная выход по току и силу тока на серии, можно рассчитать суточную производительность электролизера по формуле
P = 8,04 * l * ήт / 1000 кг/ сутки.
Например, производительность электролизера на силу тока 160 000 А и при выходе по току 0,82 в сутки составит:
Р = 8,04 * (160 000 * 0,82) / 1000 = 1055 кг.
Выход по току – один из основных показателей, определяющих количество произведенного алюминия и расход электроэнергии на его получение. По этому показателю судят о качестве всей работы электролизного цеха, корпуса, бригады и электролизера.
По фактической величине выхода по току видно, что 15-18% от теоретического количества получаемого алюминия теряется.
К основным причинам непроизводительного расхода электроэнергии и снижению выхода по току относятся:
- утечки электрического тока в землю (при нарабатывании алюминия, ток проходит через электролит одного электрода ванны к другому, но некоторая часть проходит, не участвуя в электролизе, что называется утечками тока).
- утечки в результате технологических нарушений (потеря тока через конус на подошве анода при контакте его с зеркалом металла. Куски анода, скопление угольной пены в междуполюсном пространстве).
- электролиз окислов кремния, железа, меди и других, более электроположительных, чем алюминий, элементов. (эти примеси, при попадании в электролит с сырьем повышают расход электроэнергии и загрязняют алюминий).
- снижение выхода по току в следствие растворения его в электролите и последующего взаимодействия растворенного алюминия с анодными газами и кислородом воздуха.
На величину этих потерь и на величину выхода по току оказывают влияние следующие факторы:
- температура электролита;
- межполюсное расстояние;
- плотность тока;
- состав электролита;
- качество обслуживание электролизеров.
На практике часто пользуются показателем расхода электроэнергии, называемым выходом по энергии. За выход по энергии принимают количество алюминия, полученное на каждый киловатт-час затраченной электроэнергии (ήэн = г/кВч = 0,336 *ήT/ Vср * 103), т. е. выход по энергии прямопропорционален выходу по току и обратно пропорционален среднему напряжению на ванне.
Удельный расход электроэнергии
W = V cp * 103 / 0,336 * ήт кВч/т
V ср – среднее напряжение, чем оно больше , тем больше расход электроэнергии.
Vср = Vраб + ∆Иаэ + ∆И корпусной шинковки.
Расход электроэнергии W может быть определен как частное от деления количества затраченной электроэнергии на полученное при этом количестве Al.
A = Y * V * t * 10-3
P = 0,336 * Y * t * ήт * 10-6
W = Y * V * t * 10-3 / 0,336 * Y * t * ήт * 10-6 =
= V * 10-3 / 0,336 * ήт = H1 * 3 *10-3 / 0,336 * 88% =
= 4300 / 0,336 * 0,88 = 4300/ 29,568 = 14 543кВч/т, при 4,5 = 15219 кВч/т
Похожие работы
... 11,9 11,5 16,6 медь 9,8 15,5 16,4 Выпуск алюминия высокой чистоты, % марок: А995 47,8** 3,5 2,1 А99 30,4 67,1 54,2 А97 8,3 21,5 43,7 А95 10,4 7,9 — ниже А95 3,1 — — * Показатели производства алюминия высокой чистоты. ** Сортность по электролизерам без расшихтовки. Основным фактором, снижающим выход по току, помимо прямых потерь тока ...
... 17-25 кг/т алюминия, что на ~ 10-15 кг/т выше по сравнению с результатами для песчаного глинозёма. В глинозёме, используемом для производства алюминия, должно содержаться минимальное количество соединений железа, кремния, тяжелых металлов с меньшим потенциалом выделения на катоде, чем алюминий, т.к. они легко восстанавливаются и переходят в катодный алюминий. Нежелательно также присутствие в ...
... В случае применения самообжигающегося анода, часть анодной массы выбывает из процесса в виде летучих составляющих ее коксование. При материальном расчете определяют производительность электролизера и расход сырья на производство алюминия. производительность электролизера (Р), при силе тока J = 155А и принятом выходе по току = 86% составляет: где 0,3354 - электрохимический эквивалент для ; - ...
... другое соотношение входящих в состав примесей железа и кремния. Буква Е в марке АЕ означает, что алюминий данной марки предназначается для производства электропроводов. Дополнительным требованием к свойствам алюминия является низкое электросопротивление, которое для проволоки, изготовленной из него, должно быть не более 0.0280 ом мм м при 20 C. Алюминий применяют для производства из него изделий ...

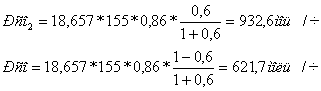
0 комментариев