Навигация
Вариант – переаминирование кислот (фермент - трансамидаза)
1 вариант – переаминирование кислот (фермент - трансамидаза)
α-кетоглутаровая кислота + а/к → L-глутаминовая кислота + α-кетокислота;
2 вариант – восстановительное аминирование (фермент - глутаматдегидрогеназа)
α-кетоглутаровая кислота + NH4+ + НАДН → L-глутаминовая кислота + Н2О + НАД+
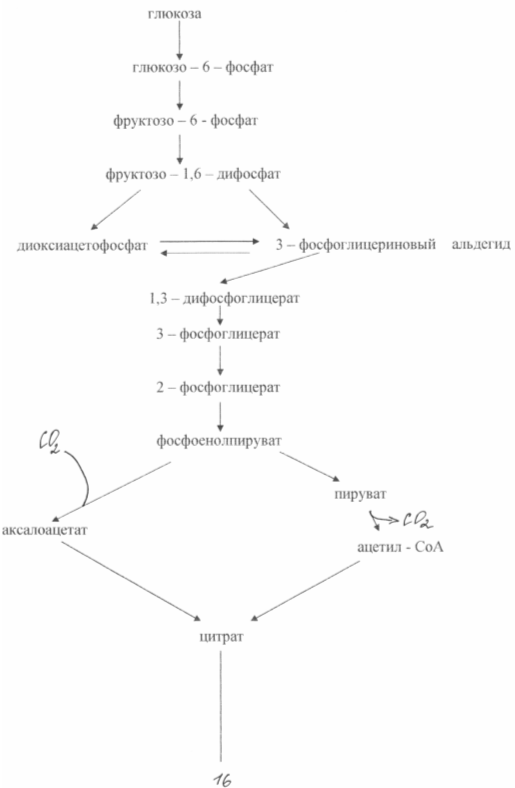
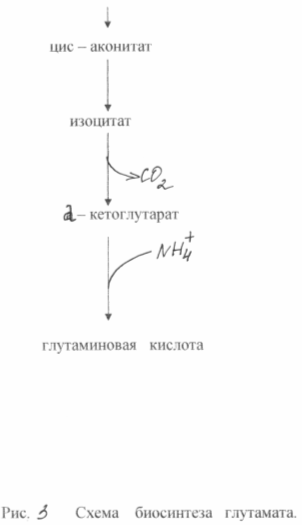
В каждом из этих процессов α-кетоглутаровая кислота играет роль предшественника.
Для осуществления любого из этих превращений необходимы источники α-кетоглутарата и соответствующей ферментной системы. Первую из этих задач решают с помощью подбора м/о, способных продуцировать значительное количество α-кетоглутаровой кислоты из доступных источников сырья. Продуцентами α-кетоглутарата могут быть Pseudumonas и Escherichia, а при культивировании продуцента Kluyverd citrophila α-кетоглутаровая кислота была получена с 57%-ным выходом. Дрожжи рода Candida при выращивании на н-парафинах продуцируют α-кетоглутарат совместно с пируватом в соотношении 6:1. Экономический коэффициент процесса биосинтеза достигает 90% от количества потребленных углеводородов.
В роли продуцента фермента трансамидазы могут выступать различные м/о, например E. Coli. Донором аминогрупп может быть аспарагиновая кислота или аланин.
Восстановительное аминирование возможно осуществить с помощью Pseudomonas или Aeromonas, причем некоторые штаммы этих м/о в качестве субстрата могут использовать D,L-α-оксиглутаровую кислоты, производимую химическим синтезом.
В последние годы внимание исследователей привлекают методы получения аминокислот с использованием иммобилизованных ферментов. Способ имеет ряд преимуществ, в частности, конечный продукт отличается высокой концентрацией и чистотой, нет опасности заражения в ходе реакции посторонними микроорганизмами, в результате синтеза образуются только природные изомеры, имеется возможность осуществления непрерывных технологических процессов.
Микроорганизмы являются основными источниками ферментов, переводимых в иммобилизованную форму. Имея в виду преимущества иммобилизованных ферментов, необходимо учитывать, что они всегда будут дороже растворимых, но их внедрение экономически оправдано при удовлетворении даже одного из приводимых ниже условий: повышение стабильности фермента, обеспечивающее его многократное применение и тем самым сокращение расходов на препарат; улучшение качества продукта благодаря отсутствию в нем следов фермента и предотвращению нежелательных побочных реакций.
Выход продукта
Организация «дробной» подпитки приводит к активизации биосинтетической деятельности микроорганизмов. На мелассной среде осуществление «дробной» подпитки позволяет увеличить выход до 60 г/л. Количество фосфора в среде должно быть в пределах 8-20 мг %. Увеличение данной концентрации на один порядок почти на половину снижает выход глутамата. Повышение оптимальной температуры культивирования на 5о приводит к быстрому автолизу клеток, и в среде накапливается меньше глутамата. Недостаточная аэрация приводит к образованию аланина и лактата за счет снижения выхода глутамата. Слишком интенсивная аэрация способствует усиленному росту биомассы, выход целевого продукта при этом также начинает снижаться.
При использовании в качестве продуцента бактерий Micrococcus glutamicus и при оптимальных условиях культивирования выход целевого продукта составляет примерно 45 г в 1 л среды. Культура Microbacterium ammoniophilum на среде с тростниковой мелассой дала выход глутаминовой кислоты более 70 г/л. Corynebacterium glutamicum 7198 накапливает до 100 г/л глутаминовой кислоты.
Чем больше синтезируется продуцентом глутаминовой кислоты, тем больше образуется глутамата натрия при дальнейших превращениях глутамата.
Определение стехиометрических коэффициентов и теплового эффекта реакции
Общее стехиометрическое уравнение для аэробного процесса выглядит следующим образом:
ns*[C12H22O11] + nO2*[O2] + nN*[NH4Cl]=[X] + np*[p] + nCO2 *[CO2 ] + nH2O* [H2O],
где ns,nO2,nN,np,nCO2 ,nH2O – стехиометрические коэффициенты для субстрата, кислорода, азота, продукта, углекислого газа и воды соответственно.
[C12H22O11], [O2], [NH4Cl], [X], [p], [CO2], [H2O] – концентрации субстрата, кислорода, мочевины, продукта реакции, углекислого газа, воды
1. Для определения ns,np приведем все количества к 1 С-молю биомассы
Для биомассы Х используем формулу Стоухамера CH1,8N0,5O0,2
На 280 г сухого вещества биомассы выделяется 380 г продукта. В качестве углеродного субстрата используется 2 кг мелассы. Меласса содержит 50% сахарозы, следовательно сахарозы в ней содержится 1кг. Запишем полученное уравнение:
1000/342 [C12H22O11] = 280/24,6 [X] + 380/147 [C5H9NO4]
2,92/11,38 [C12H22O11] = 11,38/11,38 [X] + 2,59/11,38 [C5H9NO4]
0,26 C12H22O11] = [X] + 0,23 [C5H9NO4]
ns= 0,26, np= 0,23
2. Для определения коэффициентов по другим веществам необходимо составить систему уравнений элементарного баланса:
С: ns*mS = 1 + np*mp + nCO2;
H: ns*nS +n NH4Cl*4 = 1,8 + np*np + nH2O* 2;
O: ns*pS + nO2*2 = 0,5 + np*pp + nH2O +nCO2*2;
N: ns*qS +n NH4Cl = 0,2 + np*qp.
ns=0.26, np= 0.23
ms=12, mp= 5
ns=22, np= 9
ps=11, pp= 4
qs=0, qp=1.
С: 0.26*12 = 1 + 0.23*5 + nCO2 => nCO2=1.97
H: 0.26*22 +n NH4Cl*4 = 1,8 + 0.23*9 + nH2O* 2
N: n NH4Cl = 0,2 + 0.23*1=> n NH4Cl = 0.43
O: 0.26*11 + nO2*2 = 0,5 + 0.23*4 + nCO2 *2 + nH2O
nH2O = 1.785
nO2 = 2.145
Полученное уравнение:
0.26* [C12H22O11] + 2.145*[O2] +0.43*[ NH4Cl] = [X] + 0.23*[C5H9NO4]+ 1.97 *[CO2 ] + 1.785* [H2O],
Список используемой литературы
1) Яковлев В.И. Технология микробиологического синтеза. – Л.: Химия, 1987
2) Биотехнология: Учеб. пособие для вузов. В 8 кн./Под ред. Н.С. Егорова, В.Д. Самуилова. Кн. 6: Микробиологическое производство биологически активных веществ и препаратов / Быков В.А., Крылов И.А., Манаков М.Н. и др. – М.: Высш. шк., 1987. – 143с.: ил.
3) Биотехнология / Т.Г. Волова. – Новосибирск: Изд-во Сибирского отделения Российской Академии наук, 1999. – 252 с.
4) Бекер М.Е. Введение в биотехнологию. – Изд-во «Пищевая промышленность», 1978. – 238 с.
Похожие работы
... инженерию. Необходимо отметить, что если базовый стандарт по химии не предусматривает изучение вопросов биотехнологии, то таковой по биологии содержит наиболее общие её аспекты: достижения генной инженерии и перспективы биотехнологии. 2.2 Межпредметные связи по изучению аспектов биотехнологии в средней школе По программе Р.Г. Ивановой и Л.А. Цветкова в 10 классе предусмотрено изучение темы ...
... изолейцин, лейцин, лизин, метионин, треонин, триптофан, валин, фенилаланин. Аминокислоты — это не только питательные вещества, но также ароматические и вкусовые агенты, и потому они широко используются в пищевой промышленности. Как питательную добавку в пищу чаще всего вносят лизин и метионин. Глутамат натрия и глицин употребляют как ароматические вещества для усиления и улучшения вкуса пищи. У ...
... обществ по защите прав потребителей (КонфОП), например, заверяет, что у них уже на протяжении пяти лет нет претензий к производителям. "Пищевые добавки - это технические составляющие продуктов, необходимые на данном этапе развития пищевой промышленности. Опасного в них ничего нет", - официальное заверение высокого чиновника вице-президента КонфОПа Дмитрия Янина. Однако с ним согласны далеко не ...
... микроб - продуцент культивируют в среде, где он получается и синтезирует все необходимые ингредиенты для последующего синтеза ( в идиофазу ) целевого продукта. Если ферменты биосинтеза аминокислоты накапливаются внутриклеточно, но после 1 - ой ступени клетки сепарируют, дезинтегрируют и применяют клеточный сок. В других случаях для целей биосинтеза целевых продуктов применяют непосредственно ...
0 комментариев