Навигация
2. ПРОДУЦЕНТЫ АМИНОКИСЛОТ
Специфические ферменты, регулирующие биосинтез аминокислот, широко распространены у бактерий; они с определенной глубиной изучены у Escherichia coli. Salmonella typhimurium, Bacillus subtilis и прочие. У грибов, на аминокислотное лимитирование, отмечается некоординированное, параллельное возрастания уровня ферментов, катализирующих реакции биосинтеза различных аминокислот. Этот « общий контроль биосинтеза аминокислот » был также назван « метаболическим интерблоком », или « перекрестнопутевой регуляцией », впервые выявленной у Neurospora crassa в 1965 году М. Карсиотисом и сотрудниками, а позднее - у Saccharomyces cerevisiae, Aspergillus nidulas и других грибов.
В гиперпродукции отдельных аминокислот культурами Escherichia coli, Serratia marcescens и другие важную роль играют Feedak - репрессия, например, при биосинтезе ароматических аминокислот на последних стадиях.
В любом живом организме аминокислоты расходуются прежде всего на биосинтез первичных метаолитов - ферментных и неферментных белков. Следовательно, кроме биосинтеза аминокислот de novo, возможен другой путь их получения, а именно - из гидролизатов соответствующих белков ( триптофан разрушается при кислотном гидролизе ), в том числе из нативной биомассы микробных клеток.
Природные аминокислоты являются, как правило, оптически активными L - и D - формами, которые трудно разделить. Вот почему микробный синтез с помощью коринебактерий и некоторых других микробов является ныне основным и экономически выгодным. Первое место здесь по праву занимает Япония, где лишь глутаминовой кислоты изготавливается свыше 100 тысяч тонн в год; большинство природных незаменимых аминокислот производит фирма «Такеда». С. Киношита, впервые в 50-е годы открывший и доказавший перспективность микробного синтеза, уже 1963 году признавал: «Мало сомнения в том, что недалеко то время, когда с помощью микроорганизмов будет возможно производить все известные аминокислоты». Это время наступило уже к 70 -м годам. Получены микробы - суперпродуценты из родов Brevibacterium, Corynebacterium, Micrococcus и другие, с помощью которых освоено крупнотоннажное производство не только глутамата, но и L - лизина, L - валина, L - гистидина и других. При суперпродукции уровень экспрессии клонированного гена выражается в синтезе специфического белка в количестве 2 % от всех растворимых белков клетки - хозяина. В настоящее время имеются продуценты, у которых количество синтезируемого специфического белка достигает 10-15% (здесь важнейшую роль играют многокопийные плазмиды, несущее встроенный гены). Генно - инженерными методами во ВНИИ генетики и селекции промышленных микроорганизмов ( Москва ) был получен штамм Escherichia coli, обладающий сверхпродукцией L - треонина (30 г / л за 40 часов ферментации ).
С любым штаммом - продуцентом какой - либо аминокислоты необходимо внимательное и бережное обращение в целях поддерживания ее в активном состоянии в течении длительного времени.
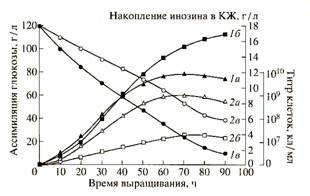
Получен штамм Escherichia coli, продуцирующий за 48 часов 27 г / л L - пролина, и штамм, продуцирующий до 22,4 г / л L - фениланина.
С помощью Corynebacterium sp. можно получигь алкапосодержащих средах L - тирозин (до 19 г/л ); с помощью Corynebacterium glutamicum на глюкозной среде - L - валин (до 11 г / л; L - аргинин, L - гистидин, L - изолейцин - 15 - 20,8 г / л.
3. БИОСИНТЕЗ АМИНОКИСЛОТ
Технология получения аминокислот базируется на принципах ферментации продуцентов и выделении вторичных метаболитов, то есть размножают маточную культуру вначале на агаризованной среде в пробирках, затем - на жидкой среде в колбах, инокуляторах и посевных аппаратах, а затем в головных (основных ) ферментаторах. Обработку культуральных жидкостей и выделение аминокислот проводят по схеме, аналогичной схеме получения антибиотиков. Изолированные чистые кристаллы целевого продукта обычно высушивают под вакуумом и упаковывают.
3.1 Одноступенчатый метод получения аминокислот
Известны два способа получения аминокислот: одноступенчатый и двухступенчатый. Согласно первому способу, например, мутантный полиауксотрофный штамм - продуцент аминокислоты культивируют на оптимальной для биосинтеза среде. Целевой продукт накапливается в культуральной жидкости, из которой его выделяют согласно схеме на рисунке d
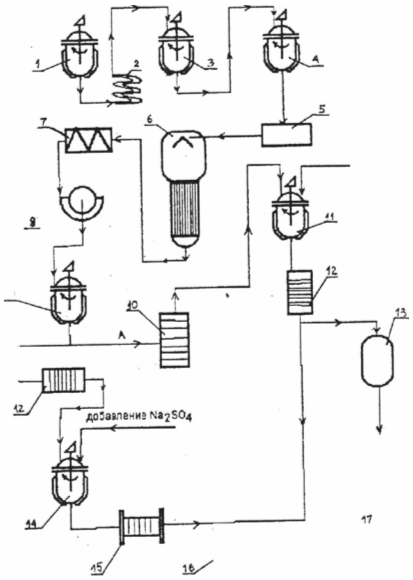
1 - ферментатор,
2 - охладитель, 3,9 - рефрижераторы,
4 - емкость для предварительной обработки,
5 - центрифуга,
6 - вакуум - упариватель,
7 - аппарат прямой
8 - барабанный фильтр, А,Б - пути ( при необходимости смыкающиеся ),
10 - аппарат для ультрофилырации,
11 - емкость для консервации раствора фермента,
12 - мембранный фильтр,
13 - накопитель жидкого консерванта, 14-емкость для осаждения фермента,
15 - фильтр - пресс,
16 - распылительная сушилка,
17 - накопитель сухого концентрата.
Рисунок №1 Примерная технологическая схема получения аминокислот.
3.2 Двухступенчатый метод получения аминокислот
В двухступенчатом способе микроб - продуцент культивируют в среде, где он получается и синтезирует все необходимые ингредиенты для последующего синтеза ( в идиофазу ) целевого продукта.
Если ферменты биосинтеза аминокислоты накапливаются внутриклеточно, но после 1 - ой ступени клетки сепарируют, дезинтегрируют и применяют клеточный сок. В других случаях для целей биосинтеза целевых продуктов применяют непосредственно клетки.
3.3 Получение лизина
Если аминокислота предусмотрена в качестве добавки к кормам, то биотехнологический процесс кормового продукта включает следующие стадии: ферментацию, стабилизацию аминокислоты в культуральной жидкости перед упариванием, вакуум - упаривание, стандартизацию упаренного раствора при добавлении наполнителя, высушивание и упаковку готового продукта, в котором должно содержатся не более 10 % основного вещества. Например, в промышленности изготавливают сухой кормовой и жидкий кормовой концентраты лизина наряду с кристаллическим лизином.(рис. 2)
Рисунок №2
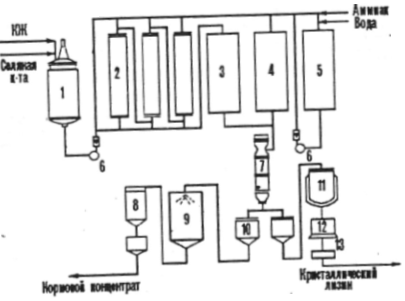
1 - емкость для культуральной жидкости (КЖ),
2 - ионообменные колонны,
3 - сборник злюата,
4 - сборник фильтрата,
5 - емкость для элюата,
6 - насос,
7 - вакуум - выпарной аппарат,
8 - циклон,
9 - сушилка кормового концентрата,
10 - сборник,
11 - реактор - кристаллизатор,
12 - центрифуга,
13 - сушилка.
Если концентрат содержит 70 - 80 % сухих веществ, то достаточно устойчив против микробной порчи за счет повышенной осмотической концентрации ингредиентов.[5]
3.4 Получение аминокислот с помощью иммобилизованных ферментов и клеток
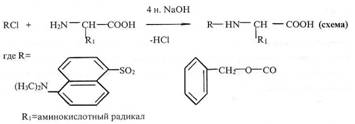
Экономически целесообразным являются способы получения аминокислот с помощью иммобилизованных ферментов и клеток. Сравнительно давно реализован процесс получения L - аспаргиновой кислоты из фумаровой и аммиака в одну стадию с помощью иммобилизованных клеток Е. coli или Pseudomonas aeruginosa, обладающая аспартазной активностью (см схему)
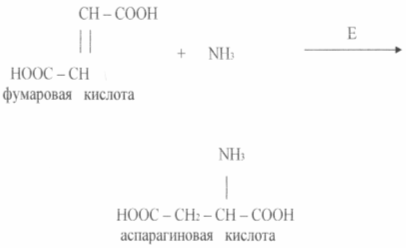
Аспартаза катализирует реакцию присоединения аммиака к фумаровой кислоте. Фермент в иммобилизованном состоянии сохраняет активность на исходном уровне 2 -2,5 недель и более.
L - Аспаргиновую кислоту можно получить и с помощью иммобилизованных клеток, что существенно повышает длительность функционирования системы, производительность которой по целевому продукту составляет около 2000 кг с 1м реактора. Периодические ферментации используют при получений других L - аминокислот (глутаминовой, фенилаланина, лизина, триптофана и др. ). При этом культивируют обычно специальные мутантные штаммы, метаболизм которых по целевому продукту изучен достаточно полно. Так, например, установлено, что лимитирующем агентом коринебак герий, образующих глутаминовую кислоту, является биотип в дозе 1 - 5 мкг/ л. Биотин индуцирует структурно - функциональные изменения в клеточной мембране, благодаря чему увеличивается ее проницаемость для глутаминовой кислоты, выходящей из клетки в культуральную жидкость. Отдельные штаммы продуцентов способны накапливать ее более 50 г/л на мелассных средах.
Роль биотина аналогична в случае получения пролина, являющимся производным глутаминовой кислоты.
Несложность этой технологии и ее преимущества по сравнению с глубинной ферментацией наглядно иллюстрируют опыт японской фирмы «Танабе Сейяку ». В 1973 году эта фирма разработала способ получения аспарагиновой кислоты при помощи иммобилизованных бактериальных клеток, обладающих аспартазной активностью. Аспартаза катализирует присоединение аммиака по двойной связи фумаровой кислоты, т.е. аспарагиновая кислота образуется в одной стадии и данный биотехнологический процесс можно отнести к категории биотрансформации органических соединений. Иммобилизованный в геле фермент функционировал хорошо, длительность его полуинактивации составила 1 месяц. Затем в геле иммобилизовали клетки продуцента, дополнительно стабилизируя их путем химического связывания между собой и с гелем. Длительность полуинактивации клеток в этом случае увеличивалась до 4 месяцев. Технологию биотрансформации фумаровой кислоты, таким образом, можно представить в такой последовательности:
выращивание клеток методом глубинной ферментации и их выделение центрифугированием;
иммобилизация клеток биокатализатора в геле в виде гранул размером 2 -3 мм;
биотрансформация фумарата аммония в колонке с катализатором в проточном режиме и получение раствора аспарагиновой кислоты;
кристаллизация, центрифугирование и промывка кристаллов.
Производительность системы биотранеформации аспарагиновой кислоты 1 м биореактора 1700 кг.
Похожие работы
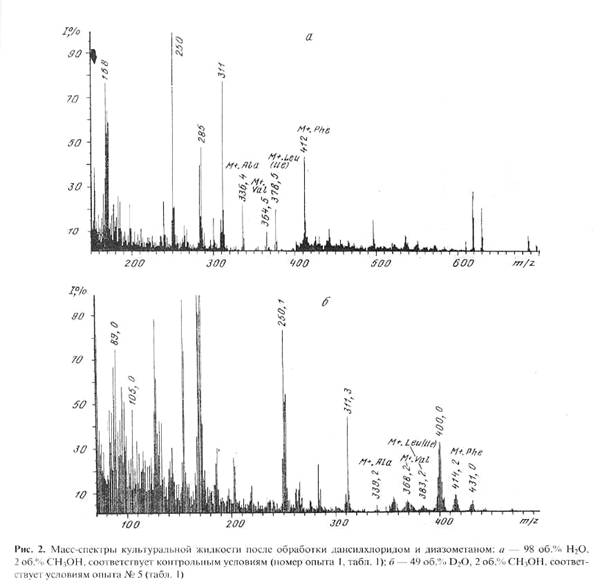
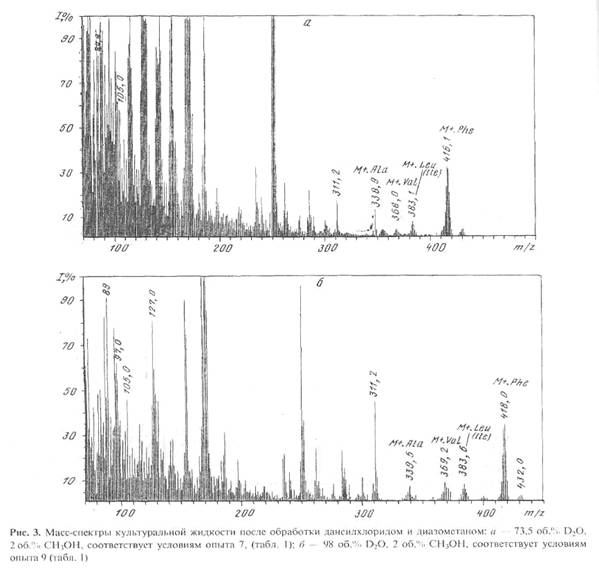
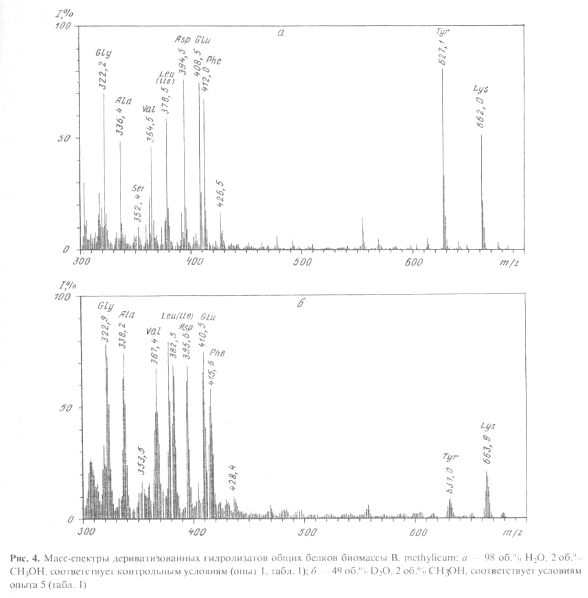
... использование данного штамма метилотрофных бактерий для наработки униформно меченного белка и аминокислот, было необходимо изучить уровни включения дейтерия в аминокислоты белковых гидролизатов B. methylicum, при росте бактерий на среде, содержащей максимальные концентрации тяжелой воды. Данные по степеням включения дейтерия в аминокислоты белка B. methylicum, полученного со среды, содержащей 98 ...
... . Так, в Phe детектировалось 80,5 % метки, в Ala - 95 %, в Gly - 90% (см. табл. 6). Во всех экспериментах степени включения дейтерия и изотопа углерода 13С в метаболически связанных аминокислотах обнаружили определённую коррелляцию. Так, степени изотопного обогащения валина и лейцина (семейство пирувата), фснилаланина и тирозина (семейство ароматических аминокислот} совпадают (табл. 6). Степени ...
... трансаминирования. Образуется альдегид и новая аминокислота, соответствующая исходной кетокислоте. Декарбоксилирование, связанное с реакцией конденсацией двух молекул: Обезвреживание аммиака в организме. В организме человека подвергается распаду около 70г аминокислот в сутки: при этом освобождается большое количество аммиака, являющегося высокотоксичным соединением. Поэтому крнцентрация аммиака ...
... инженерию. Необходимо отметить, что если базовый стандарт по химии не предусматривает изучение вопросов биотехнологии, то таковой по биологии содержит наиболее общие её аспекты: достижения генной инженерии и перспективы биотехнологии. 2.2 Межпредметные связи по изучению аспектов биотехнологии в средней школе По программе Р.Г. Ивановой и Л.А. Цветкова в 10 классе предусмотрено изучение темы ...
0 комментариев