Навигация
Методы выделения и анализа кумаринов в лекарственное растительное сырьё
КУРСОВАЯ РАБОТА
«Методы выделения и анализа кумаринов в ЛРС».
Оглавление
Введение
1.Основная часть
1. Общая характеристика кумаринов
2. Классификация производных кумарина
3. Краткая характеристика методов выделения и анализа
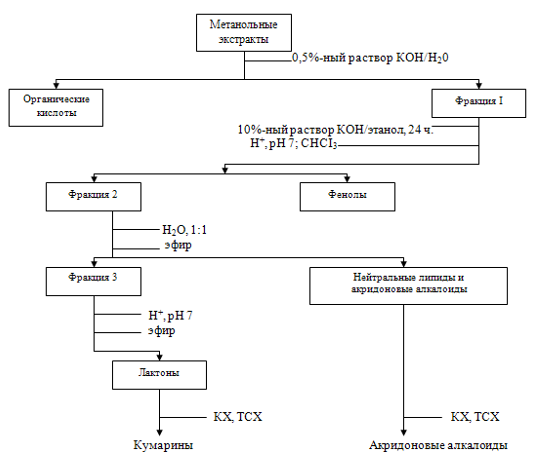
4. Методы выделения кумаринов
5. Методы анализа кумаринов
Заключение
Литература
Условные обозначения
ЛВ – лекарственное вещество
ЛФ – лекарственная форма
ЛРС – лекарственное растительное сырьё
ТСХ – хроматография в тонком слое сорбента
УФ область – ультрафиолетовая область
ГЖХ – газожидкостная хроматография
ВЭЖХ – высокоэффективная жидкостная хроматография
Введение
Физиологическая роль кумаринов до конца не установлена. Известно, что они участвуют в регуляции роста растений, являясь антагонистами ауксинов; поглощают ультрафиолетовые лучи, защищая молодые растения от чрезмерного солнечного облучения; предохраняют растения от вирусных заболеваний.
Одним из характерных фармакологических свойств производных кумарина является антикоагулирующее действие, также известны коронарорасширяющие, бэта-блокирующие и желчегонные свойства кумаринов. Многие фурокумарины обладают фотосенсибилизирующей способностью и спазмолитической активностью. Ряд кумаринов и фурокумаринов проявляют бактериостатические и антимитозные свойства. У куместрола и родственных ему соединений отмечено выраженное эстрогенное действие. Имеются литературные данные об анти-ВИЧ активности некоторых синтетических и природных производных кумарина.(6)
Собственно кумарин (лактон цисо-гидроксикоричной кислоты) широко применяется в парфюмерной промышленности. Установлена его эффективность при некоторых видах лимфедемы, почечной карциноме и меланоме. Однако известно, что в экспериментах на печени крыс кумарин проявляет гепатотоксичность, а при длительном применении в высоких дозах сам является канцерогеном.
К числу растительных объектов, содержащих кумарин, следует отнести донник лекарственный (Melilotus officinalis (L.) Pall.). Проводимыми исследованиями установлено наличие у травы донника лекарственного антигипоксической, антиишемической и других видов кардиотропной активности, что явилось основанием для разработки технологии и методов стандартизации сухого экстракта, таблеток, мази и суппозиториев на его основе, а также жидкого экстракта травы донника лекарственного и препарата "Флокрамел". Однако все предложенные методы оценки качества разработанных преператов (УФ-спектрофотометрия, ВЭЖХ, ТСХ) требуют наличия стандартного образца веществ класса кумаринов.(11)
При изучении НД на стандартные образцы, применяемые для оценки качества лекарственного растительного сырья (ЛРС) и фитопрепаратов, установлено, что стандартные образцы на производные собственно кумарина отсутствуют. Существующие стандартные образцы фурокумаринов псоралена, ксантотоксина, фловерина (сумма пиранокумаринов — дигидросамидина и виснадина) неприемлемы для оценки качества лекарственного растительного сырья, содержащего лактон цисо-гидроксикоричной кислоты и его замещенные аналоги.
В связи с этим представляет интерес обзор возможных методов выделения, а также синтеза и последующего анализа данного класса природных веществ с целью разработки адекватных методов получения стандартного образца и использования его для оценки качества ЛРС, фитосубстанций и препаратов, содержащих экстракты травы донника лекарственного. (7)
Основная часть
1. Общая характеристика кумаринов
Кумарины – природные кислородсодержащие гетероциклические соединения, в основе структуры которых лежит бензо-а-пирон (лактон цис-орто-гидроксикоричной кислоты).
Кумарины представляют собой производные 2Н-1-бензопиран-2-она. Они наиболее широко распространены в семействах Apiaceae Lindl., Rutaceae Juss., Fabaceae Lindl., Hippocastanaceae DC, при этом место их локализации различно: плоды, подземные органы, кора, листья, стебли и т.д. Количественное содержание кумаринов в растениях колеблется от 0,5 до 2 %, нередко достигая 5 - 6 % . Кумарины представляют собой бесцветные или окрашенные в желтый цвет кристаллические вещества, хорошо растворимые в органических растворителях — хлороформе, диэтиловом эфире, этиловом спирте, а также в жирах и жирных маслах. При нагревании до 100° С возгоняются.(1,2)
2. Классификация производных кумарина:
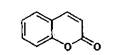
1. Незамещенные кумарины:
|
|
кумарин
2. Гидрокси-, метокси(алкокси)- и метилендигидроксикумарины и их гликозиды:
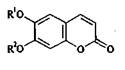
2.1. С гидроксильными или алкоксильными группами в бензольном кольце;
|
|
R1 = Н, R2 = ОН умбеллиферон
R1, R2 = ОН эскулетин
R1 = ОСН3 R2 = ОН скополетин
2.2. С гидроксильными или алкоксильными группами в пироновом кольце (галфордин);
2.3. Алкилированные в бензольном или пироновом кольце гидрокси- или метоксикумарины.
3. Фурокумарины:
3.1. Производные псоралена:
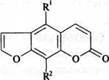
R1 = Н R2 = Н псорален
R1 = Н R2 = ОСНз ксантотоксин
R1 – OCH3 R2 = Н бергаптен
R1 – ОСН3 R2 = ОСН3 изопимпинеллин
3.2. Производные ангелицина:
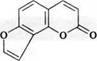
ангелицин
4. Пиранокумарины:
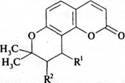
|
|
|
|
виснадин
|
|
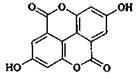
5. 3,4-бензокумарины:
эллаговая кислота
6. Куместаны: куместрол и др.
7. Другие более сложные соединения, в состав которых входит кумариновая система (новобиоцин, афлатоксин и др.) (2,7)
3. Краткая характеристика методов выделения и анализа
Экстракция – метод разделения, основанный на использовании экстрагента, не смешивающегося с исходной фазой и легко отделяющегося от неё и от экстрагируемых компонентов. В зависимости от исходной фазы различают эстракцию из твёрдого твёрдого вещества и экстракцию из раствора (жидкостную). По количеству операций экстракция может быть однократной и многократной.
Хроматографические методы разделения веществ основаны на их распределении между двумя фазами: подвижной и неподвижной. Подвижная фаза – жидкость или газ; неподвижная – твёрдое вещество или жидкость, адсорбированная на твёрдом носителе. Относительная скорость перемещения частиц вдоль пути разделения зависит от их взаимодействия с неподвижной фазой. Поэтому каждое вещество проходит на носителе определенный путь. Отношение пути перемещения вещества к пути перемещения растворителя есть величина постоянная, обозначаемая Rf. Она является константой для данных условий разделения и используется для идентификации ЛФ.
Хроматография на бумаге. Носителем неподвижной фазы (например, воды) служит специальная хроматографическая бумага. Распределение происходит между водой, находящейся на поверхности бумаги, и подвижной фазой, которая представляет собой систему из нескольких растворителей. Проводят испытания. Для подтверждения подлинности одновременно хроматографируют испытуемое вещество и стандартный образец. Если они идентичны, то пятна на хроматограммах будут иметь одинаковый вид и равные значения Rf.Хроматографию используют при испытании на чистоту.
Хроматография в тонком слое сорбента (ТСХ) отличается от хроматографии на бумаге тем, что процесс хроматографирования происходит на носителе (сорбенте), нанесенном тонким слоем на инертную поверхность. Твердый сорбент может быть закрепленным или незакрепленным на этой поверхности. Сорбентом служит силикагель или оксид алюминия. Для закрепления добавляют небольшие количества крахмала или сульфата кальция, Используют также пластинки промышленного изготовления типа «Силуфол УФ-254», «Сорбфил» и др.
Преимуществами ТСХ является простота приемов и оборудования, более высокая чувствительность, чем у бумажной хроматографии, устойчивость пластинок к температурным и химическим воздействиям, значительно большие возможности процессов разделения, детектирования, элюировання, меньшая продолжительность выполнения испытания. Все это создает широкие возможности в использовании ТСХ для выполнения испытаний на подлинность, на чистоту, для количественного определения ЛВ в ЛФ.
Двумерное хроматографирование отличается повторным (после высушивания) пропусканием той же или иной подвижной фазы, но в перпендикулярном по отношению к первоначальному направлению. При этом используют квадратные пластины или листы бумаги.
В фармацевтическом анализе широко применяют сочетание ТСХ с физико-химическими методами анализа. Такие комбинированные методы, как хромато-спектрофотометрия, хромато-флуориметрия, хромато-масс-спектроскопия, особенно эффективны в анализе ЛРС и препаратов, содержащих большое число сопутствующих компонентов.
Гравиметрический метод – основан на измерении массы вещества. Сущность определения состоит в последовательном выполнении реакций осаждения, отделения, высушивании и взвешивании осадка.
Перманганатометрия основана на использовании окислительных свойств титранта – перманганата калия в кислой среде.(2)
Колориметрический метод основан на способности веществ вступать во взаимодействие с солями диазония. В качестве реагентов применяют диазотированный п-нитроанилин, сульфаниловую кислоту,сульфаниламид.
Спектрофотонетрия в УФ- и видимой областях—один из наиболее широко используемых физико-химических методов в фармацевтическом анализе.
Анализируемые ЛВ должны иметь в структуре молекулы хромофорные группы (сопряженные связи, ароматическое ядро и др.), обуславливающие различные электронные переходы в молекулах и поглощение электромагнитного излучения.
Кривая зависимости интенсивности светопоглощения от длины волны (нм) называется спектром поглощения вещества и является его специфической характеристикой. Измерение спектров поглощения растворов анализируемых веществ в ультрафиолетовой (190-380 нм) и видимой (380-780 мм) областях производят с помощью спектрофотометров различных марок (СФ-26, СФ-46 и др.). В качестве растворителей используют свободные от примесей воду, растворы кислот и щелочей, этанол, хлороформ и другие органические растворители.
Слектрофотометрической константой является удельный показатель поглощении (Е1см1%), который рассчитывают по формуле:
(1) Е1см1% = А/С * l
Удельный показатель поглощения E1см1% представляет собой величину оптической плотности раствора, содержащего 1,0 г вещества в 100 мл раствора, измеренную в кювете с рабочей длиной 1 см. Установив по стандартному образцу величину Е1см1% и преобразовав эту формулу, можно рассчитать концентрацию анализируемого вещества с относительной погрешностью до ±2%.
Идентификацию ЛВ можно провести по Е1см1%, характеру спектральных кривых в различных растворителях, положению максимума и минимума светопоглощения или их отношению (при различных длинах волн). Для количественного спектрофотометрического анализа важен выбор аналитической полосы поглощения. Последняя должна быть свободна от наложения полос поглощения других компонентов смеси и иметь достаточно высокий удельный показатель поглощения анализируемого вещества.(2)
Фотоколориметрия отличается от спектрофотометрического анализа тем, что анализируемое вещество с помощью какого-либо реагента переводят (количественно) в окрашенное соединение. Вначале получают окрашенные растворы, используя растворы стандартных образцов (ГСО или РСО). Измерение оптической плотности производят на фотоколориметрах. Затем строят калибровочный график зависимости интенсивности поглощения окрашенных растворов от концентрации, по которому рассчитывают содержание ЛВ в испытуемых образцах ЛВ или ЛФ.
Флуоресцентные методы основаны на способности веществ флуоресцировать в УФ-свете, обусловленной либо химической структурой самих органических веществ, либо продуктов их диссоциации, сольволиза, других превращений. Способностью флуоресцировать обладают обычно органические соединения с симметричной структурой молекул, в которых имеются сопряженные связи (нитро-, нитрозо-, азо-, амидные, карбонильные или карбоксильные группы).
Полярография — метод, основанный на измерении силы тока, возникающего на микроэлектроде, при электровосстановлении анализируемого вещества в растворе. Растворителем служит вода, или органические и смешанные растворители. Электролиз проводят в полярографической ячейке, состоящей из электролизера и двух микроэлектродов: ртутного капающего и внешнего насыщенного каломельного. При соблюдении идентичных условий измерений для идентификации используют величину потенциала полуволны, а для количественного определения — высоту волны (измерение предельного диффузного тока). Количественный анализ выполняют методами калибровочных кривых с использованием стандартных растворов и методом добавок.(1,2)
Газожидкостная хроматография (ГЖХ) основана на распределении компонентов смеси между газовой и жидкой или твердой фазами. Распределение происходит в результате многократных актов сорбции и десорбции анализируемых веществ, которые вводятся в поток газа-носителя, испаряются и в парообразном состоянии проходят через колонку с сорбентом. Поэтому метод ГЖХ применим для анализа летучих веществ или веществ, которые могут быть переведены в газообразное состояние. Разделенные вещества элюируются из колонки потоком газа-носителя, регистрируются детектором и фиксируются на хроматограмме в виде пиков, по которым можно идентифицировать или определять содержание каждого компонента смеси.
Газовый хроматограф включает в себя систему измерения и регулирования скорости потока газа-носителя, систему ввода пробы испытуемого образца, газохроматографическую колонку, систему термостатирования и контроля температуры в различных узлах прибора и систему детектирования, регистрации и обработки информации, полученной на приборе.
Подлинность ЛВ методом ГЖХ можно подтвердить либо с помошью свидетелей, либо методом относительных удерживаний, В первом случае доказательством идентичности служит совпадение времени удерживания вешества-свидетеля и одного из компонентов смеси ЛВ при хроматографировании каждого в отдельности в одинаковых условиях. Во втором случае вещество-свидетель добавляют к пробе, затем анализируют по рекомендуемой методике. Рассчитывают по формуле величину относительного удерживания, которая является постоянной для ЛВ в конкретных условиях. Количественный анализ выполняют в тех же условиях, используя для расчетов такие параметры, как площадь или высота пиков ЛВ. Площадь пиков устанавливают на хроматограмме с помощью планиметра, интегратора или умножением высоты пика на его полуширину.
Высокоэффективная жидкостная хроматография (ВЭЖХ) отличается от ГЖХ тем, что подвижной фазой служит не газ, а жидкость, причем она проходит через колонку, наполненную сорбентом, с большой скоростью за счет значительного давления. Поэтому ВЭЖХ позволяет разделять многокомпонентные смеси на индивидуальные вещества высокой степени чистоты. ВЭЖХ отличается высокой чувствительностью {до 10 6 г). На разделение 10-15 компонентов затрачивается 20-30 мин.
Жидкостный хроматограф включает такие узлы, как дозатор, насос высокого давления, высокоэффективная колонка, детектор с регистрирующим устройством. Колонки изготавливают из нержавеющей стали, они имеют длину 10-25 см, внутренний диаметр 0,3-0,8 см и плотно набиваются адсорбентом с размером частиц 5-10 мкм. В качестве элюента используют различные углеводороды в сочетании с этанолом. Детектором обычно служит спектрофотометр с переменной длиной волны (190-900 нм), но существуют также флуориметрические. электрохимические и другие детекторы.
Подлинность испытуемых ЛВ подтверждают по времени выхода каждого компонента смеси из колонки, которое будет стабильно при одинаковых условиях проведения эксперимента. Количественное содержание рассчитывается по площади пика, которая пропорциональна количеству ЛВ в пробе.(2)
Похожие работы
... заболеваниях дыхательных путей, а также при заболеваниях желудочно-кишечного тракта. Мукалтин – препарат, приготовленный из травы, содержащей смесь полисахаридов; применяют в качестве отхаркивающего средства при бронхитах, пневмонии и бронхоэктазии. Он особенно показан детям. Алтей лекарственный используется в гомеопатии, входит в состав БАД. В качестве заменителей алтея перспективны виды рода ...
... растением, количество веществ специализированного обмена. Только благодаря правильно разработанной стратегии получения высокопроизводительных штаммов к настоящему времени получены культуры тканей, в которых содержание вторичных продуктов достаточно велико, чтобы служить лекарственным сырьем. Однако для многих культур неоднократные попытки различных исследователей определить условия накопления ...

0 комментариев