Навигация
Методы выделения кумаринов
4. Методы выделения кумаринов
Для выделения кумаринов из растений обычно применяются различные растворители: этанол, метанол, бензол, хлороформ, диэтиловый и петролейный эфиры или их комбинации.
4.1. Наиболее полная экстракция кумаринов (в свободной форме и в форме гликозидов) достигается при использовании спирта этилового различных концентраций, как на холоду, так и при нагревании. Для очистки суммы кумаринов от сопутствующих веществ густой экстракт, полученный после отгонки экстрагента, обрабатывают хлороформом, диэтиловым или петролейным эфиром. При использовании в качестве экстрагента петролейного эфира хорошо извлекается смесь фурокумаринов, которые после концентрирования экстракта можно выделить в кристаллическом состоянии. В ряде случаев дополнительно проводится обработка экстракта активированным углем, кипящей водой с последующим сгущением и дальнейшим извлечением гидроксилированных и метоксилированных кумаринов хлороформом, этилацетатом и бутанолом, непосредственная обработка сухого остатка смесью хлороформа — этиловый спирт (97:3) (для выделения аналогичных производных) или же используется само спиртовое извлечение. Например, для извлечения суммы 7-гидроксилированных кумаринов из корней Helianthus annum L. предложено проводить последовательную экстракцию ацетоном, смесью ацетон — метанол (1:1) с последующим освобождением от пигментов в делительной воронке смесью гексан — эфир (6:4). Иногда целесообразно растительный материал обрабатывать петролейным эфиром, а затем исчерпывающе экстрагировать хлороформом или метанолом. Для выделения пеуцеданина применяют экстракцию метанолом в аппарате Сокслета, аналогичным способом с использованием последовательной экстракции семян Angelica archangelica L. н-гексаном, дихлорметаном и метанолом и последующей препаративной ТСХ были выделены шесть производных фурокумарина. Эти же экстрагенты позволяют получить сумму кумаринов и фурокумаринов из растения Metrodorea flavida. Для выделения гидрокси-, алкоксикумаринов и их гликозидов из семян Aesculus hippocastanum L. применяется экстракция 80 % этиловым спиртом с последующей обработкой горячей водой, фильтрованием и многократным извлечением веществ хлороформом, этилацетатом и бутанолом. Эскулин и фраксин из коры каштана получали путем экстракции из метанола. В гексановых и метанольных извлечениях из побегов Kielmeyera reticulata Saad., полученных последовательно, обнаружены 4-фенилкумарины и 4-н-пропилкумарины.
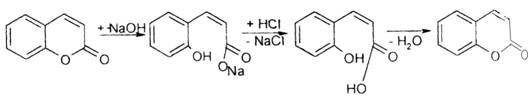
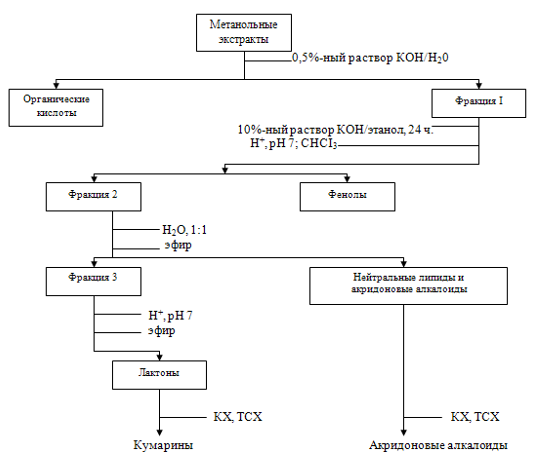
4.2. Для очистки кумаринов от сопутствующих веществ возможно использование метода омыления. Для выделения кумаринов проводят:
1. Экстракцию ЛРС органическим растворителем (эфиром) получают сумму кумаринов и балластных веществ.
2. Эфирный слой отделяют, отработанное сырьё выбрасывают.
3. Полученное эфирное извлечение обрабатывают 0,5% водным раствором КОН для очистки от фенолов и кислот.
4. Затем это же извлечение обрабатывают 10% спиртовым раствором КОН. Происходит разрыв лактонного кольца и образуются кумарины, которые переходят в водный слой. А в органическом растворителе остаются балластные вещества (смолы, стерины, спирты), органическую фазу выбрасывают.
5. Водно-щелочной слой подкисляют разбавленной НСl. Происходит замыкание лактонного кольца, образуются кумарины, которые экстрагируют органическим растворителем.
6. Органический слой отгоняют - получают сумму кумаринов, которую разделяют хроматографически.
Существенными недостатками этого метода являются возможность образования вторичных продуктов распада кумаринов, дегидратации и изомеризации некоторых оксикумаринов.
Дальнейшие операции, как правило, направлены на разделение суммы кумаринов и выделение индивидуальных соединений. В ранних исследованиях использовались кристаллизация, фракционная перегонка или сублимация в высоком вакууме. Однако многие кумарины обладают сходной растворимостью в органических растворителях, поэтому даже многократная перекристаллизация не позволяет достичь надежного результата.
Поэтому дальнейшее развитие химии кумаринов привело к использованию для этих целей различных видов хроматографии, лишенных вышеуказанных недостатков.(6,7)
4.3 Хроматографическое определение:
Для обнаружения кумаринов в растениях и сырье используются лактоновые свойства кумаринов, их способность флуоресцировать при ультрафиолетовом освещении и давать окрашенные растворы со специальными реактивами, микросублимацию и хроматографический анализ экстрактов сырья.(1):
На пластинку "Силуфол" или хроматографическую бумагу наносят исследуемые экстракты и помещают в хроматографическую камеру с системой, указанной в НД на исследуемое сырье. Хроматограммы после высушивания просматривают в УФ-свете. Флуоресцирующие пятна кумаринов отмечают простым карандашом и хроматограммы обрабатывают щелочью. После этого их высушивают в сушильном шкафу при t=120°C и вновь просматривают в УФ-свете. Затем хроматограмму обрабатывают диазотированным сульфаниламидом, от действия которого кумарины в зависимости от структуры окрашиваются в оранжевый, красно-оранжевый, фиолетовый цвета.
В некоторых случаях после просматривания хроматограммы в УФ-свете ее обрабатывают реактивом Драгендорфа (Bil3 в KI) или парами иода. Кумарины проявляются в виде пятен, окрашенных в коричневый цвет.
В первую очередь, проводят колоночную хроматографию с использованием различных сорбентов и систем растворителей.(5)
Так, для разделения гидрокси- и алкоксикумаринов, замещенных в бензольном цикле, предлагается применять колонку, заполненную силикагелем, и проводить последовательное элюирование гексаном, смесью гексан — хлороформ (с увеличением концентрации хлороформа), смесью хлороформ — метанол (9:1; 8:2; 7:3) или смесью хлороформ — этанол (97:3) . В других случаях для этих же целей берут оксид алюминия и смесь этилацетат — бензол (2:1) или бензол, силикагель и системы: хлороформ — бензол (1:1), хлороформ, хлороформ — этанол (98:2; 99:1; и т.д. до 90:10), бензол - бутанол (4:1; 3:1). Для разделения 4-фенил, 4-н-пропилкумаринов и 4-н-пропил-пиранокумаринов используют силикагель и элюируют последовательно системами гексан — этилацетат (градиент), метанол — вода — дихлорэтан, гексан — ацетон.
Фурокумарины фракционируют на оксиде алюминия (III степень активности) при помощи петролейного эфира, смеси петролейный эфир - хлороформ (2:1), хлороформа, смеси хлороформ — этанол (9:1, 4:1, 2:1), а также на силикагеле — смеси гексан — хлороформ и хлороформ — этанол с постепенным увеличением содержания более гидрофильного компонента.
О присутствии кумаринов свидетельствует характерная флуоресценция в УФ-свете отдельных зон сорбента, содержащих эти соединения, или же положительный эффект химических реакций, проводимых с элюатами.
При слабом сродстве вещества к сорбенту необходимо использовать активные слои и слабополярные растворители, а при сильном — малоактивные слои и сильнополярные растворители. В частности, кумарины с фенольными или спиртовыми гидроксилами активнее сорбируются на окиси алюминия и элюируются большими объемами полярных растворителей (этанол), иногда с добавлением 0,5 % уксусной или хлористоводородной кислоты; метилированные производные и пиранокумарины слабее удерживаются на сорбенте. В процессе элюирования целесообразно постепенно заменять гидрофобные растворители гидрофильными.
Для разделения суммы кумаринов, в том числе при их сочетании с другими низкомолекулярными БАВ, их очистки и анализа в настоящее время предложена колоночная хроматография с использованием сорбентов аффинного типа на основе фенольных и полифенольных лигандов. Рекомендованы эпоксиактивированные сорбенты с матрицей HW-35, содержащей резорциновые и катехиновые лиганды. В качестве подвижной фазы используются вода, водные растворы этанола, минеральных кислот, нейтральных солей и различных их сочетаний. Установлено, что при использовании данных типов сорбентов результаты значительно превосходят те, которые были получены при использовании классических кремнеземных, полиамидных и декстрановых сорбентов.
Контроль за эффективностью колоночной хроматографии осуществляется с использованием бумажной (БХ), а чаще — тонкослойной (ТСХ) хроматографии, что позволяет быстро устанавливать однородность исследуемых веществ и обнаруживать даже незначительные их количества. Для ТСХ наиболее часто применяются пластинки Силуфол или Сорбфил, иногда используется оксид алюминия II степени активности, силикагель, а в качестве систем растворителей — смеси бензола и ацетона (1:2), бензола, метанола и ацетона (8:2:10), гексана и хлороформа, толуола и н-бутанола (гидрокси- и метоксикумарины), спирта этилового и хлороформа (5,5:4,5), хлороформа и формамида (скополетин), этилацетата и бензола (1:2), диэтилового и петролейного эфира (фурокумарины) и другие.
Наилучшим сорбентом для разделения суммы кумаринов методом ТСХ считается оксид алюминия, при этом в качестве элюентов используют смеси: петролейный эфир — этилацетат (2:1), петролейный эфир — хлороформ, циклогексан — этилацетат (3:1), бензол — этилацетат в различных соотношениях и бензол.
В бумажной хроматографии используются различные марки бумаги. Следует отметить, что ввиду избирательной растворимости кумаринов в водных и неполярных растворителях, применяется метод импрегнирования хроматографической бумаги 20 % водными растворами этиленгликоля или пропиленгликоля, раствором формамида (или диметилформамида) в метаноле или ацетоне, растворами бората или фосфата натрия. В первом случае гидроксилсодержащие кумарины остаются на линии старта, поэтому используется пропитывание бумаги другими растворами или проводится хроматографирование в системе БУВ без импрегнирования бумаги .
Детекция кумаринов на хроматограммах чаще всего проводится по флуоресценции в УФ-свете при характерных длинах волн до и после обработки хроматограммы водно-спиртовыми растворами гидроксида калия, парами аммиака, а также по другим цветным реакциям. Цвет флуоресценции не позволяет с достаточной степенью точности определить структуру кумаринов, но в ряде случаев по нему можно судить о наличии и примерном расположении функциональных группировок.
Индивидуальные вещества выделяют с использованием препаративной ТСХ. Идентичность выделенного вещества устанавливают по таким характеристикам, как температура плавления, ИК-, ЯМР- и масс-спектры . ИК-спектры кумаринов имеют характерные полосы поглощения при 1750-1700 см -1 (-С=О группы) и при 1620- 1470 см -1 (для –С=С- ароматического кольца). При исследовании кристаллической структуры синтетических веществ данного класса возможно использование кристаллографического анализа с применением программного обеспечения SHELXL97. В качестве характеристики кумаринов с боковой цепью, содержащей асимметрические атомы углерода, хиральных атомов углерода фуранового цикла замещенного дигидроангелицина и пиранового цикла замещенного келлактона может использоваться величина удельного вращения.
Для подтверждения структуры выделенных из растений кумаринов возможно использование встречного синтеза. Среди методов синтеза следует отметить конденсацию Перкина (из салицилового альдегида и уксусного ангидрида), реакции Пехмана (из фенола и яблочной кислоты или Р-кетоэфиров), реакцию Кневе-нагеля (конденсация о-гидроксибензальдегидов с эфирами малоновой и других кислот).(7)
Похожие работы
... заболеваниях дыхательных путей, а также при заболеваниях желудочно-кишечного тракта. Мукалтин – препарат, приготовленный из травы, содержащей смесь полисахаридов; применяют в качестве отхаркивающего средства при бронхитах, пневмонии и бронхоэктазии. Он особенно показан детям. Алтей лекарственный используется в гомеопатии, входит в состав БАД. В качестве заменителей алтея перспективны виды рода ...
... растением, количество веществ специализированного обмена. Только благодаря правильно разработанной стратегии получения высокопроизводительных штаммов к настоящему времени получены культуры тканей, в которых содержание вторичных продуктов достаточно велико, чтобы служить лекарственным сырьем. Однако для многих культур неоднократные попытки различных исследователей определить условия накопления ...

0 комментариев