Навигация
5.11 Флуоресцентный анализ
Многие кумарины и фурокумарины проявляют характерную (желтую, зеленую, голубую или фиолетовую) флуоресценцию при УФ-возбуждении в нейтральных спиртовых растворах, в растворах щелочей и концентрированной серной кислоте в видимой и ультрафиолетовой областях спектра. Флуоресценция усиливается в щелочной среде за счет образования хиноидной структуры, в кислой среде флуоресценция менее выражена. По величине стоксового сдвига и максимуму флуоресценции предлагается проводить идентификацию фитохимических препаратов. Для кумаринов и фурокумаринов получены спектры флуоресценции и установлена линейная зависимость ее интенсивности от концентрации, что позволило применить метод флуороденситометрии для количественного определения фурокумаринов псоралена и ангелицина в препарате псорален. Образование флуоресцирующих соединений компонентов препаратов "Аммифурин", "Бероксан" и "Пастинацин" с насыщенным раствором брома в щелочной среде позволило идентифицировать их на основании одинаковых максимумов возбуждения (380 нм) и флуоресценции (480 нм).
Предложен флуориметрический метод определения количественного содержания фурокумаринов в плодах Pastinaca sativa L. при длине волны возбуждения 350 нм и флуоресценции 470 нм. Аналогичная методика приведена и для близкого структурного аналога кумаринов, келлина, в плодах Ammi visnaga L. (Lam.).
Также предложен селективный способ количественного определения неодикумарина путем последовательной обработки анализируемой пробы в диметилформамиде раствором аммиака и насыщенным раствором магния хлорида в этом же растворителе.
Флуоресценция производных кумарина зависит от концентрации водородных ионов, поэтому данные об изменении окраски и интенсивности флуоресценции в различных пределах рН, а также в зависимости от строения кумаринов могут оказаться необходимыми при использовании флуориметрических методов. Количественный анализ с использованием данного метода не получил широкого распространения из-за не всегда проявляющейся линейной зависимости интенсивности флуоресценции от концентрации.
В литературе имеются данные об использовании 7-(2-бромэтокси) кумарина в качестве флуоресцентной метки для количественного флуориметрического анализа лекарственных препаратов, содержащих третичный атом азота.
Возможно применение флуоресцентной микроскопии для локализации и определения количества гидроксилированных производных кумарина, выполняющих роль фотопротекторов, в зеленых водорослях Da-sycladis vermicularis (Scopoli) Krasser.
Интерес представляет флуоресцентный экспресс-метод обнаружения кумарина в топливе, основанный на реакции его щелочного гидролиза с образованием о-кумаринат-ионов и последующим их превращением в о-кумарат-ионы, обладающие интенсивной флуоресценцией.
5.12 Бумажная хроматография чаще всего сочетается с другими физико-химическими методами. Например, после разделения суммы кумаринов на бумаге (петролейный эфир; ДМФА в ацетоне) возможно полярографическое определение суммы фурокумаринов в плодах Pastinaca sativa L. и в препарате "Бероксан". Сочетание бумажной хроматографии с фотоколориметрическим определением на основе реакции с диазотированной сульфаниловой кислотой используют для анализа фурокумаринов Psoralea drupacea Bge., псоралена и бергаптена в листьях Ficus carica L.. Этот же метод использован для определения фурокумаринов в некоторых видах зонтичных. К существенным недостаткам БХ относятся длительность проведения анализа и необходимость концентрирования вытяжки из-за малой сорбционной емкости бумаги.
5.13 Метод тонкослойной хроматографии в значительной степени лишен указанных недостатков, т.к. позволяет относительно быстро производить разделение компонентов смеси. Как и БХ, его можно использовать для идентификации кумаринов в исследуемых препаратах.
Имеются данные о колориметрических методах количественного определения пеуцеданина в корнях Ре-ucedanum morrissonii Bess., основанных на реакции азосочетания, с разделением на тонком слое оксида алюминия в системе гексан — бензол — метанол (5:4:1), и для анализа бероксана, пастинацина и псоралена. Также описано колориметрическое определение ксантотоксина, императорина и бергаптена в Ammi majus L. после хроматографирования на си-ликагеле, импрегнированном формамидом, в системе дибутилового эфира. Предложена методика определения псоралена и суммы псоралена и бергаптена, по отдельности, в листьях Ficus carica L.. При этом очищенный от балластных веществ экстракт хроматографируют в тонком слое оксида алюминия в диэти-ловом эфире, а затем при помощи УФ-спектрофотометрии устанавливают содержание кумаринов. Имеются литературные данные о возможности использования двумерной хроматографии в слое силикагеля для определения бергаптена в системах гексан — четыреххлористый углерод — трет-бутиламин (180:12:9) и гексан — толуол — этилацетат - уксусная кислота (100:10:10:0,5) в сочетании со спектрофлуориметрией.
Последнее десятилетие характеризуется широким использованием ГЖХ и ВЭЖХ для решения задач, связанных с разделением и оценкой качества различных соединений класса кумаринов.
5.14 Газожидкостная хроматография (ГЖХ) применяется в основном для идентификации и количественного анализа фурокумаринов в препаратах и растительном сырье. Установлено различие во временах удерживания для замещенных фурокумаринов. Из общих закономерностей следует упомянуть следующие: при переходе от гидрокси- к метоксикумаринам время удерживания уменьшается (снижается возможность сорбции за счет водородных связей), а фурокумарины с О-алкильным заместителем при С5 регистрируются позже, чем 8-гидроксиизомеры. Кроме того, отмечено, что величина десятичного логарифма относительного времени удерживания линейно зависит от молекулярной массы вещества. Полученные данные могут быть использованы при определении структуры или времени удерживания сходных кумаринов.
Описано также определение псоберана в субстанции методом ГЖХ.
Для анализа корней Phlojodicarpus sibiricus и фловерина предлагается ГЖХ методом абсолютной калибровки после экстракции кумаринов хлороформом в сравнении со стандартным образцом фловерина. При этом дигидросамидин и виснадин выходят одним симметричным пиком. Сравнение проводят со стандартным образцом фловерина. Раздельное определение виснадина и дигидросамидина возможно после предварительного переведения солей, образовавшихся при щелочном гидролизе, в свободные кислоты. Кислоты экстрагируют эфиром и хроматографируют. Аналогичный метод применяют для анализа аммифурина и плодов Ammi majus L. после экстракции их этиловым спиртом. В качестве внутреннего стандарта используют стандартный образец ксантотоксина.
Метод газовой хроматографии также применяется для обнаружения кумарина и его метаболитов в печени животных и человека.
5.15 Широкое распространение в анализе производных кумарина и фурокумарина в настоящее время получила высокоэффективная жидкостная хроматография (ВЭЖХ). Описано одновременное количественное определение методом ВЭЖХ действующих веществ семян Coronilla varia L. (кумаринов — скополетина, дафноретина и умбеллиферона и кардио-тонических гликозидов). Влияние метоксалена (ксантотоксина) на метаболизм никотина также проводилось при помощи этого метода.
Имеются данные об исследовании содержания кумарина в зависимости от времени заготовки южноамериканского растения Mikania laevigata, применяемого метода экстракции и экстрагента. Предложено использовать ВЭЖХ в изократическом режиме для разделения, одновременного качественного и количественного анализа кумаринов коры Aesculus hyppocasta-пит L. без предварительной очистки, для количественной оценки кумарина в листьях Mikania glomera-ta Spreng . Известна методика определения кумаринов с помощью ВЭЖХ в градиентном режиме (флуоресцентный детектор) при изучении биохимических функций кумаринов в корнях подсолнечника (Heliant-hus annum L.).
Весьма перспективным методом является сочетание ВЭЖХ и масс-спектрометрии. Предложены соответствующие методики определения антикоагулянтов непрямого действия и родентицидов кумаринового ряда (производные 4-гидроксикумарина) в плазме крови в практике токсикологического анализа. Определенный интерес представляет использование хроматомасс-спетрометрии для определения наличия кумарина в табачной продукции.(7)
Заключение
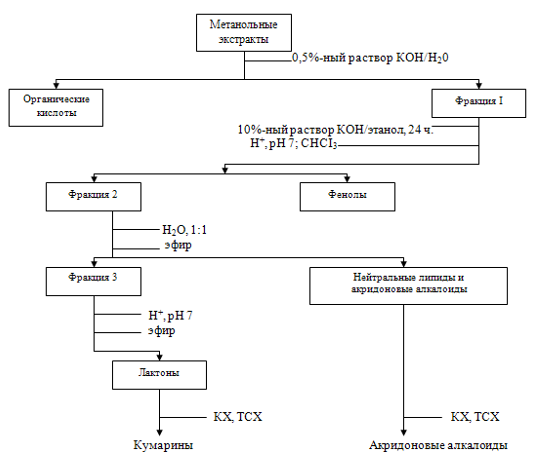
Для выделения суммы кумаринов из ЛРС было предложено использовать экстракцию этиловым спиртом различных концентраций с последующей очисткой хлороформом. Изучение качественного состава кумаринов проводили с использованием различных методов хроматографии — бумажной, тонкослойной и ВЭЖХ.
Качественный анализ производных кумарина, содержащихся как в экстракте, так и в лекарственных формах можно проводить, используя для этих целей как химические, так и физико-химические методы.
В качестве химических методов идентификации кумаринов используется общепринятая реакция азосочетания, лактонная проба, а также другие цветные реакции. Эти способы могут быть использованы в методах ТСХ и БХ, а также непосредственно путем проведения химических реакций с извлечением.
Качественное определение суммы кумаринов предложено проводить методом ТСХ на пластинках Сорбфил в системе бензол - этилацетат (1:2) с последующей обработкой раствора спиртовым раствором щелочи. Пятна идентифицируют по величине Rf и желтой окраске. Однако как уже было отмечено, реакция с диазореактивами неспецифична для кумаринов, к тому же значения Rf не всегда воспроизводимы, поэтому целесообразно применение ТСХ со стандартным образцом преобладающих соединений данного класса.
При использовании УФ-спектрофотометрии идентификацию кумаринов проводят по наличию полос поглощения при определенных длинах волн. ВЭЖХ предполагает нахождение параметров удерживания.
Для количественного определения суммы кумаринов в ЛРС были предложены такие методы, как титриметрия, гравиметрия, фотоколориметрия, УФ-спектрофотометрия и ВЭЖХ.(5,7)
Литература
1. Арзамасцев, А.П. Фармацевтическая химия – М.:Гэотар-мед,2004.-635 с.
2. Беликов, В.Г. Фармацевтическая химия – Пятигорск, 2003. – 715 с.
3. Государственная фармакопея СССР XI издание / 1 и 2 т. – М.: Медицина,1987. – 334 с., 1990. – 398 с.
4.Кемертелидзе, Э.П. Физико – химические методы анализа некоторых биологически активных веществ растительного происхождения – Тбилиси, 1976. – 198 с.
5. Коноплёва, М.М. Фармакогнозия: Природные биологически активные вещества – Витебск 2007. – 272 с.
6. Кузнецова, Г.А. Природные кумарины и фурокумарины – Л., 1967, 28 с.
7. Ложкин, А.В. Природные кумарины: методы выделения и анализа /А.В. Ложкин, Е.И. Сакалян // Хим. – фарм. журн. – т.40, №6 – 2006 – с 47 - 57
8. Машковский, М.Д. Лекарственные средства – Москва 2005
9. Справочник Видаль. Лекарственные препараты в России. – М.: АстраФармСервис, 1995 - 2007
10. Фармакопея РБ, 1т.
11. Шелюто, В.Л. Фармакогнозия – Витебск,2003 – 490 с.
Похожие работы
... заболеваниях дыхательных путей, а также при заболеваниях желудочно-кишечного тракта. Мукалтин – препарат, приготовленный из травы, содержащей смесь полисахаридов; применяют в качестве отхаркивающего средства при бронхитах, пневмонии и бронхоэктазии. Он особенно показан детям. Алтей лекарственный используется в гомеопатии, входит в состав БАД. В качестве заменителей алтея перспективны виды рода ...
... растением, количество веществ специализированного обмена. Только благодаря правильно разработанной стратегии получения высокопроизводительных штаммов к настоящему времени получены культуры тканей, в которых содержание вторичных продуктов достаточно велико, чтобы служить лекарственным сырьем. Однако для многих культур неоднократные попытки различных исследователей определить условия накопления ...

0 комментариев