Навигация
Микрогетерогенные системы
СУСПЕНЗИИ
Суспензии — это дисперсные системы, в которых дисперсной фазой являются частицы твердого вещества размером более 10-7 м, а дисперсионной средой — жидкость.
Условно суспензии обозначают в виде дроби: Т/Ж, в числителе которой указывается агрегатное состояние фазы, а в знаменателе - агрегатное состояние среды.
Можно дать суспензиям и другое определение: суспензии — это взвеси порошков в жидкостях.
Данное определение, являясь менее формальным, чем первое, ближе к реальной жизни уже потому, что сам термин «суспензия» (suspensio) в переводе с позднелатинского означает «подвешивание».
Формально суспензии от лиозолей (коллоидных растворов) отличаются только размерами частиц дисперсной фазы. Размеры твердых частиц в суспензиях (более 10-7м) могут быть на несколько порядков больше, чем в лиозолях (10-9-10-7 м). Это количественное различие обусловливает чрезвычайно важную особенность суспензий: в большинстве суспензий частички твердой фазы не участвуют в броуновском движении. Поэтому свойства суспензий существенно отличаются от свойств коллоидных растворов; их рассматривают как самостоятельный вид дисперсных систем.
Рассматривая в дальнейшем конкретные свойства суспензий, полезно сопоставлять их с аналогичными свойствами коллоидных растворов, которые изучались в предыдущих разделах коллоидной химии.
КЛАССИФИКАЦИЯ СУСПЕНЗИЙ
Суспензии разделяются по нескольким признакам.
1. По природе дисперсионной среды:
органосуспензии (дисперсионная среда-органическая жидкость),
водные суспензии.
2. По размерам частиц дисперсной фазы:
грубые суспензии (d > 10-4 м),
тонкие суспензии (5·10-7 < d < 10-4 м), мути (1·10-7 < d < 5·10-7 м).
3. По концентрации частиц дисперсной фазы: разбавленные суспензии (взвеси) и концентрированные суспензии (пасты).
В разбавленных суспензиях частицы свободно перемещаются в жидкости, сцепление между частицами отсутствует и каждая частица кинетически независима. Разбавленные суспензии — это свободнодисперсные бесструктурные системы.
В концентрированных суспензиях (пастах) между частицами действуют силы, приводящие к образованию определенной структуры (пространственной сетки). Таким образом, концентрированные суспензии — это связнодисперсные структурированные системы.
Конкретные значения концентрационного интервала, в котором начинается структурообразование, индивидуальны и зависят, в первую очередь, от природы фаз, формы частиц дисперсной фазы, температуры, механических воздействий. Механические свойства разбавленных суспензий определяются, главным образом, свойствами дисперсионной среды, а механические свойства связнодисперсных систем определяются, кроме того, свойствами дисперсной фазы и числом контактов между частицами.
МЕТОДЫ ПОЛУЧЕНИЯ РАЗБАВЛЕННЫХ СУСПЕНЗИЙ
Суспензии, так же как и любую другую дисперсную систему, можно получить двумя группами методов:
со стороны грубодисперсных систем — диспергационными методами,
со стороны истинных растворов — конденсационными методами.
Рассматривая конкретные методы получения суспензий, полезно вспомнить, что суспензии — это взвеси порошков в жидкости. Следовательно, наиболее простым и широко распространенным как в промышленности, так и в быту методом получения разбавленных суспензий является взбалтывание соответствующего порошка в подходящей жидкости с использованием различных перемешивающих устройств (мешалок, миксеров и т. д.). Для получения концентрированных суспензий (паст) соответствующие порошки растирают с небольшим количеством жидкости,
Так как суспензии отличаются от лиозолей только тем, что частицы в них на несколько порядков больше, все методы, которые используются для получения лиозолей, можно применять и для получения суспензий. При этом необходимо, чтобы степень измельчения диспергационными методами была меньше, чем при получении лиозолей. При конденсационных методах конденсацию необходимо проводить так, чтобы образовывались частицы, имеющие размеры 10-7-10-4 м. Размер образующихся частиц зависит от соотношения скоростей образования зародышей кристаллов и их роста. При небольших степенях пересыщения обычно образуются крупные частицы, при больших — мелкие. Предварительное введение в систему зародышей кристаллизации приводит к образованию практически монодисперсных суспензий. Уменьшение дисперсности может быть достигнуто в результате изотермической перегонки при нагревании, когда мелкие кристаллы растворяются, а за их счет растут крупные.
При этом должны соблюдаться условия, ограничивающие возможности значительного разрастания и сцепления частиц дисперсной фазы. Дисперсность образующихся суспензий можно регулировать также введением ПАВ.
Суспензии очищают от примесей растворенных веществ диализом, электродиализом, фильтрованием, центрифугированием.
Суспензии образуются также в результате коагуляции лиозолей. Следовательно, способы осуществления коагуляции — это одновременно и методы получения суспензий.
Все вышесказанное касалось промышленных и бытовых суспензий. Природные суспензии (а ими являются практически все водоемы Земли) образуются вследствие попадания в воду твердых частиц в результате разрушения аэрозолей, а также при диспергировании почв, грунтов и скальных пород под воздействием сил прибоя, приливно-отливных явлений, при движении ледников.
СЕДИМЕНТАЦИОННАЯ УСТОЙЧИВОСТЬ РАЗБАВЛЕННЫХ СУСПЕНЗИЙ
Седиментационная устойчивость суспензии — это способность ее сохранять неизменным во времени распределение частиц по объему системы, т. е. способность системы противостоять действию силы тяжести.
Так как большинство суспензий оказываются полидисперсными системами, содержащими и относительно крупные частицы, которые не могут участвовать в броуновском движении, суспензии являются седиментационно (кинетически) неустойчивыми системами. Если плотность частиц меньше плотности дисперсионной среды, то они всплывают, а если больше — оседают.
Изучение седиментации суспензий связано, в первую очередь, с получением кривых накопления осадка (кривых седиментации) m = f(t). Кривые накопления могут быть двух видов: с перегибом или без перегиба. Установлено, что вид кривых седиментации зависит от того, является ли седиментирующая суспензия агрегативно устойчивой или нет:
1) Если седиментация сопровождается укрупнением частиц, а следовательно, увеличением скорости их оседания, то на кривых седиментации появляется точка перегиба.
2) Если же суспензия агрегативно устойчива (нет коагуляции), то на кривой седиментации перегиб отсутствует. Характер осадков, полученных в том и другом случаях, также различен.
В агрегативно устойчивых суспензиях оседание частиц происходит медленно и формируется очень плотный осадок. Объясняется это тем, что поверхностные слои препятствуют агрегированию частиц; скользя друг по другу, частицы могут перейти в положение с минимальной потенциальной энергией, т. е. с образованием упаковки, близкой к плотнейшей. В этом случае расстояние между частицами и координационное число (число соседних частиц) в осадке такой седиментирующей, но предельно стабилизированной суспензии, определяется соотношением между:
• силой тяжести;
• межмолекулярным притяжением частиц;
• силами отталкивания между частицами, обеспечивающими агрегативную устойчивость суспензии.
В агрегативно неустойчивых суспензиях оседание частиц происходит значительно быстрее вследствие образования агрегатов. Однако выделяющийся осадок занимает гораздо больший объем, так как частицы сохраняют то случайное взаимное расположение, в котором они оказались при первом же контакте, силы сцепления между ними соизмеримы с их силой тяжести или больше ее. Наблюдается анизометрия (т. е. преобладание одного из размеров частицы над двумя другими) образующихся агрегатов или флокул. Исследования показывают, что наиболее вероятны цепочечные и спиральные первоначальные агрегаты, из которых затем получаются осадки большого седиментационного объема.
Различие седиментационных объемов агрегативно устойчивых и неустойчивых систем наиболее четко проявляется, если частицы имеют средние размеры. Если частицы крупные, то, несмотря на то, что суспензия агрегативно неустойчивая, осадок получается более плотным из-за значительной силы тяжести, зачастую преобладающей над силами сцепления между частицами. Если же частицы очень мелкие, то и в агрегативно устойчивой системе из-за малой силы тяжести образуется чрезвычайно подвижный осадок.
АГРЕГАТИВНАЯ УСТОЙЧИВОСТЬ РАЗБАВЛЕННЫХ СУСПЕНЗИЙ
Агрегативная устойчивость суспензии — это способность сохранять неизменной во времени степень дисперсности, т. е. размеры частиц и их индивидуальность.
Агрегативная устойчивость разбавленных суспензий весьма сходна с агрегативной устойчивостью лиофобных золей. Но суспензии являются более агрегативно устойчивыми системами, так как содержат более крупные частицы и, следовательно, имеют меньшую свободную поверхностную энергию.
При нарушении агрегативной устойчивости суспензии происходит коагуляция — слипание частиц дисперсной фазы. Коагуляция — это самопроизвольный процесс, так как сопровождается уменьшением свободной энергии системы за счет уменьшения межфазной поверхности. Этот процесс аналогичен тому, который происходит в лиозолях, более того, коагуляция лиозолей приводит к образованию суспензий и далее может продолжаться в них, приводя к образованию осадка. Этот осадок часто является концентрированной суспензией (пастой) — т. е. структурированной системой.
Для достижения агрегативной устойчивости суспензии необходимо выполнение по крайней мере одного из двух условий:
• смачиваемость поверхности частиц дисперсной фазы дисперсионной средой;
• наличие стабилизатора.
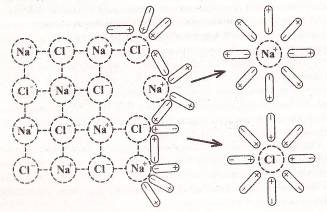
Первое условие. Если частицы суспензии хорошо смачиваются дисперсионной средой, то на их поверхности образуется сольватная оболочка, обладающая упругими свойствами и препятствующая соединению частиц в крупные агрегаты. Хорошая смачиваемость частиц наблюдается в суспензиях полярных частиц в полярных жидкостях и неполярных частиц в неполярных жидкостях.
Примером агрегативно устойчивых суспензий без стабилизатора с сольватационным механизмом устойчивости являются суспензии кварца в воде и сажи в бензоле. Так как кварц хорошо смачивается водой, а сажа — бензолом, эти суспензии агрегативно устойчивы без третьего компонента — стабилизатора. Если заменить дисперсионную среду, исключая тем самым смачивание (например, размешать порошок сажи в воде), то получается агрегативно неустойчивая система — частицы сажи водой не смачиваются, гидратная оболочка не образуется и незащищенные частички легко соединяются друг с другом.
Второе условие. Если частицы суспензии не смачиваются или плохо смачиваются дисперсионной средой, то используют стабилизатор.
Стабилизатор — это вещество, добавление которого в дисперсную систему повышает ее агрегативную устойчивость, т. е. препятствует слипанию частиц.
В качестве стабилизаторов суспензий применяют:
• низкомолекулярные электролиты;
• коллоидные ПАВ;
• ВМС.
Механизм их стабилизирующего действия различен, в зависимости от природы стабилизатора реализуется один, а чаще несколько факторов устойчивости, аналогично тому, как это происходит в лиофобных золях. Отметим возможные факторы устойчивости:
адсорбционно-сольватный,
электростатический,
структурно-механический,
энтропийный,
гидродинамический.
Если стабилизатор является ионогенным веществом (распадается в растворе на ионы), то обязательно действует электростатический фактор устойчивости: на поверхности частиц образуется двойной электрический слой, возникает электрокинетический потенциал и соответствующие электростатические силы отталкивания, препятствующие слипанию частиц. Электростатическое отталкивание частиц описано теорией. Если это ионогенное вещество — низкомолекулярный неорганический электролит, то его стабилизирующее действие ограничивается только этим фактором. Если же ионогенное вещество — коллоидное ПАВ или полиэлектролит, то реализуются и другие факторы устойчивости, рассмотрим их подробнее.
СТАБИЛИЗИРУЮЩЕЕ ДЕЙСТВИЕ КОЛЛОИДНЫХ ПАВ
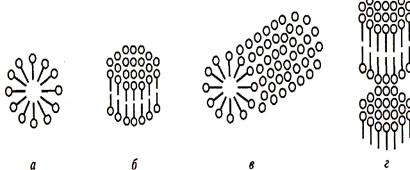
Стабилизирующее действие коллоидных ПАВ определяется их способностью адсорбироваться на межфазной поверхности, образуя адсорбционные пленки. Вследствие высокой поверхностной активности концентрация ПАВ в поверхностном слое в десятки тысяч раз превышает объемную концентрацию, поэтому в адсорбционных пленках, так же как и в мицеллах ПАВ, происходит ассоциация неполярных групп. Строение адсорбционного слоя зависит от:
• природы ПАВ;
• природы межфазной поверхности (границы: «твердая частица-жидкая среда»);
• степени заполнения поверхности;
• наличия в дисперсионной среде различных добавок. Изменение строения адсорбционного слоя отражается на его защитных свойствах.
Коллоидное ПАВ, имея дифильное строение, способно адсорбироваться как на полярных, так и на неполярных поверхностях, лиофилизируя их.
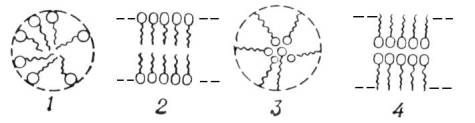
В соответствии с правилом уравнивания полярностей Ребиндера стабилизирующее действие ПАВ проявляется тем заметнее, чем больше первоначальная разница в полярностях твердой частицы и жидкой дисперсионной среды. Таким образом, при использовании в качестве стабилизатора коллоидного ПАВ реализуется адсорбционно-сольватный фактор устойчивости. Например, чтобы получить суспензию сажи в воде, используют олеат натрия, который неполярным углеводородным радикалом адсорбируется на частицах сажи, а полярная группа, направленная в сторону воды, ею гидратируется и тем самым поверхность частицы становится смачиваемой водой (гидрофилизируется), суспензия стабилизируется. Аналогичный процесс мы проводим, когда моем руки, загрязненные сажей, или моем посуду после жирной пищи.
Олеат натрия:
Олеат натрия можно использовать и для стабилизации суспензии силикагеля (SiO2) в бензоле (неполярная жидкость):
Бензол
В этом случае олеат натрия будет адсорбироваться на поверхности твердой частицы своей полярной группой, направляя углеводородный радикал в сторону бензола. Тем самым поверхность силикагеля становится гидрофобной, бензол ее смачивает, и суспензия стабилизируется.1
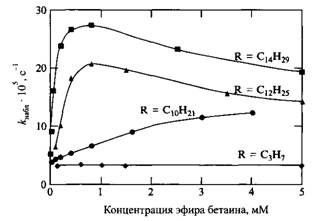
Но лучший стабилизирующий эффект достигается при более специфическом выборе ПАВ. Подбор ПАВ для стабилизации суспензий различного типа сходен с подбором ПАВ для стабилизации прямых и обратных эмульсий. Если необходимо стабилизировать суспензию полярных частиц в неполярной жидкости, то используется коллоидное ПАВ с низкими значениями чисел ГЛБ, обычно 3-6, т. е. малорастворимые в воде, известны случаи стабилизации ПАВ с 30 атомами углерода в цепи.
В пищевой промышленности для этих целей используются липоиды (лецитин), ланолин и т. д.
Если необходимо стабилизировать суспензию неполярных частиц в полярной жидкости, то применяются коллоидные ПАВ с высокими значениями чисел ГЛБ, обычно 8-13, т. е. достаточно хорошо растворимые в воде, такие соединения содержат 10-18 атомов углерода в цепи.
Максимум стабилизирующих свойств наблюдается у ПАВ с 14-16 атомами углерода (так называемый максимум Донана). В пищевой промышленности для этих целей часто используют пропиловый спирт, соли высших карбоновых кислот и т. д.
СТАБИЛИЗИРУЮЩЕЕ ДЕЙСТВИЕ ВМС И ПОЛИЭЛЕКТРОЛИТОВ
Строго говоря, в качестве стабилизаторов дисперсных систем, в том числе и суспензий, можно использовать только такие ВМС, которые являются поверхностно-активными веществами и их надо было бы называть поверхностно-активными высокомолекулярными веществами (ПАВМС или ВМПАВ). Чтобы оказать защитное действие, молекулам полимера необходимо адсорбироваться на поверхности частицы, а это может произойти только в том случае, .если при этом уменьшится поверхностное натяжение на границе раздела фаз. Эти вещества отличаются от коллоидных ПАВ тем, что для них характерно возникновение структурно-механического фактора устойчивости.
Таким образом, если в качестве стабилизатора применяются ВМС, то механизм их действия аналогичен механизму коллоидной защиты лиофобных золей: адсорбция молекул полимера на твердых частицах приводит к возникновению защитной оболочки, обладающей механической прочностью и упругостью, причем отмечено, что адсорбция ВМС является необратимой. Для этого вокруг частицы должен существовать избыток макромолекул, необходимый для образования насыщенного монослоя или даже полислоя. Электронномикроскопические снимки непосредственно доказали наличие таких защитных оболочек. Например, адсорбционные слои метилцеллюлозы на частицах полистирола имеют толщину 70-100 А˚. Таким образом, возникает структурно-механический фактор устойчивости, полностью предотвращающий коагуляцию частиц и возникновение между ними непосредственного контакта. Он играет главную роль в обеспечении агрегативной устойчивости суспензий. Обычно он сопровождается энтропийным фактором устойчивости, вклад которого достаточно велик. Это обусловлено тем, что при сближении частиц, стабилизированных молекулами ВМС, уменьшается число возможных конформаций молекул полимера, а это приводит к уменьшению энтропии системы, поэтому частицы стремятся оттолкнуться друг от друга.
Если в качестве ВМС используются полиэлектролиты, то к этим двум факторам добавляется и третий — электростатический фактор устойчивости. Полиэлектролиты-стабилизаторы применяются для водных суспензий, т. е. для стабилизации гидрофобных частиц в полярных жидкостях. Наиболее распространенные водорастворимые полиэлектролиты — это белковые вещества, альгинаты, карбоксиметилцеллюлоза, алкилполиамин и т. д.
СЕНСИБИЛИЗАЦИЯ
При использовании ВМС в качестве стабилизаторов суспензий надо помнить о таком явлении как сенсибилизация. Сенсибилизация — явление уменьшения агрегативной устойчивости системы при добавлении к ней высокомолекулярных соединений.
Ранее это явление рассматривалось в отношении лиофобных золей, но оно характерно и для суспензий. Сенсибилизация, как правило, обнаруживается при малом содержании макромолекул в дисперсионной среде и объясняется образованием между отдельными частицами мостиков стабилизатора. В суспензиях каолина и полистирола возникновение мостиков доказано электронномикроскопическими исследованиями: концентрациям метилцеллюлозы до 1-2% от веса твердой фазы обычно отвечает неустойчивое, а выше 4% — устойчивое состояние суспензии.
Таким образом, решающее влияние на защитное действие макромолекул оказывает соотношение между количеством полимера и удельной поверхностью частиц.
Для стабилизации суспензии полистирола необходима поверхностная концентрация метилцеллюлозы 6 · 10 -4 г/м2. Аналогичные соотношения установлены и для других ВМС.
В заключение можно сказать, что агрегативная устойчивость суспензий в сильной степени зависит от специфического взаимодействия макромолекул с поверхностью частиц дисперсной фазы. Следовательно, выбор ВМС для стабилизации суспензии носит, во многом, эмпирический характер.
АЭРОЗОЛИ
Аэрозолем называется микрогетерогенная система, в которой частички твердого вещества или капельки жидкости взвешены в газе. Условное обозначение аэрозолей: Т/Г или Ж/Г.
Чтобы было ясно, насколько важным является этот вид дисперсных систем, приведем примеры аэрозолей. Космическое пространство, атмосфера Земли, воздух, которым мы дышим, — все это аэрозоли. Аэрозоли возникают естественным путем, образуются искусственно и сопутствуют промышленному производству.
Ветер поднимает и разносит облака пыли, создавая пыльные бури. Пыль может подниматься на высоту 5— 6 км и переноситься на расстояния, измеряемые тысячами километров. В Норвегии, например, была обнаружена пыль пустыни Сахара. При извержении вулканов, а их на Земле более 600, в атмосферу выбрасывается несколько десятков миллионов тонн грунта, большая часть которого переходит в аэрозольное состояние. Так, в результате гигантского извержения вулкана Тамбора в Индонезии в 1815 г. в стратосферу было выброшено такое количество пыли, что следующий, 1816 г., вошел в историю как «год без лета». Микроорганизмы, вирусы и споры растений подхватываются потоком воздуха и образуют аэрозоли. Споры плесени и дрожжей находят в атмосфере на высоте свыше 11 км. Аэрозоли биологического происхождения переносятся на огромные расстояния — были отмечены случаи, когда споры грибов были обнаружены над Карибским морем в 1000 км от ближайшего возможного места их образования. Вода, испаряемая с водной поверхности Земли, образует аэрозоли, разрушение которых приводит к возникновению дождя, снега, града. До 30% всех естественных аэрозолей дает космическая пыль. Все это — аэрозоли, которые возникают естественным путем, без участия человека.
Около 10% всех аэрозолей получается искусственно: это распыление ядохимикатов и удобрений, орошение, бытовые аэрозоли и т. д.
И, наконец, третья группа аэрозолей — это промышленные аэрозоли. В шахтах, карьерах для добычи полезных ископаемых, около металлургических и химических комбинатов, при работе различных агрегатов (дробилок, мельниц, многочисленных котельных) образуются аэрозоли, загрязняющие воздух. Все виды наземного, воздушного и водного транспорта являются источниками аэрозолей за счет сгорания топлива. Достаточно отметить, что в результате сгорания топлива ежегодно выбрасывается в атмосферу более 100 т твердых и 1 млн т газообразных веществ. Производство ядерного топлива, эксплуатация атомных электростанций, испытания ядерного оружия приводят к образованию радиоактивных аэрозолей.
Таковы основные источники образования аэрозолей. Ежегодно в среднем 1 км2 земной поверхности выбрасывает в атмосферу 20 т раздробленной массы, которая превращается в атмосферные аэрозоли.
КЛАССИФИКАЦИЯ АЭРОЗОЛЕЙ
1. По агрегатному состоянию дисперсной фазы:
· туман (Ж/Г);
· дым, пыль (Т/Г);
· смог (Ж+Т)/Г [Smog] = Smoke (дым) + fog (туман)
2. По дисперсности:
· туман (Ж/Г), 10-7 <d< 10-5 м;
· дым (Т/Г), 10-9 < d < 10-5 м;
· пыль Т/Г, d > 10-5 м.
3. По методам получения:
· конденсационные;
· диспергационные.
МЕТОДЫ ПОЛУЧЕНИЯ АЭРОЗОЛЕЙ
Как и другие микрогетерогенные системы, аэрозоли могут быть получены двумя разными путями:
из грубо-дисперсных систем (диспергационные методы),
из истинных растворов (конденсационные методы).
КОНДЕНСАЦИОННЫЕ МЕТОДЫ
Эти методы связаны с образованием в гомогенной системе новой фазы. Обязательным условием ее образования является наличие пересыщенного пара, конденсация которого и приводит к образованию частиц дисперсной фазы. Объемная конденсация пересыщенного пара может происходить в трех случаях:
при адиабатическом расширении;
при смешении паров и газов, имеющих разные температуры;
при охлаждении газовой смеси.
1. Адиабатическое расширение газа.
Таким путем образуются облака. Теплые массы влажного воздуха поднимаются в более высокие слои атмосферы. Поскольку там атмосферное давление ниже, происходит адиабатическое расширение, сопровождающееся охлаждением воздуха и конденсацией водяного пара. На относительно небольшой высоте образуются кучевые облака, в которых вода находится в виде жидких капель, в верхних же слоях атмосферы, где температура более низкая, возникают перистые облака, содержащие кристаллики льда.
Похожие работы
... образом зависят от их микроструктуры. Контроль размера, распределения по размерам и морфологии отдельных зерен или кристаллитов чрезвычайно важен для получения материалов с заданными свойствами. Химические реакции в микроэмульсиях используют как один из возможных путей получения тонкодисперсных частиц. В таблице 1 приведены примеры областей, в которых используется микроэмульсионный метод получения ...
... натрия: Объем раствора нитрата серебра 2000, 42 мл----------------------------х мл 58 г/моль 107 г/моль х = 2000, 42*107 /58 = 3690,43 мл Соотношение объемов веществ: 98. Коагуляция дисперсной системы. Скорость коагуляции. Причины, вызывающие процесс самопроизвольной коагуляции. Коагуляция – процесс самопроизвольного укрупнения (слипания) дисперсных частиц, ...
... . Реакция среды в этом случае зависит от соотношения констант диссоциации соответствующих основания и кислоты. Усилить гидролиз можно разбавлением раствора, нагреванием системы. 2. Химические реакции Химические реакции (химические явления) – это процессы, в результате которых одни вещества превращаются в другие. Признаками осуществления химических реакций являются: – изменение цвета; ...
... и многое другое, без чего немыслима сама жизнь. Все человеческое тело – это мир частиц, находящихся в постоянном движении строго по определенным правилам, подчиняющимся физиологии человека. Коллоидные системы организмов обладают рядом биологических свойств, характеризующих то или иное коллоидное состояние: 2.2 Коллоидная система клеток. С точки зрения коллоидно-химической физиологии ...

0 комментариев