Навигация
Министерство Образования и Науки РФ
Казанский Государственный Технологический Университет
Кафедра Общей Химической Технологии
Реферат
по курсу: Технология химических производств
на тему:
Хлорирование метана
Казань 2008
Содержание
Хлорирование метана
Технологические и технико-экономические показатели
Реклама
Список литературы
Хлорирование метана
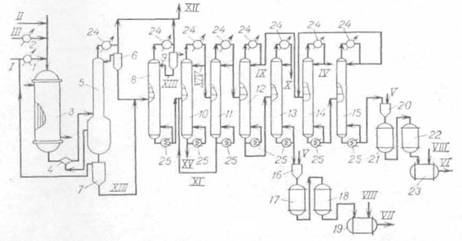
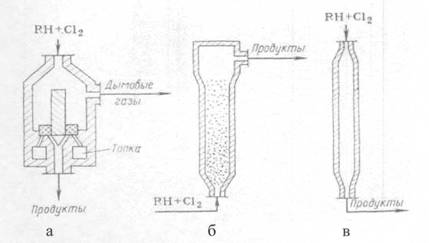
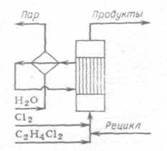
Процесс совместного получения хлорметанов можно осуществлять в реакторе со стационарным или псевдоожиженным слоем катализатора. Вторая технология более перспективна, она включает следующие стадии: хлорирование в псевдоожиженном слое катализатора; пылеулавливание и отпаривание газов кислотного характера; абсорбция хлороводорода; нейтрализация и осушка рециркулирующего реакционного газа; компримироваиие рециркулирующих газов; ректификация хлорметанов с выделением товарных продуктов.
Хлор и метан подают в реактор в соотношении от 1: 2 до 3,88: 1 в зависимости от того, какое хлорпроизводное желательно получить. Например, при соотношении С12: СН4-1: 2 образуется продукт, содержащий [п% (мол)]: СН3С1 - 62; СН2С12 - 30; СНС13 - 7; СС14 - 1; при соотношении С12: СН4 = 3,88: 1 образуется продукт, содержащий только 4% (мол) СНС13 и 96% (мол) СС14.
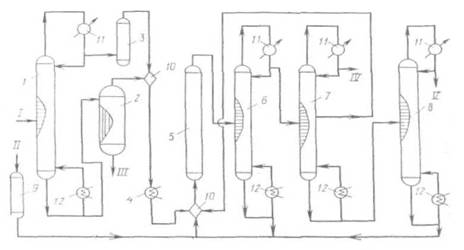
Метан и хлор поступают в реактор 1 с псевдоожиженным слоем катализатора. Реактор выполнен из хромоникелевоп стали.
Хлорирование ведут; при 350 °С и атмосферном давлении, время контакта 0,1-20 с. Реакционная смесь проходит систему пылеулавливания (циклон 2) и поступает на нейтрализацию в колонну 3, где отпариваются кислые газы. После этой колонны продукты реакции промывают водой в скруббере 6; при этом получается товарная соляная кислота. Далее газы нейтрализуют раствором щелочи в скруббере 7 и осушают серной кислотой в скруббере 8.
Нейтрализованные газы, содержащие в основном метан и метилхлорид, компримируют и возвращают в реактор на хлорирование. Конденсат после отпаривания кислых газов поступает на ректификацию в колонны 10, 12 и 13, в которых последовательно выделяют метиленхлорид, хлороформ и тетрахлорид углерода.
Для удалении инертных примесей часть реакционного газа после компрессора 9 и скруббера 6 выводят в атмосферу (на схеме не показано). Расход основного сырья на 1 т готового продукта составляет 133 кг метана и 1784 кг хлора.
В процессе на 1 т хлороформа образуется 0,9 т метиленхлорида и 0,5 т тетрахлорида углерода. Кубовые остатки (в основном со стадии ректификации) в количестве 0,01 т на 1 т хлороформа направляют па установку термического обезвреживания. В процессе образуется соляная кислота (примерно 1 т па 1 т хлороформа), которую после очистки от хлорорганических примесей можно применять вместо синтетической. Отработанную серную кислоту (0,1 т на 1 т хлороформа) передают на производство сульфата натрия.
Задание:
Составить и описать технологическую схему процесса хлорирование метана
Составить материальный баланс процесса
Рассчитать технологические технико-экономические показатели
В основу расчета принять следующие реакции:
CH4+Cl2→CH3Cl+HCl
CH3Cl+Cl2→CH2Cl2+HCl
CH2Cl2+Cl2→CHCl2+HCl
CHCl3+Cl2→CCl4+HCl
Исходные данные:
| Производительность установки по хлорсодержащим продуктам, т/сут | 60 |
| Состав сырья,% масс природный газ с содержание метана технический хлор с содержанием примесей | 93 1.5 |
| Состав продуктов,% моль метан хлористый метан хлористый метилен хлороформ четыреххлористый углерод | 32 18 25 20 5 |
| Мольное соотношение хлор-метан | 2.6 |
| Потери метана,% масс | 1.3 |
Материальный баланс. Схема потоков:

![]()
![]() CH4; Cl2; природный газ; CH3Cl; CH2Cl2; CHCl3; CCl4; CH4;
CH4; Cl2; природный газ; CH3Cl; CH2Cl2; CHCl3; CCl4; CH4;
примесь Cl2 Cl2; прир. газ; примесь Cl2; HCl
| Приход | Расход | |||
| кг/ч | кмоль/ч | кг/ч | кмоль/ч | |
| CH4 Cl2 CH3Cl CH2Cl2 CHCl3 CCl4 HCl прим. CH4 прим. Cl2 | 604,88 6969,9 0 0 0 0 0 45,53 106,14 | 37,81 98,306 0 0 0 0 0 | 191 + 7,76 3053,38 339 792,25 890,75 287 2013,5 45,53 106,14 | 11,94 + 0,485 43,07 6,72 9,33 7,46 1,87 55,24 |
| Σ1 = 7726,45 | Σ2 = 7726,31 | |||
Молярные массы веществ:
Mr (CH4) = 12+4=16 кг/кмоль
Mr (Cl2) = 35,45*2=70,9 кг/кмоль
Mr (CH3Cl) = 12+3+35,45=50,45 кг/кмоль
Mr (CH2Cl2) = 12+2+35,45*2=84,9 кг/кмоль
Mr (CHCl3) = 12+1+35,45*3=119,35 кг/кмоль
Mr (CCl4) = 12+35,45*4=153,8 кг/кмоль
Mr (HCl) = 1+35,45=36,45 кг/кмоль.
Похожие работы
... радикал (изопропил); (СН3)3С— - третичный одновалентный радикал (mpem-бутил). 1.2. Номенклатура и изомерия Номенклатура. Для названия предельных углеводородов применяют в основном систематическую и рациональную номенклатуры. Названия первых четырех членов гомологического ряда метана тривиальные: метан, этан, пропан, бутан. Начиная с пятого названия образованы от греческих числительных с ...
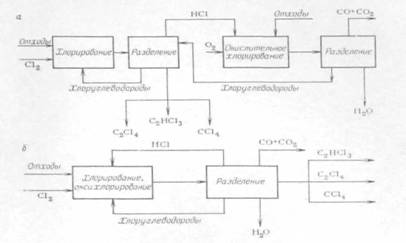
... СС12=СС12 + 5НС1 (2.26) Побочно получаются продукты конденсации (гексахлорбутадиен-1,3, гексахлорбензол), которые в этих условиях не подвергаются хлоролизу, и их уничтожают. Технологическая схема производства тетрахлорметана и тетрахлорэтилена из хлорорганических отходов изображена на рис. 2.1. Смесь отходов подают в испаритель 1, где отделяются тяжелые продукты, направляемые на сжигание. Пары ...
ие химические превращения их, большое внимание уделял реакциям галоидирования, в том числе хлорирования углеводородов и их производных. Капитальным вкладом в разработку теоретических основ реакций хлорирования парафиновых углеводородов явились известные исследования В.В. Марковникова по теории взаимного влияния атомов в молекулах химических соединений. Пользуясь большим экспериментальным ...
... - С=С - Н + ЗН2 Эта реакция дегидрирования (отщепления водорода) имеет большое промышленное значение, так же как и дегидрирование других предельных углеводородов, в том числе этана С2Н6: Углеводороды нормального строения под влиянием катализаторов и при нагревании подвергаются реакциям изомеризации и превращаются в углеводороды разветвленного строения: пентан 2-метилбутан Применение метана ...

0 комментариев