Навигация
Предельные, или насыщенные, углеводороды ряда метана (алканы, или парафины)
Алканы, или парафины — алифатические предельные углеводороды, в молекулах которых атомы углерода связаны между собой простой (одинарной) (s-связью.
Оставшиеся валентности углеродного атома, не затраченные на связь с другими атомами углерода, полностью насыщены водородом. Поэтому предельные (насыщенные) углеводороды содержат в молекуле максимальное число водородных атомов.
1.1. Строение алканов
Простейшим представителем и родоначальником предельных углеводородов является метан СН4. Строение молекулы метана можно выразить структурной (I) или электронной (II) формулой:
| H | H—C—H | H (I) | H .. H :C : H .. H (II) |
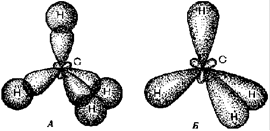
В предельных углеводородах атомы углерода находятся в первом валентном состоянии (sp3-гибpидизaция). В этом случае, .как известно, все четыре гибридные орбитали в пространстве составляют геометрическую фигуру — тетраэдр (углы между осями связей С—Н равны 109° 28'). Пространственное расположение атомов в молекуле метана можно показать с помощью тетраэдрических и шаростержневых моделей. Для этого наиболее удобны объемные модели Бриглеба, которые более наглядно отражают относительные размеры атомов в молекуле. Эти модели изготовлены в соответствии с действительным соотношением радиусов атомов (в масштабе 0,05 нм = 1 см).
Если в молекуле метана один атом водорода заместить на метильную группу СН3, то можно вывести структурную формулу следующего за метаном углеводорода — этана C2H6:
| H H | | H—C—C—H | | H H |
или H3C—CH3 |
Замещая в молекуле этана один атом водорода на метальную группу, выводим формулу третьего углеводорода — пропана С3Н8:
| H H H | | | H—C—C—С—H | | | H H H |
или H3C—CH2—CH3 |
Повторяя это действие много раз, можно вывести формулы и других предельных углеводородов, отличающихся друг от друга числом углеродных атомов (табл. 1). В результате образуется ряд соединений, в котором каждый член отличается от предыдущего на одну группу СН2. Такой ряд называется гомологическим рядом (от греч. homos — последовательный), а его отдельные члены — гомологами. Они обладают близкими химическими свойствами и закономерным изменением физических свойств. Из табл. 1 видно, что у каждого члена гомологического ряда на п атомов углерода приходится 2n + 2 атомов водорода. Следовательно, состав любого члена этого ряда будет выражаться общей формулой СnН2n + 2. Используя эту формулу, можно легко написать молекулярную формулу любого предельного углеводорода — алкана, зная число углеродных атомов в его молекуле. Например, если п = 25, то углерод будет выражаться формулой C25H52.
Таблица 1. Гомологический ряд предельных углеводородов (алканов) нормального (неразветвленного) строения и их одновалентные радикалы
| Углеводород (алкан) | Число возможных изомеров у алкана | Радикал (алкил) | ||
| Формула | Название | Формула | Название | |
| СН4 | Метан | 1 | СН3- | Метил |
| С2Н6 | Этан | 1 | С2Н5- | Этил |
| С3Н8 | Пропан | 1 | С3Н7- | Пропил |
| С4Н10 | Бутан | 2 | С4Н9- | Бутил |
| С5Н12 | Пентан | 3 | С5Н11- | Пентил |
| С6Н14 | Гексан | 5 | С6Н13- | Гексил |
| C7H16 | Гептан | 9 | C7H15- | Гептил |
| C8H18 | Октан | 18 | C8H17- | Октил |
| С9Н20 | Нонан | 35 | С9Н19- | Нонил |
| С10Н22 | Декан | 75 | С10Н21- | Децил (декил) |
Гомологические ряды характерны для всех классов органических соединений. Они являются прекрасным подтверждением основного закона природы — перехода количественных изменений в качественные.
Если от алкана "отнять" один атом водорода, то образуется одновалентный углеводородный остаток — радикал (не смешивайте с реально существующим свободным радикалом). При потере двух или трех атомов водорода образуются соответственно двух- или трехвалентные радикалы (табл. 2).
Таблица 2. Наиболее часто встречающиеся углеводородные радикалы
| Название | Формула радикала | Название | Формула радикала |
| Метил | СН3— | Этил | CH3—CH2— |
| Метилен | СН2== | Этилиден | CH3—CH== |
| Метин | СНºº | Этилидин | CH3—Cºº |
| н-Пропил | CH3—CH2—CH2— | Изобутил (первичный изобутил) | (СН3)2СН—СН2— |
| Пропилиден | CH3—CH2—CH== | втор-Бутил | CH3 | CH3—CH2—CH— |
| Изопропил | (СН3)2СН— | терет-Бутил | (СН3)3С— |
| н-Бутил | CH3—CH2—CH2—CH2— | н-Пентил | CH3—CH2—CH2—CH2—CH2— |
В приведенных названиях радикалов используют обозначения: н-нормальный, втор- — вторичный, трет- — третичный.
Как видно из табл. 2, свободная валентность в радикале может находиться при разных углеродных атомах. Если свободная валентность в радикале находится у первичного атома углерода, то такой радикал называется первичным. Соответственно этому могут быть вторичные (свободная валентность принадлежит вторичному атому углерода) и третичные (свободная валентность у третичного углеродного атома) радикалы:.
Н3С— - первичный одновалентный радикал (метил);
(СН3)2СН— - вторичный одновалентный радикал (изопропил);
(СН3)3С— - третичный одновалентный радикал (mpem-бутил).
Похожие работы
... образующих этот ряд соединениях одинаково и может быть выражено общей формулой СnH2n+2, где n – число атомов углерода. Все эти вещества подобно метану являются предельными, насыщенными углеводородами. Такой ряд соединений, расположенных в порядке возрастания числа углеродных атомов, в котором каждый последующий член ряда отличается по составу от предыдущего на группу СН2, причем состав каждого ...
... СН3 b-метилнафталин (эталон вещества с наиболее плохой способностью к воспламенению) Способы получения насыщенных углеводородов Каждый класс органических веществ, в том числе предельные углеводороды, характеризуется рядом общих методов синтеза. Последние позволяют судить о связи соединений данного класса с веществом других классов и о путях их взаимных превращений. Кроме того ...
... - С=С - Н + ЗН2 Эта реакция дегидрирования (отщепления водорода) имеет большое промышленное значение, так же как и дегидрирование других предельных углеводородов, в том числе этана С2Н6: Углеводороды нормального строения под влиянием катализаторов и при нагревании подвергаются реакциям изомеризации и превращаются в углеводороды разветвленного строения: пентан 2-метилбутан Применение метана ...
... учебного процесса; 4) Абсолютно неудовлетворительная объективность оценки знаний обучающихся, невозможность сопоставления оценок, полученных или разных обучающих или, тем более, в разных учебных заведениях [10]. 1.8 Тестовый контроль знаний на уроках химии В последние годы в связи с проведением в стране эксперимента по внедрению единого государственного экзамена (ЕГЭ) тестовые задания все ...


0 комментариев