Навигация
Реакторы для процессов с использованием иммобилизованных катализаторов
14. Реакторы для процессов с использованием иммобилизованных катализаторов
Иммобилизованные биокаталитические системы функционируют в биореакторе в виде неподвижной фазы, через которую протекает среда с субстратом, подлежащим биоконверсии. Возможны различные инженерные решения для подобного проточного биореактора. Наряду с непрерывным в таких реакторах используют и периодический режим. Аппараты для иммобилизованных биокатализаторов имеют аналогию с реакторами для химических процессов с гетерогенным катализом.
Если иммобилизованные катализаторы имеют вид гранул, то важной задачей является их максимально плотная упаковка в аппарате. Таким путем реализуют еще одно преимущество метода — возможность повышения концентрации биообъекта в реакторе, что влечет за собой и более высокий выход целевого продукта. Например, плотность популяции животных клеток in vitro не превышает 106 на 1 мл среды, тогда как в составе гелевых гранул или капсул достигает 108— 109на 1 мл.
Плотную упаковку реализуют в биореакторе с циркуляционным перемешиванием и насадкой, роль которой играют гранулы с иммобилизованным биокатализатором. Это один из преобладающих типов биореакторов для иммобилизованных биокаталитических систем, используемый, например, для получения спирта с помощью клеток дрожжей или бактерий Zymomonas mobilis. Применение циркуляционных биореакторов с насадкой порождает, однако, серьезные проблемы: 1) недостаточно эффективное перемешивание, что обусловливает формирование нежелательных температурных, концентрационных и рН-градиентов в объеме аппарата; 2) затруднения с удалением ССЬ и других газообразных продуктов, которые, прокладывая себе путь к верхней части аппарата, разрушают гранулы с иммобилизованным биокатализатором.
Для улучшения перемешивания и газообмена биореактор снабжают механической мешалкой, что ощутимо повышает энергозатраты и может быть причиной разрушения гранул. Борьба с повреждающим действием мешалки ведется путем укрепления гранул. Отметим, что мембранные капсулы для животных клеток обладают прочностью, достаточной для сохранения их целостности при работе механической мешалки. Свободные животные клетки при тех же оборотах мешалки подвергаются лизису.
Предохранение гранул с катализатором от повреждения мешалкой достигается в биореакторе «корзиночного» типа. Биореактор снабжен мешалкой, которая вращается в полом цилиндре из проволочной сетки — «корзине». «Корзина» несет в своих ячейках гранулы, содержащие биокатализатор. Получаются два уровня иммобилизации — гранулы с иммобилизованным биокатализатором, которые, в свою очередь, фиксированы в ячейках проволочной сетки. Проволочная корзина предохраняет гранулы от разрушения в процессе перемешивания.
. Для стимуляции газообмена предложена оригинальная конструкция реактора, в частности для целых клеток, включенных в полимерный гель. Этот гель не оформляют в виде гранул, а еще незастывшим заливают в аппарат, где и происходит гелеобразование. Например, гелеобразование альгината вызывают добавлением Са2+. Получается монолит геля с иммобилизованным биокатализатором. В этой массе геля прорезают вертикальные каналы для оттока газов. Такие каналы можно изготовить, поместив в биореактор с незастывшим гелем вертикально ориентиро ванные стержни. Подобный биореактор не дает, однако, возможности реализовать принцип протока и поэтому годится лишь для периодического режима работы.
Для биокатализаторов, иммобилизованных в полых волокнах, создан специальный реактор. Раствор субстрата протекает через сосуд, рыхло заполненный полыми волокнами, во внутреннем объеме которых содержится биокатализатор. В таком биореакторе достигнута 90%-ная конверсия фумарата аммония в аспартат с помощью клеток Е, coli.
Имеются сообщения о пневматических (эрлифтных, колоночных) биореакторах для иммобилизованных растительных клеток.
Колонны с насадкой иммобилизованного катализатора в настоящее время используются в нескольких промышленных процессах, и есть все основания полагать, что в ближайшее время область их применения существенно расширится. В таких реакторах, называемых реакторами с неподвижным слоем катализатора, с помощью иммобилизованных ферментов осуществляют изомеризацию глюкозы, частичный селективный гидролиз пенициллина, селективное расщепление смеси производных рацемических аминокислот. В реакторах с неподвижным слоем изучались также процессы с участием иммобилизованных клеток.
В простейшем и часто довольно успешно применяющемся математическом описании работы реактора с неподвижным слоем катализатора в основу положена модель реактора полного вытеснения, модифицированная с целью учета влияния каталитической насадки на структуру течений и кинетику реакций. Поверхностную скорость потока через реактов определяют как объемную скорость потока исходных веществ, отнесенного к площади поперечного сечения пустот, которое представляет собой произведение общей площади поперечного сечения колонны на долю пустот .
Для простой реакции S>T, протекающей с собственной скоростью v = v (s, p), скорость образования продукта в единице объема гранулы иммобилизованного катализатора в какой-либо определенной точке реактора равна:
vобщ = (ss, ps)v(ss, ps)
Здесь ss и ps концентрации субстрата и продукта соответственно на наружной поверхности частицы катализатора в данной точке объема реактора. Как указано в уравнении (1), в общем случае коэффициент эффективности , определяющий скорость диффузии в частицу катализатора, и скорость реакции v зависят как от ss, так и от ps.
Математический балланс по сустрату в сферический частице катализатора радиусом R в стационарном состоянии будет выражаться уравнением:
4R2ks(sss) = 4/3R3(ss, ps)v(ss, ps)
или: Скорость диффузии субстрата из жидкой фазы = скорости трансформации субстрата внутри частицы в результате реакции.
Преобразование и подстановка величин уравнений (1) и (2) дает выражение, позволяющее определить общую скорость утилизации субстрата, отнесенную к единице объема частиц катализатора, если известна концентрация субстрата в жидкой фазе.
Течение вокруг частицы, составляющих слой насадки, и особенно смешения жидкой фазы в пустотах между частицами создают обратное смещение, которое может вызвать отклонение от режима полного вытеснения. В таких случаях можно применять дисперсионную модель или модель на основе каскада реакторов. Влияние небольшой дисперсии на работу реактора в сравнении с режимом идеального вытеснения мы уже обсуждали при изучении стерилизаторов.
15. Гидролиз растительного сырья. ПреколяцияПроизводственной основой современной биотехнологии является микробиологическая промышленность, включающая гидролизные производства. Эти производства основаны на реакции гидролитического расщепления гликозидных связей полисахаридов биомассы одревесневшего растительного сырья с образованием в качестве основных продуктов реакции моносахаридов, которые подвергаются дальнейшей биохимической или химической переработке, либо входят в состав товарной продукции.
Гидролиз растительного сырья — наиболее перспективный метод химической переработки древесины, так как в сочетании с биотехнологическими процессами позволяет получать кормовые и пищевые продукты, биологически активные препараты, мономеры и синтетические смолы, топливо для двигателей внутреннего сгорания и разнообразные продукты для технических целей.
Созданию отечественной гидролизной промышленности предшествовали многолетние исследовательские и опытные работы, которые обеспечили необходимые предпосылки для разработки современной технологии гидролиза растительного сырья и получения этанола, кормовых дрожжей, фурфурола, ксилита и других продуктов.
В качестве исходного сырья для получения этих веществ и продуктов используются источники органического углерода — различные углеводы, органические кислоты, а в производстве кормового белка и углеводороды нефти. Потребляемый микроорганизмами связанный азот используется в виде синтетического аммиака или его производных, а необходимый для биохимических процессов фосфор — в виде растворимых в воде солей фосфорной кислоты. В результате ферментативных процессов, протекающих в микроорганизмах, из этих веществ образуются разнообразные белки, нуклеиновые кислоты, жиры и многочисленные биологически активные вещества, к которым относятся витамины, антибиотики, ферменты и др.
Большая часть производств, объединяемых микробиологической промышленностью, основана на использовании в качестве источника углерода различных углеводов, накапливающихся в зеленых растениях. Под действием хлорофилла и света из углекислоты и воды в зеленых частях растений синтезируется сахароза С12Н22О11, из которой в результате сложных биохимических превращений образуется все разнообразие органических соединений, входящих в состав однолетних и многолетних растений.
Часть растений, накапливающих сахарозу в значительных количествах (сахарный тростник, сахарная свекла), используется в промышленности для ее получения. В других растениях сахароза превращается в резервный полисахарид — крахмал, получивший широкое применение как основной источник питания человека и многих животных, а также как сырье в ряде микробиологических процессов. Огромные ресурсы полисахаридов, часть которых ежегодно возобновляется, также являются потенциальным сырьем для ряда производств микробиологической промышленности. Однако перед использованием их в этом направлении полисахариды клеточных стенок должны быть вначале превращены в соответствующие моносахариды путем присоединения к ним элементов воды. Примером такой реакции может быть превращение целлюлозы в глюкозу:
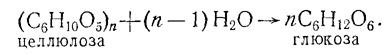
Реакция присоединения воды к полисахаридам с образованием исходных простейших Сахаров носит название гидролиза (от двух греческих слов: хидор — вода и лизис — расторжение). Этот процесс положен в основу гидролизной промышленности, на предприятиях которой полисахариды клеточных стенок растений в результате реакции гидролиза превращаются в смесь моносахаридов: пентоз (С5Н1005) и гексоз (С6Н12О6).
Водный раствор продуктов гидролиза, получивший название гидролизата, после соответствующей очистки и подготовки используется на этих предприятиях в качестве среды для развития различных микроорганизмов. Последние в результате действия системы ферментов превращают, например, гексозиые сахара в этиловый спирт и углекислоту.
При гидролизе растительного сырья разбавленными кислотами возникают трудности применения единого режима вследствие большой разницы в скоростях гидролиза гемицеллюлоз и целлюлозы. В некоторых случаях эта разница является полезной и на ее основе строятся специальные технологические режимы. Так, при раздельном использовании пентозных и гексозных гидролизатов в микробиологической промышленности реакцию гидролиза растительного сырья, богатого пентозанами, осуществляют последовательно в две ступени. Вначале, применяя мягкий режим гидролиза, в моносахариды превращают большую часть гемицеллюлоз, почти не затрагивая целлюлозу. После удаления пентозного гидролизата остаток, состоящий из целлюлозы и лигнина (целлолигнин), гидролизуется в более жестких условиях.
Аналогичный процесс осуществляется при получении из растительного сырья фурфурола и гексозного гидролизата. Такие процессы можно рассматривать как двухступенчатые.
Ступенчатый метод гидролиза имеет большое значение и для гидролиза целлюлозного остатка. При одноступенчатом гидролизе целлюлозы количество образующегося сахара z изменяется во времени по кривой, проходящей через максимум. Дальнейшее продолжение гидролиза нецелесообразно из-за снижения общего выхода сахара в результате энергично протекающей реакции его разрушения. Однако при максимальном выходе сахара значительная часть целлюлозы еще остается не гидролизованной и теряется для производства. Во избежание этих потерь был предложен многоступенчатый метод гидролиза растительной ткани. Первая ступень гидролиза проводится в мягких условиях, на этой ступени гидролизуются гемицеллюлозы. Затем полученный гидролизат удаляется из гидролизаппарата, а целлолигнин гидролизуется снова в более жестких условиях до момента, отвечающего максимальному выходу сахара. Полученный гидролизат второй ступени также удаляется, а оставшиеся полисахариды снова гидролизуются в аналогичных условиях. Этот процесс продолжается до тех пор, пока все полисахариды, содержащиеся в растительном сырье, будут гидролизованы.
При осуществлении этого способа гидролиза часть гидролизата предыдущей ступени остается в целлолигнине. Чтобы избежать возможной потери Сахаров при повторном гидролизе, после удаления гидролизата из целлолигнина последний промывается разбавленной кислотой и промывные воды присоединяются к основному гидролизату.
Похожие работы
... инновационных технологических решений, способный трансформировать их в конкурентный продукт для конечного использования. 3. Основные направления и перспективы развития технологических процессов прокатного и кузнечнопрессового производства Основные направления деятельности должны формироваться из круга проблем и вопросов, стоящих перед предприятиями и организациями. К ним нужно отнести ...
... сельского хозяйства и предпринимательства. Возрастут объемы инвестирования в интеллектуальный капитал как наиболее эффективный объект размещения ресурсов. Инвестиции в основной капитал в 2010 году по сравнению с 2005 годом увеличатся в 1,65 - 1,75 раза. 3. Наукоемкие отрасли и производства в развитых странах Какие конкретно отрасли промышленности можно отнести сегодня к наукоемким? Как ...
... куриных эмбрионов при культивировании, например, вируса гриппа, некоторые тканевые культуры млекопитающих и т.д., а также органические и неорганические вещества, используемые в биотехнологическом процессе, которые при попадании в окружающую среду могут послужить причиной экологической катастрофы. Поэтому на предприятии должны быть созданы условия для предотвращения хищений подлежащих уничтожению ...
... хозяйства, использования методов биотехнологии и биоинженерии. В этих целях нами совместно с учеными ведущих вузов, НИИ РАСХН и РАН разработан Инновационный проект по биотехнологии в агропромышленном производстве на 2004-2007гг. Этот проект предлагается как межведомственный, финансируемый Минпромнауки РФ и Минсельхозом РФ. Он отражает назревшие экономические и технологические проблемы сельского ...
0 комментариев