Навигация
Расчет материального баланса
13. Расчет материального баланса
2H2S + 3O2 = 2SO2 + 2 H2O
Производительность по газу 1749,8 м3/ч степень превращения H2S = 99.9
| Приход | Расход | |||||||||||
| Mr | кг | % масс | м3 | % об | кмоль | Mr | кг | % масс | м3 | % об | кмоль | |
| 58,00 | 45,31 | 0,23 | 17,50 | 0,12 | 0,78 | SO2 | 64,00 | 4944,48 | 25,64 | 1730,57 | 12,53 | 77,26 |
| 34,00 | 2629,39 | 13,63 | 1732,30 | 11,82 | 77,33 | H2O | 18,00 | 1460,94 | 7,57 | 1818,06 | 13,16 | 81,16 |
| 32,00 | 3870,85 | 20,07 | 2709,59 | 18,49 | 120,96 | N2 | 28,00 | 12741,53 | 66,06 | 10193,23 | 73,79 | 455,05 |
| 28,00 | 12741,53 | 66,06 | 10193,23 | 69,57 | 455,05 | H2S | 34,00 | 2,63 | 0,01 | 1,73 | 0,01 | 0,08 |
| - | 19287,07 | 100,00 | 14652,62 | 100,00 | 654,13 | CO2 | 44,00 | 137,48 | 0,71 | 69,99 | 0,51 | 3,12 |
| ∑ | - | 19287,07 | 100,00 | 13813,58 | 100,00 | 616,68 | ||||||
SО2 + 0,5О2 <=> SО3
Степень превращения SО2 = 98,5
| Приход | Расход | |||||||||||
| Mr | кг | % масс | м3 | % об | кмоль | Mr | кг | % масс | м3 | % об | кмоль | |
| 64,00 | 4944,48 | 46,03 | 1730,57 | 27,70 | 77,26 | SO3 | 80,00 | 6087,90 | 56,67 | 1704,61 | 31,60 | 76,10 |
| 32,00 | 1217,58 | 11,33 | 852,31 | 13,64 | 38,05 | SO2 | 64,00 | 74,17 | 0,69 | 25,96 | 0,48 | 1,16 |
| 28,00 | 4580,42 | 42,64 | 3664,33 | 58,66 | 163,59 | N2 | 28,00 | 4580,42 | 42,64 | 3664,33 | 67,92 | 163,59 |
| - | 10742,48 | 100,00 | 6247,21 | 100,00 | 278,89 | ∑ | - | 10742,48 | 100,00 | 5394,90 | 100,00 | 240,84 |
SO3 + H2O = H2SO4
Степень превращения SO3 = 99,5%
| Приход | Расход | ||||||||||||
| Mr | кг | % масс | м3 | % об | кмоль | Mr | кг | % масс | м3 | % об | кмоль | ||
| SO3 | 80,00 | 6087,90 | 80,90 | 1704,61 | 49,75 | 76,10 | H2SO4 | 98,00 | 7420,39 | 98,61 | 1696,09 | 98,06 | 75,72 |
| H2O | 18,00 | 1362,93 | 18,11 | 1696,09 | 49,50 | 75,72 | SO3 | 90,00 | 30,44 | 0,40 | 7,58 | 0,44 | 0,34 |
| SO2 | 64,00 | 74,17 | 0,99 | 25,96 | 0,76 | 1,16 | SO2 | 64,00 | 74,17 | 0,99 | 25,96 | 1,50 | 1,16 |
| ∑ | 7524,99 | 100,00 | 3426,66 | 100,00 | 152,98 | ∑ | 7524,99 | 100,00 | 1729,62 | 100,00 | 77,22 | ||
Похожие работы
... еще не всегда осуществима. В то же время отходящие газы – наиболее дешевое сырье, низки оптовые цены и на колчедан, наиболее же дорогостоящим сырьем является сера. Следовательно, для того чтобы производство серной кислоты из серы было экономически целесообразно, должна быть разработана схема, в которой стоимость ее переработки будет существенно ниже стоимости переработки колчедана или отходящих ...
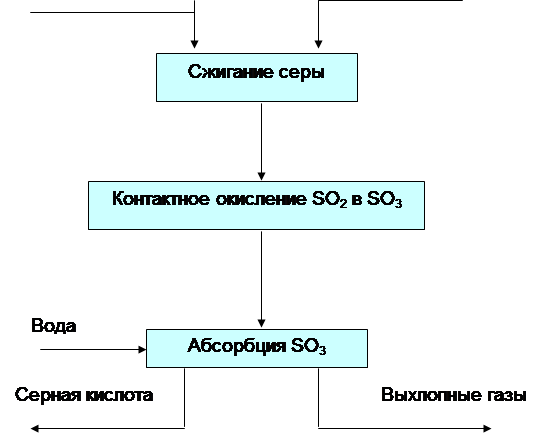
... как температура газов снижается добавкой холодного воздуха между слоями. Абсорбция SO3 производится так же, как и в технологической схеме. Важнейшие тенденции развития производства серной кислоты контактным способом: 1) интенсификация процессов проведением их во взвешенном слое, применением кислорода, производством и переработкой концентрированного газа, применением активных катализаторов; ...
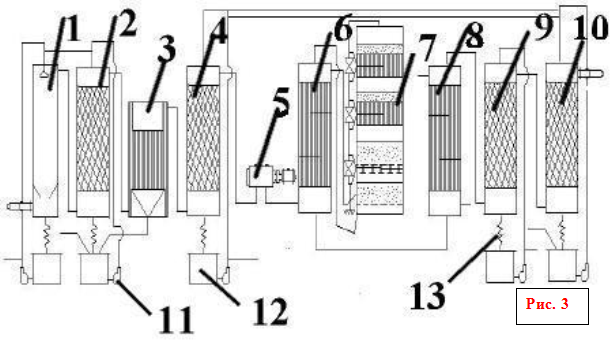
... образуется азотная кислота: NO(HSO4) + H2O®H2SO4 + HNO2 Она - то и окисляет SO2 по уравнению: SO2 + 2HNO2®H2SO4 + 2NO В нижней части башен 1 и 2 накапливается 75% - ная серная кислота, естественно, в большем количестве, чем её было затрачено на приготовление нитрозы (ведь добавляется «новорождённая» серная кислота). Окись азота NO возвращается снова на окисление. Поскольку некоторое количество ...
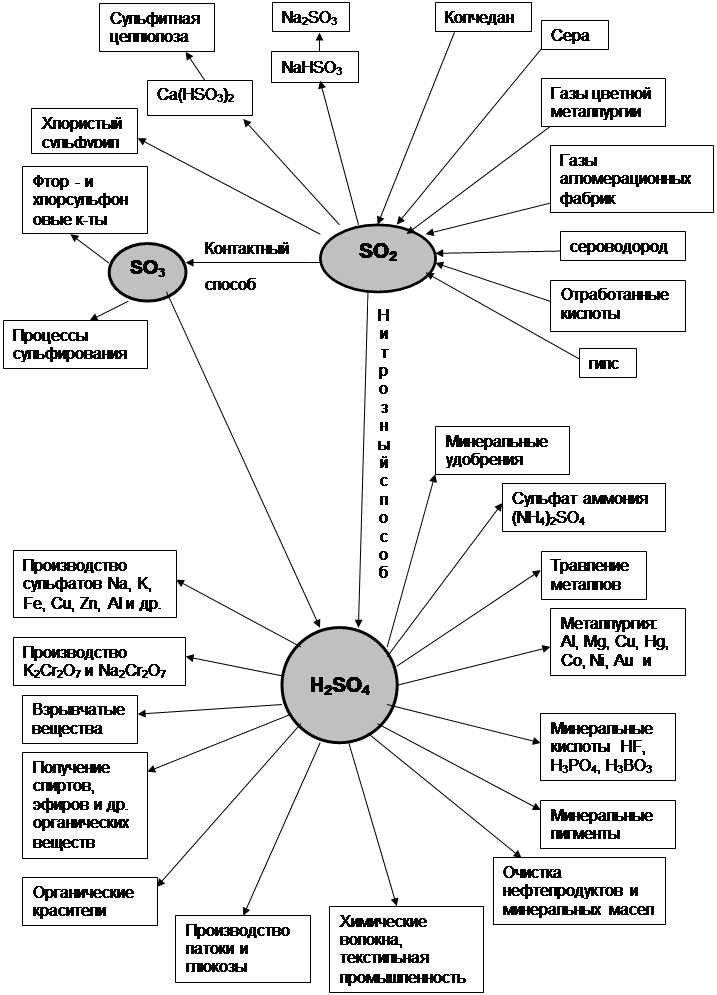
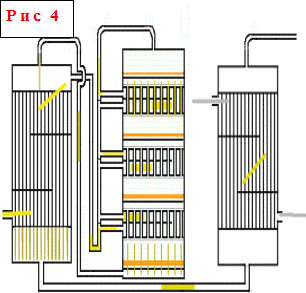
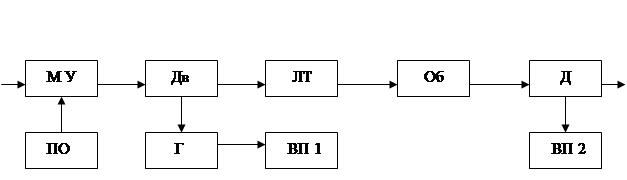
... . Для автоматического регулирования необходимо максимально знать требования, предъявляемые различным химико-технологическим процессом. 1.Основная часть 1.1 Технологический процесс получение серного ангидрида при получении серной кислоты. Производство серной кислоты контактным способом состоит из следующих действий: 1. Разгрузка, складирование и подготовка сырья ...


0 комментариев