Навигация
Количество Fe, находящегося в шлаке в форме FeO
5. Количество Fe, находящегося в шлаке в форме FeO
348,59-62,8=285,8 кг.
Количество FeO в шлаке
(285,8*71,8)/55,8=367,7 кг.
Общее количество О2 необходимое для окисления Fe до FeO
367,7-285,8=81,9 кг.
6. Количество О2, необходимое для окисления S
(246*32)/32,07=245,4 кг.
Всего SO2 в газовой фазе
245,4+230=475,4 кг.
В шлак полностью перейдет полностью из концентрата SiO2 и прочие
Таблица 4 – Состав и количество шлака при плавке без флюсов
| Компонент | Cu | Ni | Fe | S | O2 | SiO2 | Прочие | Итого | ||||||||
| кг. | 13,8 | 1,46 | 285,8 | 3,72 | 81,9 | 5 | 9 | 399,7 | ||||||||
| Компонент | Cu | Ni | Fe | S | O2 | SiO2 | Прочие | Итого | ||||||||
| % | 3,3 | 0,4 | 73 | 1 | 21 | 1 | 0,9 | 100 | ||||||||
плавка взвешенный состояние штейн
Со шлаками такого состава теряется много Cu, поэтому плавку необходимо вести с флюсами. В качестве флюса используется кварцевая руда, %:
SiO2 – 74,8; Fe(в FeO) – 3,8; прочие – 17,8.
Расчет шлака при плавке с флюсом
В качестве исходных данных для состава рационального шлака взято содержание в нем SiO2,равное 30 %, и содержание Fe3O4 равное 14 %.
0,784Х+5=0,3(391,4+Х+Y)
Y=0.0691*0.14(391.4+X+Y)
Y=0.00967*(391,4+X+Y)
Y=3.79+0.00967X+0.00967Y
где, 0,786 – доля SiO2 в песчанике; 5 – масса SiO2 из концентрата;
0,3 – доля SiO2 в шлаке (30 %); 391,4 – масса первичного шлака; 0,0691 – коэффициент пересчета на О2.
Решив уравнение получил
X=256 кг;
Y=6,6 кг.
Приняв пылевынос 4 %, получаем массу песчанника, добавляемого в шихту
256/0,96=266,7 кг.
В 256 кг. Песчанника содержится
256*0,784=200,8 кг.
256*0,038=9,7 кг.
прочие 256*0,178=45,6 кг.
Масса шлака
391,4+256+6,6=654 кг.
Так как в песчанике содержится 9,7 кг. FeO, находим количество Fe, поступившего с флюсом
(9,7*55,8)/71,8=7,5 кг.
С ним связано 2,2 кг. О2
Так как содержание Fe3O4 в шлаке равно 14 %, то масса его составит
(654*14)/100=91,6 кг.
В 91,6 кг. Fe3O4 содержится
Fe – 66,3 кг.
О2 – 91,6-66,3=25,3 кг.
Всего Fe в виде закиси
219,5+7,5=227 кг.
С 227 кг. Fe будет связано О2
(227*16)/55,8=65,1 кг.
Таблица 5 – Количество и состав шлака с учетом флюса
| Компонент | Cu | Ni | Fe | S | O2 | SiO2 | Прочие | Всего |
| Cu2S | 12,8 | – | – | 3,22 | – | – | – | 16 |
| Ni3S2 | – | 1,46 | – | 0,5 | – | – | – | 1,96 |
| FeO | – | – | 227 | – | 65,1 | – | – | 292,1 |
| Fe3O4 | – | – | 66,3 | – | 25,3 | – | – | 91,6 |
| SiO2 | – | –– | – | – | – | 200 | – | 200 |
| Прочие | – | – | – | – | – | – | 9 | 9 |
| Итого | 12,8 | 1,46 | 293,3 | 3,72 | 90,4 | 200 | 9 | 610,7 |
Расчет пыли
1. Количество Cu, перешедшей в пыль
280-278,9=1,1 кг.
2. Количество Ni, перешедшего в пыль
9,96-8,5=1,46 кг.
3. Количество S перешедшей в пыли
349-347,6=1,3 кг.
4. Количество SiO2 перешедшего в пыль
5-4,98=0,02 кг.
из песчаника
200-192=8,02
Всего SiO2 в пыли 8+0,02=8,02 кг.
5. Количество прочих в пыли
из концентрата – 16,3-16,2=0,1 кг.
из песченика – (266,8-256,1)*0,178=1,9 кг.
Всего прочих в пыли
0,1+1,9=2 кг.
6. Количество Fe в пыли
Из концентрата – 349-348,5=0,5 кг.
Из песчаника – (266,8-256,1)*-0,038=0,4 кг. FeO или 0,31 кг. Fe
Всего Fe в пыли
0,315+0,5=0,815 кг.
7. Количество О2 в пыли
0,4-0,3=0,09 кг.
0,09+2,2=2,29 кг.
Таблица 6 – Количество и состав пыли
| Компонент | Cu | Ni | Fe | S | O2 | SiO2 | Прочие | Итого |
| кг. | 1,1 | 1,46 | 0,815 | 1,3 | 2,29 | 8,02 | 1,9 | 16,9 |
| % | 6,5 | 8,6 | 4,8 | 7,7 | 13,5 | 47,4 | 11,2 | 100 |
Расчет количества отходящих газов
Примем, что весь О2, необходимое для окисления реакции поступает с подогретым дутьем.
1) Количество О2, необхождимое для окисления Fe до FeO, составляет 90,4 кг.
2) Для окисления Fe до Fe3O4 необходимо О2
5,5+25,3=30,8 кг.
3) Для окисления S требуется 245,4 кг. О2
Общий расход на плавку О2, составит 366,6 кг.
Вместе с О2 в печь поступит N2 при содержании О2 в дутье 24,6 %:
366,6/0,246*0,754=1123,6 кг.
При содержании в концентрате влаги 0,1 % в печь поступит её
(1000+266,8)/0,999-(1000+266,8)=1,268 кг.
Таблица 7 – Количество и состав отходящих газов
| Газы | кг. | м3 | %(объемные) |
| SO2 | 475,4 | 165,9 | 15,9 |
| N2 | 1123,6 | 876,5 | 84 |
| H2O | 1,268 | 1,577 | 0,15 |
| Итого | 1600 | 1043,97 | 100 |
Таблица 8 – Материальный баланс плавки сульфидного медного концентрата на подогретом воздушном дутье, кг
| Поступило | ||||||||||
| Материал баланса | Всего | В том числе | ||||||||
| Cu | Ni | Fe | S | SiO2 | O2 | N2 | Прочие | H2O | ||
| Загружено концентрата | 1001,3 | 278,9 | 9,96 | 348,59 | 347,6 | 4,98 | – | – | 9 | 1,3 |
| Песчаника | 260,6 | – | – | 7,8 | – | 203 | 2,26 | – | 47,5 | – |
| Воздуха | 1490 | – | – | – | – | – | 366,6 | 1164 | – | –– |
| Итого | 2752 | 279 | 9,96 | 356,4 | 347,6 | 208 | 368,9 | 1164 | 56,5 | 1,3 |
| Получено | ||||||||||
| Всего | Cu | Ni | Fe | S | SiO2 | O2 | N2 | Прочие | H2O | |
| Штейна | 441 | 265,4 | 7,5 | 62,8 | 97,9 | – | 5,5 | – | – | – |
| Шлака | 610,7 | 12,3 | 1,46 | 292,5 | 3,7 | 200 | 90,4 | – | 54,6 | – |
| Пыли | 16,9 | 1,1 | 1 | 0,8 | 1,3 | 8 | – | – | 1,9 | – |
| Газов | 1683 | – | – | – | 244,7 | – | 273 | 1164 | – | 1,3 |
| Итого | 2752 | 279 | 9,96 | 356,4 | 347,6 | 208 | 368,9 | 1164 | 56,5 | 1,3 |
Степень десульфаризации
(244,7/347,6)*100=70 %
Расчет теплового быланса плавки
Приход тепла
Окисление сульфидов железа
Количество Fe, окисляемого до FeO, равно
219,5+1,4=220,9 кг.
По реакции:
2FeS + 3O2=2Fe + 2SO2 + 470786 кДж
Всего выделится тепла
(470786*220,9)/(2*55,8)=122789 кДж
Количество Fe, окисленного до Fe3O4 составляет
14,3+66,3=80,6 кг.
По реакции:
3FeS + 5O2=Fe3О4 + 3SO2 + 172537 кДж
Выделится тепла
1723537/(3*55,85)*80,6=855500 кДж
Всего при окислении FeS выделится тепла
122789+855500=977689 кДж
Окисление серы
Всего в газы переходит 244,7 кг., в том числе
от окисления FeS до FeO
244,7*32*55,8=140,3 кг.
От окисления FeS до Fe3O4
83.117*32/55,8=47,7
Количество S от диссациации составляет
244,7-47,7-140,3=56,7 кг.
Количество тепла выделяющегося при окислении S по реакции
S + O2= SO2 + 297086 кДж
47,7*2212=105512 кДж
Ошлакование закиси железа
Тепло от ошлакования FeO по реакции
2FeO = SiO2 = 2FeO*SiO2 = 29309 кДж
Всего тепла от ошлакования FeO выделится
(29309*244,4)/(2*55,8)=65119 кДж
Ошлакование CaO
Тепло от ошлакования CaO определим по реакции
CaO + SiO2 = CaO*SiO2 + 90020 кДж
На ошлакование 1 кг. CaO выделится тепла
21500/56=1605 кДж
В песчанике содержится 3 % СaO или 7,684 кг.
Всего тепла от ошлакования СаО выделится
1605*7,684=12333 кДж
Таким образом, от экзотермических реакциё поступит тепла
977689 + 105513 + 65119 + 12333 = 1160653 кДж
Физическое тепло
Твердая шихта поступает в печь взвешенной плавки предварительно подсушенной в распылительных сушилках. На выходе в печь температура шихты 25 0С. Физическое тепло шихты при 25 0С составит
4,187*1268*0,22*25=29202 кДж
а весь приход тепла составлит
1160653 + 29202 = 1189855 кДж
Расход тепла
1) Весь расход тепла на диссациацию 1 моля серы равен 83,7 кДж, получим расход на образование 47,3 серы равен
(47,3/32)*83,7=123,642 кДж
Количество тепла затрачиваемого на разложение 1 моля СаСО3 равное 177947 кДж
Расход тепла на разложение СаСО3 равен
177947*7,68/56,1=24382 кДж
Всего расход тепла на эндотермические реакции составит
1236+24382=24505,6 кДж
2) Расход тепла с продуктами плавки
При нормально ведении процесса температура продуктов плавки, то есть штейна, шлака и отходящих газов, составит соответственно 1180 0С, 1250 0С, 1300 0С. При этом расход тепла с продуктами плавки составит, кДж
со штейнами – 4,184*441*0,22*1180=478999 кДж
со шлаками – 4,184*610,7*0,29*1250=926249 кДж
с пылью – 4,184*16,9*0,836*1300=76847 кДж
с SO2 – 4,184*475,4*715,3=1422784 кДж
c N2 – 4,184*1123,6*444,9=2091538 кДж
с НО2 – 4,184*1,5=6,3 кДж
Всего – 13332423 кДж
Потери через кладку и неплотноси в печи составляют 4,5% от общего расхода тепла. Тогда общий расход тепла составит
13332423/0,95=14034129 кДж
Теплосодержание 1м3 воздуха подогретого до 200 0С равно 261,9 кДж/м3
Тогда с воздухом вводится тепла
261,9*1334,76=34574 кДж
Дефицит тепла составит
14034129-34574-2395803=11603752 кДж
Это тепло необходимо подать в печь путем сжигания природного газа
Природный газ имеет состав(по объему), %: СН4 – 98; СО2 – 1,2; N2 – 0,8.
Для подсчета теплоты сгорания используем формулу
QHP=(85,89*СН4)*4,184=4,184*(85,89*98,7)=35469 кДж/м3
Принимаем коэффициент избытка воздухадля сжигания топлива α=1,1
Определим теоретическую потребность воздуха по реакции
СН4 + 2О2 → СО2 + 2Н2О
Потребность О2 на 100 м3 природного газа составляет, м3
для сгорания СН4 – 100*0,987*2=197,4
Всего потребуется 199,775 м3 О2
С учетом α=1,1, всего потребуется О2
199,775*1,1=219,753 м3
Теоретический состав газов от сжигания топлива следующий, м3
СО2 – 0,6+0,987*100+0,00675*100*2=100,65
Р2О – 0,987*100*2+0,00675*100*3+0,0025*100=199,45
N2 – 673,55
Расход газа для восполнения потерь составим Х м3.
Для сжигания газа при α=1,1 на 1м3 газа потребуется воздуха 8,933 м3
Температура воздуха, подаваемого на сжигание Х м3 газа равна 30 0С, а его теплоемкость 1,3 кДж/м3*0Сследовательно, тепло, вносимое воздухом, будет
Х*8,933*301,3=Х*348,4 кДж
Тепло от сжигания газа равно Х*8584,238
С отходящими газами при 1300 0С расход тепла, кДж
с СО2 – 1,0065*Х*2992,4=3012*Х
с Н2О – 1,9945*Х*2327=4641*Х
с N2 – 6,671*Х*1863=12428*Х
с О2 – 0,195*Х*1970=384*Х
Всего – 20465*Х
По приходу и расходу тепла от сжигания природного газа составляет уравнение
348,4Х+35941Х-20465Х=11603752
Х=6733 м3
Таким образом количество природного газа, необходимое для поддержания теплового баланса плавки во взвешенном состоянии на 1000 кг концентрата равно 62,2 м3.
СПИСОК ИСПОЛЬЗУЕМЫХ ИСТОЧНИКОВ
1. Металлургия тяжелых цветных металлов [Электронный ресурс]; электронный учебное пособие. Н.В. Марченко, Е.П. Вершинина, Э.М. Гильбенбрандт. Красноярск ИПК СФУ, 2009.
2. Металлургия меди, никеля и сопутствующих элементов. Б.П. Бледнов, В.Е. Дульнева. Красноярск, 1983 – 104 с.
Похожие работы
... с 1350°С до 550°С, а затем после очистки в электрофильтрах от пыли, поступают в серный цех для улавливания из газов элементарной серы. Печь взвешенной плавки является головным агрегатом в цепи переработки серосульфидных концентратов. Агрегат обладает высокой интенсивностью плавления. В связи с этим печь имеет сложную и многообразную систему охлаждения. Агрегат должен обладать высокой ...
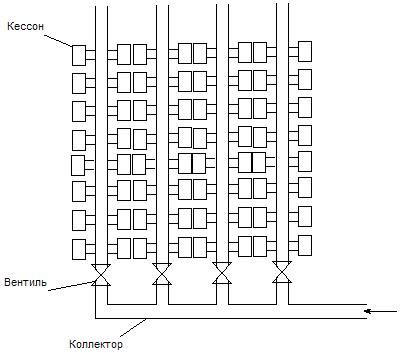
... – либо детали и понижения давления на коллекторе предусматривается сигнализация (световая, звуковая).[1] 2. Модель расчета В данном разделе представлен план выполнения расчетов для системы охлаждения кессонов реакционной шахты печи взвешенной плавки. Данная модель будет использоваться в следующем разделе. 1) Расчет начинаем с общих параметров системы охлаждения: числа кессонов в ряду, длин ...
... индукционных плавильных печей преимущественно в литейных цехах. Кроме того, высокая стоимость высокочастотных питающих преобразователей сдерживает применение высокочастотных плавильных печей. Конструкция и схема питания индукционной печи существенно зависят от наличия или отсутствия железного сердечника. Поэтому индукционные печи рассматриваются далее в соответствии с этим признаком. 2.2 Печи ...
... тем, что часть электрического тока расходуется на побочные электрохимические процессы и утечку тока. Степень использования тока на основной электрохимический процесс называется выходом металла по току. В практике электрометаллургии цветных металлов в большинстве случаев приходится иметь дело с катодным выходом по току, так как масса катодного осадка определяет конечный выход товарной продукции ...
0 комментариев