Навигация
Редкоземельные металлы и их полуторные оксиды
Федеральное агентство по образованию Российской Федерации
Государственное образовательное учреждение высшего профессионального образования
«Ярославский государственный университет им. П. Г. Демидова»
Кафедра общей и экспериментальной физики
Курсовая работа
Редкоземельные металлы и их полуторные оксиды
Научный руководитель
Доцент кафедры
Балабаева Р.Ф.
Студент группы Ф-51В
Туркина А.Н.
Ярославль 2009 г.
ОГЛАВЛЕНИЕ
1. Введение
2. Редкоземельные элементы
2.1 Европий
3. Влияние условий получения полуторных оксидов РЗЭ на их кристаллическое строение
3.1 Окисление металлов
4. Фазовые превращения полуторных оксидов РЗЭ
4.1 Необратимые или медленно протекающие фазовые превращения
4.2 Обратимые полиморфные превращения
4.3 Влияние давления на полиморфизм оксидов
5. Простые оксиды европия
6. Устойчивость полуторных оксидов РЗЭ
7. Стабилизация метастабильных форм полуторных оксидов РЗЭ
8. Заключение
9. Список литературы
1. ВВЕДЕНИЕ
Редкоземельные элементы (в минералогии — TR, от лат. terra rará), химические элементы побочной подгруппы III группы периодической системы Менделеева: скандий Sc (атомный номер Z = 21), иттрий Y (Z = 39), лантан La (Z = 57) и лантаноиды (14 элементов, Z от 58 до 71). Sc, однако, не всегда относят к редкоземельным элементам. В свободном виде — металлы. Название «редкоземельные» дано в связи с тем, что они, во-первых, сравнительно редко встречаются в земной коре и, во-вторых, образуют тугоплавкие, практически не растворимые в воде оксиды (такие оксиды в начале 19 в. и ранее назывались «землями»). Важная особенность редкоземельных элементов — их совместное нахождение в природе. Например, минерал монацит — один из основных источников этих элементов — содержит фосфаты Y, La и др. Подразделяются на иттриевую (Y, La, Gd-Lu) и цериевую (Се-Eu) подгруппы. Элементы Се-Eu называют легкими, a Cd-Lu-тяжелыми лантаноидами.
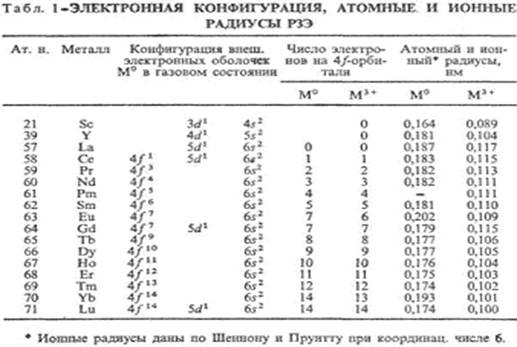
Электронная структура, лантаноидное сжатие, электронная конфигурация РЗЭ дана в табл. 1, у ионов М3+(М = Sc, Y, La) устойчивая конфигурация инертных газов. У Sc, Y и La в образовании химической связи участвуют d- и s-электроны, у других РЗЭ могут участвовать также f-электроны, однако близкие химические свойства РЗЭ определяются главным образом внешними d-и s-электронами. Поэтому эти элементы объединены в одну группу.
В состоянии М3+ РЗЭ имеют оболочку с 4f n-электронами (кроме Sc), в газовом состоянии-4f n+16s2 (кроме La, Ce, Gd и Lu, имеющих оболочку 4f n), в металлическом М°-4f n(для Еu и Yb-4f n + 1). Предполагается, что вакантная, заполненная наполовину и заполненная полностью f-оболочки обладают повышенной устойчивостью. Поэтому Sc, Y, La, Gd и Lu образуют только ионы М3+, для Се и Тb устойчиво также состояние М4+, а для Еu и Yb-также М2+ . Помимо электронной структуры на устойчивость валентных состояний РЗЭ влияют и другие факторы: например, ионы Sm+, Tm+ (конфигурации f 7 и f 14), Рr5+ (f 0), Dy5+ (f 7) крайне неустойчивы.
2. Редкоземельные элементы
РЗЭ-элементы - металлы серебристо-белого цвета, некоторые с желтоватым оттенком (Рr, Nd). Они пластичны и электропроводны, легко поддаются механической обработке. Многие свойства простых веществ и соединений изменяются симбатно в рядах La-Eu и Gd-Yb. Особенно резко отличаются свойства, отражающие переход из связанного состояния в свободное и обратно.
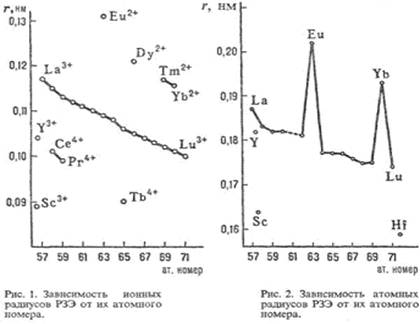
Например, при переходе из металлического состояния в парообразное мерой является давление пара металлов. При 25 °С давления паров РЗЭ различаются более чем на 40 порядков, а при 1000 °С - примерно на 10 порядков (минимальное давление характерно для La, Gd и Lu, максимальное - для Еu и Yb). Это связано с большой разницей в энергии, необходимой для перехода 4 d -электрона на 5d-уровень. С другой стороны, есть свойства, остающиеся примерно постоянными для всех РЗЭ. Вследствие лантаноидного сжатия при переходе от La к Lu ионные радиусы РЗЭ и их атомные радиусы (кроме Еu и Yb) плавно уменьшаются (рис. 1, 2), плотность простых веществ увеличивается [31].
2.1 Европий
Европий - это химический элемент, находящийся в третей группе периодической системы Менделеева и относящийся к лантаноидам. Его атомный номер 63, атомная масса 151.96. Мягкий металл, серебристо-белого цвета, плотностью 5.2456 г/см3, температура плавления = 8260С. По твердости европий очень похож на свинец- такой же мягкий и пластичный.
Европий - самый легкий из лантаноидов, и самый неустойчивый среди редкоземельных элементов - в присутствии кислорода воздуха и влаги быстро окисляется (корродирует).
В природе европий - малораспространенный элемент, даже среди редкоземельных элементов европий - один из самых редких, а потому и наиболее дорогих. В свободном виде не встречается, входит в состав таких минералов, как монацит (обезвоженный фосфат редкоземельных элементов цериевой группы - (Ce,La,Y,Th)PO4), бастнезит и других содержащих редкоземельные элементы минералов. В природные воды европий попадает в районах залегания пород, содержащих редкоземельные элементы, в результате его реакции с водой.
редкоземельный элемент металл европий оксид
Похожие работы
... MnY2S4 и фазы MgLn4S7 моноклинной сингонии. Условие существования фаз, характер плавления не известны. Ограниченность и неполнота литературных данных определяет актуальность задачи изучения фазовых равновесий в системе MgS – Y2S3. Глава 2. Методическая часть. 2.1. Методы физико-химического анализа Исходя из свойств полуторных сульфидов, таких, как термическая стабильность, летучесть, и ...
... (tпл. GdCl3 = 610˚C), остывший трихлорид хранили в герметически закрытых ампулах. Все операции с солью проводились в сухом боксе. Глава Ш. Исследование совместного электровосстановления гадолиния и алюминия в галогенидных расплавах. Из анализа литературных данных следует, что процесс электровосстановления алюминия из хлоридных и фторидных расплавов изучался в основном на платиновом ...
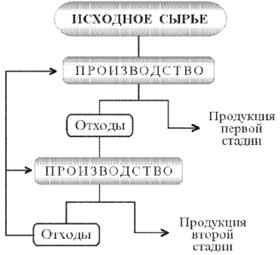
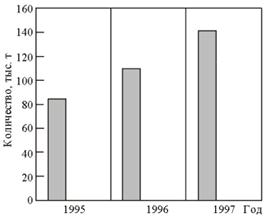
... отходам производства. В докладе «О состоянии окружающей природной среды Российской Федерации в 1997 году» Государственного комитета Российской Федерации по охране окружающей среды отмечается, что на начало 1997 г. на предприятиях различных отраслей промышленности накоплено 1431,7 млн. т токсичных отходов. За 1997 г. на промышленных предприятиях РФ образовалось 89,4 млн т токсичных отходов, из ...
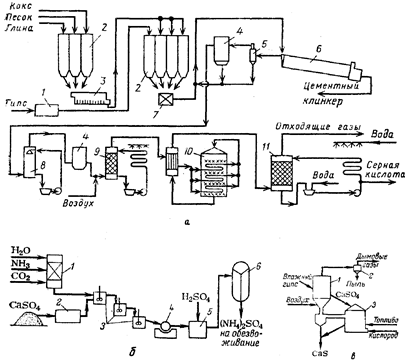
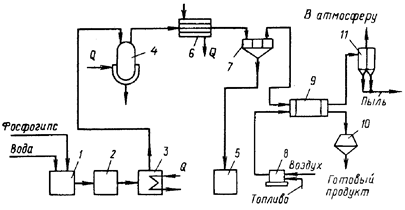
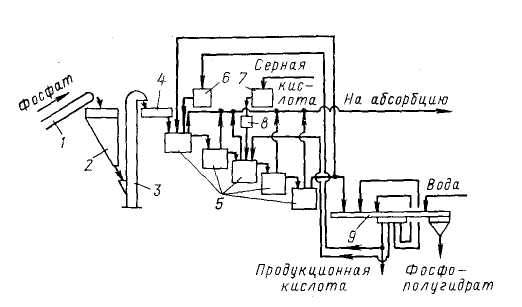
... отходы образуются в процессе переработки нефти в виде кислых гудронов, нефтяных шламов, отработанных масел и др. ГЛАВА 3. ИЗВЛЕЧЕНИЕ КРЕМНЕФТОРИСТОВОДОРОДНОЙ КИСЛОТЫ ИЗ ПРОЦЕССА ПРОИЗВОДСТВА ФОСФОРНОЙ КИСЛОТЫ В процессе производства концентрированных фосфатных удобрений фосфорсодержащая руда подвергается экстракции раствором серной кислоты. Полученная разбавленная фосфорная кислота ...
0 комментариев