Навигация
Аппараты для проведения процесса нитрования бензола
2.3. Аппараты для проведения процесса нитрования бензола
В приложении 1 показана в сокращённом виде схема одной из установок для жидкофазного нитрования бензола в аппаратах с мешалками.
Четыре нитратора показаны в данной схеме условно. Проведение процесса нитрования в несколько стадий значительно экономит расход кислот, так как для введения первой нитрогруппы в ароматическое ядро можно использовать менее концентрированную кислоту, чем это требуется для введения второй нитрогруппы; для введения второй нитрогруппы требуется менее концентрированная смесь кислот, чем для введения третьей нитрогруппы, и т.д.
Исходный бензол подают в нитратор 1. Туда же поступает частично отработанная смесь кислот из сепаратора 5. Смесь углеводорода и кислоты эмульгируется при помощи мешалки и проходит в нитратор 2. Оттуда частично пронитрованный углеводород вместе с отработанной кислотной смесью попадает в сепаратор 3. Здесь эмульсия расслаивается, отработанная кислота отводится из сепаратора снизу, а органическая фаза непрерывно перетекает в нитратор 4. В тот же аппарат поступает частично отработанная кислотная смесь из сепаратора 7. Нитрование завершают в реакторе 6, куда подают свежую нитрующую смесь.
Отделенный в сепараторе 7 нитропродукт подвергается промывке в аппаратах 8 и 12 холодной и тёплой водой и в аппарате 10 – раствором соды для нейтрализации остатков кислот.
Другая принципиальная схема установки для нитрования бензола приведена в приложении 2. Все аппараты представляют собой один агрегат. Нитрующие камеры установлены друг над другом, а между ними расположены сепарационные камеры, представляющие собой центрифуги. От электродвигателя редуктора, расположенных в верхней части агрегата, через всю его высоту проходит вал, на который насажаны пропеллерные мешалки барабаны центрифуг разделение органической и кислотной фаз осуществляется благодаря разности их удельных весов: более тяжёлая кислотная фаза опускается в нижнюю часть реактора, а органическая фаза поднимается вверх.
Показатели работы установок обоих типов примерно одинаковы: преимуществом установки, которая изображена на схеме 2, является меньшая производственная площадь.
Для нитрования 1 т бензола готовят нитрующую смесь из 63% азотной кислоты и 96 % серной, при этом образуется около 3,5 т отработанной 75 % серной кислоты. Часть ее используют для приготовления нитрующей смеси из меланжа и 18-20 % олеума. Однако и в этом случае остается неизрасходованной около 1,2 т отработанной кислоты, не находящей сбыта, что является серьезной экологической проблемой. Экономически целесообразно совмещение производств нитробензола и серной кислоты на одном предприятии.
Полученный нитробензол промывают водой и содой для удаления растворенной кислоты и примесей нитрофенолов. Затем перегоняют в вакууме для отделения от примесей динитробензола, который опасен при парофазном гидрировании при получении анилина, так как это взрывоопасное соединение накапливается в испарителе.
2.4. Техника безопасности при производстве нитробензола.
Предельно-допустимая концентрация (ПДК) для нитробензола составляет 5 10-6 г/л воздуха. При проведении реакции нитрования следует соблюдать следующие правила: герметизация аппаратуры; поглощение оксидов азота NaOH; хорошая вентиляция. Работать в специальной чистой одежде, после работы тщательно мыть руки, принять теплый (но не горячий!) душ. При попадании ароматических нитросоединений на одежду необходимо немедленно ее снять и отдать в стирку; при попадании на кожу – вымыть с мылом теплой водой или спиртом; при попадании на аппаратуру – смыть сильной струей холодной воды с моющим порошком. Признаки отравления – посинение губ, носа, ушей и кончиков пальцев, головокружение, головная боль, тошнота. Пострадавшего необходимо вывести на свежий воздух, не давать спать и не принимать молоко, так как нитросоединения жирорастворимые.
Но главное - это не допустить пожара и взрыва, так как все факторы поражения будут задействованы. Детонация, удары, искра, пожар – факторы риска.
Кроме того, необходимо знать, что: конц. азотная кислота при контакте с органическими веществами может вызвать пожар. Все ремонтные работы с использованием сварки или открытого пламени аппаратуры и трубопроводов можно проводить только после тщательной продувки их азотом.
2.5. Экология
Основной экологической проблемой получения нитробензола, является большое кол-во отработанной серной кислоты, которая не находит сбыта. Поэтому ведутся поиски способов уменьшения отходов кислот при нитровании. Один из них – проведение процесса в легко регенерируемых средах: в концентрированной азотной кислоте и в низкокипящих органических растворителях. К недостаткам концентрированной азотной кислоты как среды относятся её окислительные свойства, коррозионная активность и повышенная опасность. В органических растворителях азотная кислота является более слабым нитрующим реагентом, чем в серной кислоте. Радикальный путь – замена серной кислоты твёрдым сильнокислым катализатором, нерастворимым в условиях нитрования. Для этой цели используют, например, суперкислые перфторалкансульфокислоты и смолы на их основе. Интенсивно разрабатываются процессы нитрования в газовой фазе. На данный момент разработан процесс с азеотропной отгонкой воды. Бензол и вода дают азеотропную смесь. Используют большое количество бензола, при температуре 120 0С происходит отгонка бензола, воды и азотной кислоты, серная кислота не разбавляется. Однако качество полученного нитробензола ниже. Имеются патентные данные (ФРГ) о нитровании бензола 65% азотной кислотой, в этом процессе также отсутствует проблема с отработанной серной кислотой.
Образующиеся оксиды азота необходимо улавливать. При малотоннажном производстве их можно поглощать щелочью. При многотоннажном сжигать в токе природного газа:
CH4 + 2NO2 → CO2 + N2 +2 H2O
Однако трудными экологическими проблемами является обезвреживание промывных вод и щелочных растворов от нитросоединений, а также разбавленных кислых стоков.
2.6. Разработка новых технологий нитрования
В настоящее время продолжаются интенсивные разработки новых технологических решений процесса нитрования. В основном это направления снижение острого взрывоопасного начала реакции, снижение концентрации нитросоединений и кислых отходов в сточных водах. Возможность варьирования нитрующих реагентов, сред, катализаторов, способов выделения даёт простор для поиска оптимальных технологических режимов.
В настоящее время изучено нитрование бензола 65 %-ной азотной кислотой на вольфрам-циркониевых катализаторах, некоторых цеолитах и Al-бентоните. Показано, что выход нитробензола существенно зависит от условий проведения процесса. Наибольшую активность в нитровании проявляют WO3/ZrO2 и Al-бентонит, обладающие сильными кислотными свойствами. Выход нитробензола на WO3/ZrO2 достигает 70 % при селективности, близкой к 100 %.
Заключение
Нитрование – сложный, опасный, экологически напряженный процесс, но без него невозможен синтез ряда продуктов. Перспективы использования нитрования в новых технологических решениях – снижение острого взрывоопасного начала реакции, снижение концентрации нитросоединений и кислых отходов в сточных водах. В наше время эти проблемы стали более острее, так как из-за развития производств некоторых продуктов, сырьём для которых являются продукты нитрования, требования к количеству и качеству нитроароматики возрастают.
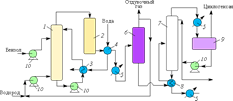
Приложение 1.
Процесс жидкофазного нитрования ароматических углеводородов
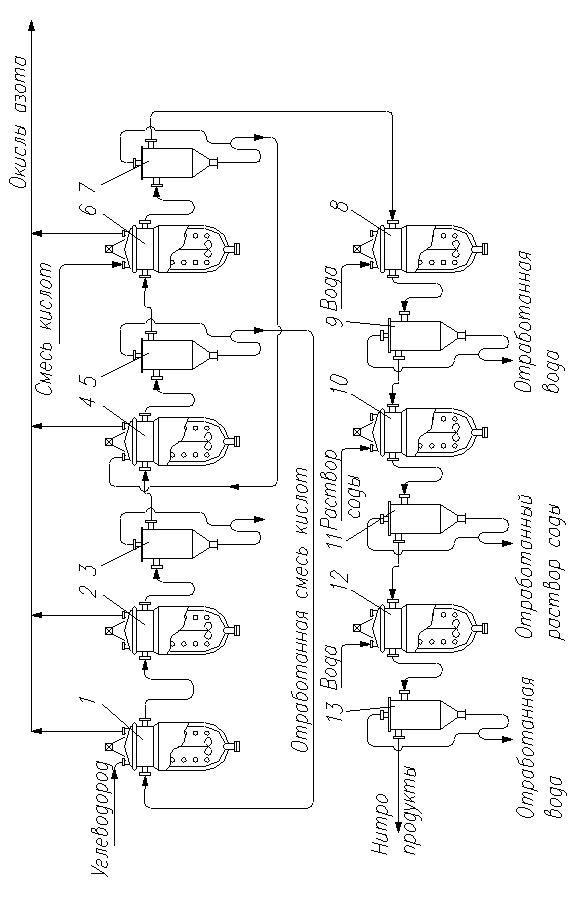
1,2,4,6 – нитраторы; 3,5,7,9,11,13 – сепараторы; 8,10,12 – промывные ёмкости
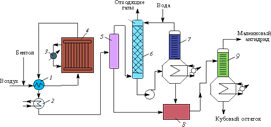
Приложение 2.
Установка для нитрования ароматических углеводородов в проточном нитраторе
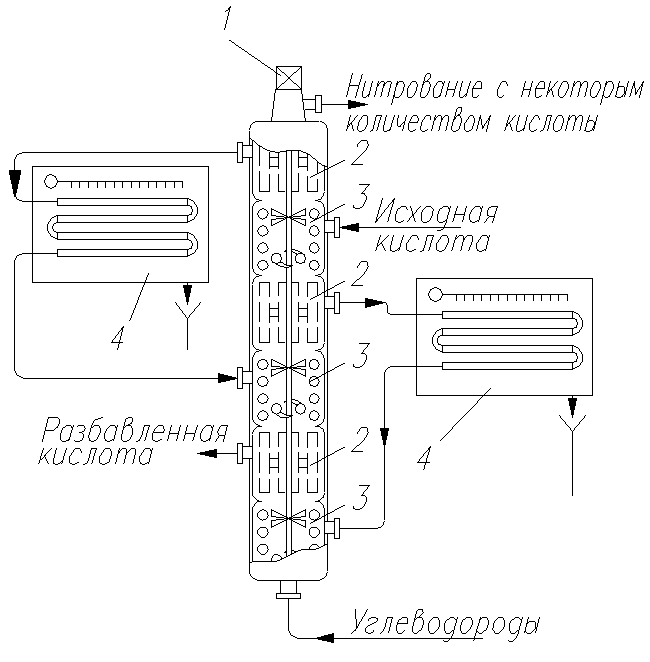
1 – мотор; 2 – сепарационные камеры; 3 – камеры нитрования; 4 – холодильники.
Список литературы
1. Лебедев Н.Н. Химия и технология основного органического и нефтехимического синтеза. М.: Химия, 1969. 670 с.
2. Адельсон С.В. и др. Технология нефтехимического синтеза. М.: Химия, 1985. 607 с.
3. Горелик М.В., Эффос Л.С. Основы химии и технологии ароматических соединений. М: Химия, 1992. 640 с.
4. Чичибабин А.Е. Основные начала органической химии. М.: Государственное научно-техническое изд-во химической литературы, 1963. т.1 545 с.
5. Грейш А.А., Демыгин С.С., Кустов Л.М. Нанесенные вольфрам-циркониевые и цеолитные катализаторы // Катализ в промышленности, 2002, № 4 с. 17
6. Чичибабин А.Е. Основные начала органической химии. М.: Государственное научно-техническое изд-во химической литературы, 1957. т.2 614 с.
Похожие работы
... ) В ряду ароматических углеводородов часто применяют тривиальные названия, например, метилбензол иначе называют толуолом. По международной номенклатуре (правила ИЮПАК) все ароматические углеводороды объединяют названием – арены. Соответственно, их одновалентные остатки, образованные отнятием водорода от углеродных атомов ядра (одновалентные ароматические радикалы), называют арилами и обозначают - ...
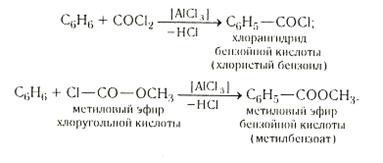
... продуктов. Сложные эфиры Б. к. (от метилового до амилового), обладающие сильным запахом, применяют в парфюмерной промышленности. Различные производные Б. к., например хлор- и нитробензойные кислоты, широко применяют для синтеза красителей. Эталон в калориметрии; основное вещество для установки титра щелочей; для бензилирования в органическом анализе; растворитель при определении молекулярного ...
... в реакторе регулируется за счет испарения циклогексана. Гидрирование проводится при 200 °С и давлении 4 МПа (парциальное давление водорода ~0,3 МПа). Рис. 3. Технологическая схема процесса производства циклогексана: 1 — основной реактор гидрирования; 2 — вспомогательный реактор гидрирования; 3 — 5, 8 — теплообменники; 6 — сепаратор высокого давления; 7 — колонна стабилизации; 9 — сепаратор; ...
... нитрования с участием нитроний-катиона NO+2 представляет собой замещение водорода: 2. Нитросоединения с нитрогруппой в боковой цепи получают теми же методами, что и нитросоединения алифатического ряда: 1. Нитрование гомологов бензола разбавленной азотной кислотой (реакция Коновалова). Ar-CH3 + HONO2 ® Ar-CH2NO2 + H2O Реакция галогенпроизводных с галогеном в боковой цепи с нитритом ...


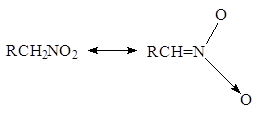
0 комментариев