Навигация
Добыча и получение солей меди из природных месторождений
7. Добыча и получение солей меди из природных месторождений.
Около 15% всех руд меди перерабатывается гидрометаллургическим методом – на измельченную руду действуют растворителем, который переводит медь в раствор. На руды, содержащие оксид меди, действуют разбавленной серной кислотой: ![]()
По сравнению со многими другими оксидами, встречающимися в руде, оксид меди растворяется сравнительно хорошо. Выделение металлической меди из раствора проводят электролизом.
Если медь находится в руде в виде сульфида, то ее в раствор можно перевести, обрабатывая ее руду раствором сульфата железа:
![]() [1, с.64]
[1, с.64]
8. Медь и живые организмы.
Медь входит в число жизненно важных микроэлементов. Она участвует в процессе фотосинтеза и усвоении растениями азота, способствует синтезу сахара, белков, крахмала, витаминов и ферментов. При отсутствии или недостатке меди в растительных тканях уменьшается содержание хлорофилла, листья желтеют, растение перестает плодоносить и может погибнуть. Чаще всего медь вносят в почву в виде пятиводного сульфата – медного купороса CuSO4*5H2O. В значительных количествах он ядовит, как и многие другие соединения меди, особенно для низших организмов. Польские ученые установили, что в тех водоемах, где присутствует медь, карпы отличаются крупными габаритами. В прудах и озерах, где нет меди, быстро развивается грибок, который поражает карпов. В малых же дозах медь совершенно необходима всему живому.
Из представителей живого мира небольшие количества меди содержат осьминоги, каракатицы, устрицы и некоторые другие моллюски. В крови ракообразных и головоногих, медь входящая в состав их дыхательного пигмента – гемоциана (0,33-0,38%), – играет ту же роль, что железо в крови других животных. Соединяясь с кислородом воздуха, гемоцианин синеет (поэтому у улиток кровь голубая), а отдавая кислород тканям, – обесцвечивается. У животных, стоящих на более высокой ступени развития, и у человека медь содержится главным образом в печени. Ежедневная потребность человеческого организма – примерно 0,005 грамма этого элемента. При недостаточном поступлении меди с пищей у человека развивается малокровие, появляется слабость.
С биологическими процессами связан и один из способов добычи меди. Еще в начале XX века в Америке были зарыты медные рудники в штате Юта: решив, что запасы руды уже исчерпаны, хозяева рудников затопили их водой. Когда спустя два года воду откачали, в ней оказалось 12 тысяч тонн меди. Подобный случай произошел и в Мексике, где из заброшенных рудников, на который махнули рукой, только за один год было “вычерпано” 10 тысяч тонн меди. Оказалось, что среди многочисленных видов бактерий есть и такие, для которых любимым лакомством служат сернистые соединения некоторых металлов. Поскольку медь в природе связана именно с серой, эти микробы неравнодушны к медным рудам. Окисляя нерастворимые в воде сульфиды, микробы превращают их в легко растворимые соединения, причем процесс этот протекает очень быстро. Так при обычном окислении за 24 дня из халькопирита выщелачивается 5% меди, то в опытах с участием бактерий за 4 дня удалось извлечь 80% этого элемента.
9. Применение меди.
История применения меди.
Археологические находки указывают, что медь довольно широко использовалась людьми для изготовления украшений и предметов быта около 7-8 тысяч лет назад.
До недавнего времени считалось, что история эры электричества началась с 1786 года после опытов Луиджи Гальвани. В то же время археологические раскопки говорят, что с электричеством люди ознакомились много веков назад. Археологи неподалеку от Багдада, а затем на берегах Тигра нашли глиняные сосуды высотой около 10 см и покрытые глазурью. Внутри сосуда обнаружили медные цилиндры, в которые были вставлены железные стержни. В сосудах имелось небольшое количество битума. Медные цилиндры были сильно разъедены. Это был первый гальванический элемент. Подозревают, что эти элементы использовались для электрохимического способа позолочения серебряных изделий.
Медь наряду с железом и золотом издавна применялась в качестве платежного средства.
Большого совершенства в изготовлении различных изделий из меди и бронзы достигли русские мастера. Уже к концу XV века в России в широких масштабах изготовлялись бронзовые пушки. [4, с.115-118]
Применение меди в настоящее время.
Примерно половина производимой меди в настоящее время используется в радиотехнике и электротехнической промышленности. Это связано с ее хорошей проводимостью и относительно высокой коррозионной стойкостью. К меди, идущей на изготовление электрических проводов, часто добавляют в небольшом количестве кадмий, который не снижает электропроводимость меди, но повышает ее прочность на разрыв.
Древнейший сплав меди с цинком – латунь и в настоящее время производится в больших количествах. Содержание цинка в латуни составляет 30-45%. Она применяется для изготовления различной арматуры, соприкасающейся с водой (краны, вентили и т.д.), а также для производства различных труб. Из латуни прокатывают полосы и листы, идущие для выработки самых разнообразных изделий (проволока, произведения искусств, предметы быта и т.д.).
Латунь хорошо прокатывается, штампуется и несколько дешевле меди, так как цинк более дешевый металл по сравнению с медью.
Другие сплавы меди называются бронзами. Наиболее распространенная бронза – оловянная. Она содержит от 5 до 80% олова. В зависимости от содержания олова свойства и назначение меняется. При содержании олова 10-13% ее цвет красновато-желтый, а более 27-30% - белый. Подшипниковая бронза содержит 81-87% меди. Для изготовления подшипников, различных тормозных устройств, где происходит скольжение металла, применяют бронзы, содержащие до 45% свинца. В часовых и других точных механизмах, где нужна высокая механическая прочность и коррозионная стойкость, применяется бериллиевая бронза, содержащая 1-2% бериллия. Ее прочность равна прочности стали.
В быту и особенно в химической промышленности применяют сплавы меди с никелем, например монель-металл, в котором отношение меди к никелю равно 2:1, и мельхиор, в котором это соотношение равно 4:1. Мельхиор по внешнему виду похож на серебро, из него приготовляют предметы домашнего обихода: ложки, вилки, подносы и т.д. Монель-металл применяют для изготовления монет, различных реакторов для химической промышленности, так как это сплав коррозионно-стоек.
Гидроксокарбонат меди (II) – (CuOH)2CO3 – применяют для получения хлорида меди (II), для приготовления синих и зеленых минеральных красок, а также в пиротехнике.
Сульфат меди (II) – CuSO4 – в безводном состоянии представляет собой белый порошок, который при поглощении воды синеет. Поэтому он применяется для обнаружения следов влаги в органических жидкостях.
Смешанный ацетат-арсенит меди (II) – Cu(CH3COO)2*Cu3(AsO3)2 – применяют под названием “парижская зелень” для уничтожения вредителей растений.
Из солее меди вырабатывают большое количество минеральных красок, разнообразных по цвету: зеленых, синих, коричневых, фиолетовых и черных. Все соли меди ядовиты, поэтому медную посуду лудят – покрывают внутри слоем олова, чтобы предотвратить возможность образования медных солей. [4, с.123-124]
10. Использованная литература.
1. Л.Ф.Попова. От лития до цезия. М., “Просвещение”, 1972.
2. В.Е.Лунев. Познакомьтесь с медью. М.,”Металлургия”, 1965.
3. Отв. за ред. Л.К.Иугалин. Химия минералов меди. Новосибирск, “Наука”, 1975.
4. Л.Ф.Попова. Медь. М., “Просвещение”, 1989.
5. Н.А.Фигуровский, "Открытие элементов и происхождение их названий". М., “Наука”, 1970.
6. В.С.Котлярова, Н.В.Касимова. Получение плёнок меди и опыты с ними // Химия в школе, №3, 1972.
7. http://www.chem.msu.su/rus/history/element/cu.html
8. И.Г.Подчайнова, Э. Н.Симонова. Аналитическая химия меди. М.,”Наука”, 1990.
Похожие работы
... 5`-р-(диаминоадамантил)-о-изопропилиденаденозинмонофосфата. 2. ОБЗОР ЛИТЕРАТУРЫ 2.1. ПЕРСПЕКТИВЫ ИСПОЛЬЗОВАНИЯ АДАМАНТАНА Химия адамантана и его производных является сравнительно молодым разделом органической химии (со времени обнаружения адамантана в нефтях прошло примерно 70 лет). В то же время, наблюдается постоянный рост числа исследований в этой области, особенно начиная с 70-х годов ...
... не только анионные, но и катионные комплексы. Так, в кислой среде существует катионный аквакомплекс [Al(OH2)6]3+, а в щелочной - анионный гидрокомплекс и [Al(OH)6]3-. В виде простого вещества алюминий - серебристо-белый, довольно твердый металл с плотностью 2,7 г/см3 (т.пл. 660оС, т. кип. ~2500оС). Кристаллизуется в гранецентрированной кубической решетке. Характеризуется высокой тягучестью, ...
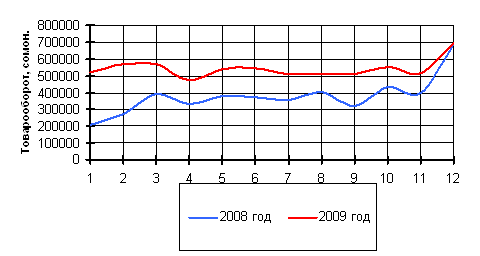
... дохода (валовой доход минус переменные затраты) для определения размера торговой надбавки. Анализ издержек обращения направлен на выявление возможностей повышения эффективности работы торгового предприятия за счет более рационального использования трудовых, материальных и финансовых ресурсов в процессе осуществления актов купли-продажи товаров и организации торгового обслуживания потребителей. ...
... ;à НbО2- + ННb + СО2 Кислотно-основные свойства лигандов, связанных с комплексообразователем, часто выражены более ярко, чем кислотно-основные свойства свободных лигандов. 4. Комплексные соединения в аналитической химии 4.1 Качественный анализ катионов Первая группа катионов В первую аналитическую группу катионов входят ионов калия K+, натрия Na+, аммония NH4+ и магния Mg2+. ...
0 комментариев