Навигация
Фракционирование протеолитического комплексного
3.2 Фракционирование протеолитического комплексного
препарата ферментов.
Полученный осаждением органическими растворителями препарат нами назван „протовортманин Г10х”. В дальнейшем представляло интерес изучить его компонентный состав и идентифицировать протеолитические фракции. Для этого был использован метод дискового электрофореза в ПААГ. Электорофорез вели с учётом „нейтральной’’природы протеолитического комплекса.
Компонентный состав препарата представлен четырьмя фракциями, отличающимися подвижностью в электрическом поле, размерами и интенсивностью окраски белковых полос.
Идентификацию протеолитических фракций проводили двумя способами: насыщением ПААГ денатурированным гемоглобином (pH 7,2) после дискового электрофореза и последующим выявлением прогидролизованных участков; экстракцией белкового спектра из ПААГ дистиллированной водой с определением протеолитической активности в экстрактах.
При гидролизе гемоглобина в ПААГ обнаружены две протеолитические фракции, которые проявились в виде двух светлых полос. Это свидетельствовало о том, что комплекс ферментов, гидролизующий белки в нейтральной области pH сложен и представлен двумя фракциями. Аналогичными были данные при использовании метода экстракции белковых полос из геля.
Таким образом, используя методы дискового электофореза было установлено, что компонентный состав полученного препарата представлен четырьмя фракциями, две из которых протеолитические. Кроме активного протеолитического комплекса препарат „протовортманин Г10х” содержал в своём составе глюкоамилазу (ГЛА 20ед/г) и альфаамилазу (3ед/г), сопутствующие ферменты, а также баластные вещества. Для получения гомогенных протеолитических фракций необходимо ввести более глубокую очистку.
3.3 Влияние температуры и рН на активность фермента.
Нами была поставлена цель определить рН и температурные оптимумы действия выделенных протеиназ Penicillium wortmannii 2091 и дать их сравнительную характеристику.
Нужное значение рН субстрата поддерживали с помощью 0,1М универсального буфера. Гидролиз вели при температуре 30оС в течение 30 минут. Ферментативную активность определяли стандартным методом [12].
Как видно на рис.2, препарат проявляет определённую активность в широкой зоне рН. Однако максимум активности наблюдается при различных значениях рН. Протеиназа 1 имеет оптимальное значение рН 7,2, в то время как протеиназа 2 – 10,0. Таким образом, протеиназа 1 имеет нейтральную природу, а протеиназа 2 – щелочную.
Температурный оптимум действия ферментов определяли в интервале температур 30 – 80оС при оптимальных значениях рН 7,2 и 10,0. На рис.3 показано влияние температуры на активность ферментов. Для протеиназы 1 максимальный гидролиз наблюдается при температуре 60оС, а протеиназы 2 – 40оС.
Таким образом, протеолитический комплекс Penicillium wortmannii 2091 представлен двумя ферментами, имеющими различные температурные и рН – оптимумы.
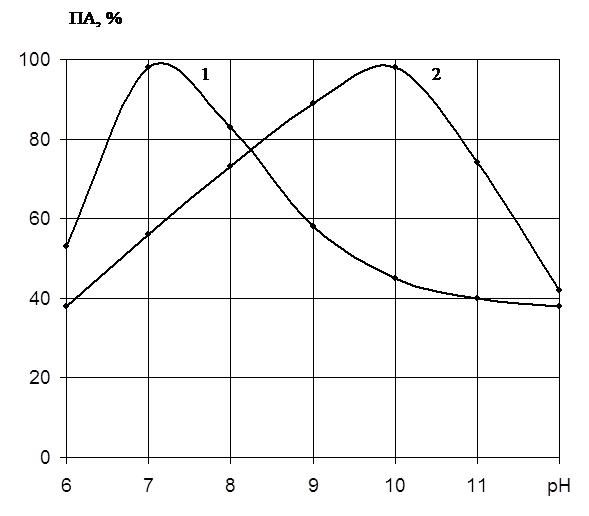 | |||
| |||
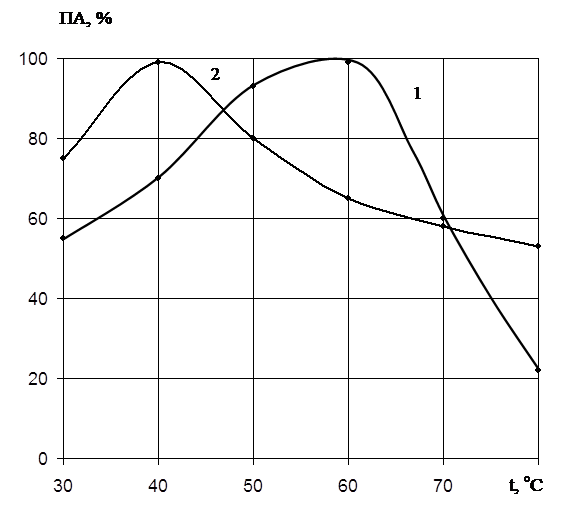 | ||||
| ||||
3.4 Определение молекулярной массы.
Молекулярную массу ферментов Penicillium wortmannii 2091 определяли методом гель-фильтрации на сефадексе У-100 [8].
Установлено, что соотношение объёма элюента, необходимого для выноса исследуемого белка из колонки (V – объём элюента) и объёма элюата, размещающемся в свободном (не занятом гранулами сефадекса) пространстве колонки (V0 – свободный объём), обратно пропорционально величине молекулярной массы белка. Для расчёта использовали формулу:
LgM=5,941-0,847 V/V0
Молекулярная масса протеиназы 1 оказалась равной 34500, протеиназы 2 – 20800, т.е. обе фракции относятся к низкомолекулярным белкам.
0 комментариев