Навигация
3 г-иона/л при 250С.
Решение.
Найдем в таблице стандартных электродных потенциалов значение ф0 для электродной реакции.
ф0 = PbO2, H+/PbSO4 = 1,685 в,
ф PbO2
H+/PbSO4 = ф0 + (2,303*8,314/2*96491,4) lg ([PbO2]*[H+]4/[PbSO4]*[H2O]2) =
ф0(0,0591/2)*lg[H+]4 = 1.685 + 0.0295*lg34 = 1.713 (в).
Двуокись свинца и сернокислый свинец – твердые вещества, концентрация их принимается равной единице. Количество воды в растворе велико по сравнению с тем, которое образуется в рассматриваемой реакции, а поэтому ее концентрация в расчет не принимается.
Пример 2.
Рассчитать значение потенциала меди, находящегося в растворе, содержащем 0,1 г-ион/л катионов Cu2+ при температуре 250 С.
Решение.
ф Cu2+/ Cu = 0,34+(0,0591/2)*lg (0.1/1) =0.31(в).
Стандартные электродные потенциалы некоторых окислительно-восстановительных систем при 250 С
| № | Окисленная форма | Восстановленная форма | Уравнение реакции | В |
| 1. | Li+ | Li | Li+ + 1ē↔Li | -3,05 |
| 2. | K+ | K | K+ + 1ē↔K | -2,92 |
| 3. | Ba2+ | Ba | Ba2+ + 2ē ↔Ba | -2,90 |
| 4. | Ca2+ | Ca | Ca2+ + 2ē ↔Ca | -2,87 |
| 5. | Na+ | Na | Na+ + 1ē↔Na | -2,71 |
| 6. | Mg2+ | Mg | Mg2+ + 2ē↔Mg | -2,36 |
| 7. | Al3+ | Al | Al3+ + 3ē↔Al | -1,66 |
| 8. | Mn2+ | Mn | Mn2+ + 2ē↔Mn | -1,05 |
| 9. | SO32- | S | SO32- + 4ē + 3H2O ↔ S + 6OH- | -0,90 |
| 10. | SO42- | SO32- | SO42- + 2ē + H2O ↔ SO32- + 2OH- | -0,90 |
| 11. | NO3- | NO2 | NO3- + ē + H2O ↔ NO2 + 2OH- | -0,85 |
| 12. | H2O | H2 | H2O + 2ē↔ H2 + 2OH- | -0,83 |
| 13. | Zn2+ | Zn | Zn2+ + 2ē ↔Zn | -0,76 |
| 14. | Cr3+ | Cr | Cr3+ + 3ē↔Cr | -0,74 |
| 15. | Fe2+ | Fe | Fe2+ + 2ē↔Fe | -0,44 |
| 16. | Ni2+ | Ni | Ni2+ + 2ē↔Ni | -0,25 |
| 17. | Sn2+ | Sn | Sn2+ + 2ē↔Sn | -0,14 |
| 18. | Pb2+ | Pb | Pb2+ + 2ē↔Pb | -0,13 |
| 19. | 2H+ | H2 | 2H+ + 2ē↔H2 | 0,00 |
| 20. | Cu2+ | Cu | Cu2+ + 2ē↔Cu | 0,34 |
| 21. | Ag+ | Ag | Ag+ + 1ē↔Ag | 0,80 |
| 22. | NO3- | NO2 | NO3- + ē + 2H+↔ NO2 + H2O | 0,81 |
| 23. | Br2 | 2Br- | Br2 + 2ē↔2Br- | 1,07 |
| 24. | O2 | H2O | O2 + 4ē + 4H+↔2H2O | 1,23 |
| 25. | Cl2 | 2Cl- | Cl2 + 2ē↔2Cl- | 1,36 |
| 26. | Au3+ | Au | Au3+ + 3ē↔Au | 1,50 |
| 27. | F2 | 2F- | F2 + 2ē↔2F- | 2,87 |
Таблица 1.
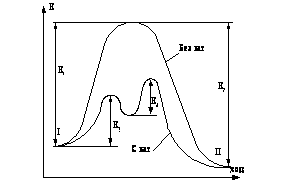
5. Напряжение разложения электролита.При наложении на электроды внешнего тока равновесие электродных реакций [Ох]+nе < > [Red] нарушается. На электроде, присоединенном к отрицательному полюсу источника тока, оно сместится вправо, а потенциал — до значения, при котором скорость реакции восстановления окислителя будет превосходить скорость обратной реакции на величину внешнего тока. На электроде, присоединенном к положительному полюсу источника тока, будут происходить аналогичные электродные процессы, но противоположно направленные. В результате смещения потенциалов в электролизере возникает э. д. с, равная напряжению, приложенному извне, и противоположная по направлению. Однако, как показывает опыт, ток заметной величины начинает проходить через электролитическую ячейку лишь при достижении напряжения на электролизере до определенной величины. Зависимость силы тока от приложенного напряжения при электролизе показана на графике (рис. 2). На кривой виден излом. Продолжение прямого участка кривой до пересечения с ось абсцисс отсекает на ней отрезок, равный минимальному напряжению, необходимому для разложения электролита инертных электродах, при котором происходит электролиз с заметной скоростью. Это минимальное напряжение называют напряжением (э.д.с.) разложения электролита.
Равновесные потенциалы электродных реакций, протекающих при электролизе, рассчитывают по формуле Нернста. Для этого в таблице стандартных электродных потенциалов находят значения потенциалов реакций, подставляют в формулу концентрации веществ, участвующих в электродных реакциях и решают уравнение с одним неизвестным. Разность найденных по формуле Нернста равновесных потенциалов катода и анода равна э. д. с, при которой скорости прямых и обратных реакций на электродах равны. Следовательно, при найденном значении э. д. с. ток в цепи равен нулю. Электролиз будет протекать лишь при напряжении, превосходящем разность равновесных потенциалов электродных реакций. Только при таком условии возможно прохождение тока. Например, при электролизе воды катод можно рассматривать как водородный, а анод как кислородный электроды. Э. д. с. такой пары электродов при отсутствии тока в цепи и рН—7 равна 1,23 в.
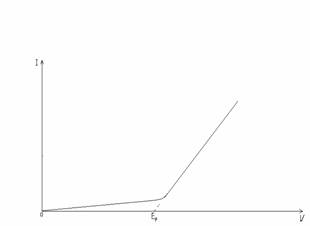
Рис. 2. График зависимости силы тока от напряжения при электролизе.
При получении кислорода и водорода электролизом, раствора серной кислоты на платиновых электродах требуется напряжение на 0,5 в большее, чем 1,23 в, а именно не менее 1,7 в. Эта часть напряжения необходима для преодоления сопротивления протеканию тока, связанного с перенапряжением (затруднением) электрохимических реакций, и сопротивления электролита.
V=фа - фк +na +nk + фраств
Где V – напряжение на электродах ванны;
фа и фк – потенциалы катода и анода, рассчитанные по формуле Нернста,
с учетом изменения концентрации веществ при электролизе;
фраств – падение напряжения на сопротивлении раствора
na и nk – перенапряжение анодной и катодной реакций.
При этом часть электродной энергии превращается в химическую, а часть – в тепловую.
A = n*F*v = n*F*(фа - фк +na +nk + фраств ) = An + Ah + Aраств
Где n*F – число Фарадеев электричества, необходимое для восстановления
на катоде и окисления на аноде 1 моля вещества.
An - Полезная работа (An = n*F*(фа - фк));
Aраств - теплота освобождающаяся на сопротивление электролита
(Араств = n*F*фраств);
Ah - теплота освобождающаяся на сопротивление перенапряжения
(Ап = n*F*(na +nk));
Из этих уравнений следует, что перенапряжение электродных реакций и сопротивление раствора снижают к. п. д. электролитической ванны.
Напряжение разложения электролита равно разности между напряжением, подаваемым на ванну, и падением напряжения на сопротивлении раствора. Оно складывается из равновесных электродных потенциалов и соответствующих перенапряжений катодной и анодной реакций:
Ep = v - фраств = фа - фк +na +nk
Напряжение разложения зависит как от природы электролита, так и от природы электродов.
6. Поляризация электродов.При электролизе потенциалы электродов смещаются в противоположные стороны до значений, при которых становится возможным протекание катодной и анодной реакций. Это явление носит название поляризации. Электроды при электролизе поляризуются в следствии следующих причин:
изменения химической природы поверхности электродов при накоплении на них продуктов электролиза (химическая поляризация);
замедленности стадии разряда (ионизации) участвующих в реакции веществ при последующих неэлектрохимических стадий (перенапряжение);
медленного подвода (отвода) к электроду веществ, участвующих в электродном процессе, по сравнению со скоростью самой реакции (концентрационная или диффузионная поляризация).
Химическая поляризация электродов наблюдается в тех случаях, когда на них адсорбируют или отлагаются продукты окисления-восстановления. Так, например, на платиновом катоде при электролизе воды адсорбируется водород и катод из платинового как бы превращается в водородный, для которого характерна электродная реакция 2Н+ + 2е « Н2 и соответствующее значение потенциала. При выделении хлора на платиновом электроде платиновый электрод превращается в хлорный. Точно так же при гальваническом покрытии меди никелем медный электрод превращается в никелевый, и потенциал смещается в отрицательную сторону до значения, соответствующего никелевому электроду.
В ряде случаев прохождению электрического тока препятствует замедленность перехода электронов с катода на восстанавливающиеся частицы или с частиц восстановителя на анод. Для того чтобы электролиз протекал с достаточно высокой скоростью, потенциал катода должен быть смещен от равновесного значения в отрицательную сторону, а потенциал анода соответственно в положительную. Затрудненной может оказаться и какая – либо другая стадия электродной реакции, например десорбция газообразных продуктов электролиза, образование новой фазы на поверхности электрода (кристаллов металла или пузырьков газа), соединение атомов в молекулы, адсорбция разряжающихся ионов и.т.д.
Перенапряжение электродных реакций можно вычислить по разности между напряжением разложения и э.д.с. химической поляризации:
na + nk = Ер - фа + фк
Оно зависит от плотности тока, проходящего через электроды, и эта зависимость выражается уравнением Тафеля:
nk = a + b * lg ik
na = a, + b, * lg ia
где ia и ik – плотность тока на аноде и соответственно на катоде, а/ см2
a(a’) и b(b’) – константы.
При повышении температуры на 10 С перенапряжение уменьшается на
2-3 мв. Оно также зависит от природы вещества, из которого изготовлен электрод. Например, при выделении водорода из соляной кислоты на катоде из платины при плотности тока 1 А/см2 требуется напряжение всего 0,1 в, в то время как на катоде из свинца – 1,5 в, а из ртути – 1,4 в.
Перенапряжение выделения водорода и кислорода на некоторых электродах при 200 С.
| Электроды | Перенапряжение, в | ||
| водорода | кислорода | ||
| ik = 1 А/см2 | ik = 1мА/см2 | iа = 1мА/см2 | |
| Платина гладкая | 0,1 | 0,02 | 0,7 |
| Никель | 0,64 | 0,34 | 1,09 |
| Железо | 0,7 | 0,33 | 1,07 |
| Серебро | 0,95 | 0,4 | 0,97 |
| Медь | 0,8 | 0,455 | 1,05 |
| Олово | 1,24 | 0,86 | 1,21 |
| Цинк | 1,24 | 0,89 | 1,75 |
| Кадмий | 1,4 | 1,04 | ¾ |
| Ртуть | 1,406 | 1,06 | 1,62 |
| Свинец | 1,56 | 1,23 | 1,44 |
| Графит | ¾ | 0,6 | 1,17 |
Таблица 2.
Таким образом, при выборе электродов кроме окислительно-восстановительного потенциала системы, необходимо учитывать и перенапряжение реакций. Так, высокое перенапряжение разряда ионов водорода на цинке делает возможным восстановление ионов цинка из водного раствора, несмотря на то, что равновесный потенциал цинкового электрода более отрицателен, чем водородного.
Пользуясь формулой Нернста, можно найти, что потенциал водородного электрода находится в линейной зависимости от рН раствора.
В тех случаях, когда перенапряжение электродной реакции невелико (что характерно для реакций восстановления многих металлов), скорость электролиза (сила тока) определяется диффузией, миграцией ионов в электрическом поле и перемешиванием раствора. Так как частицы, принимающие участие в реакциях, при достижении электрода мгновенно разряжаются, то их концентрация на поверхности электрода практически равна нулю. Из формулы же Нернста следует, что уменьшение концентрации окислителя приводит к смещению потенциала электрода в отрицательную сторону, а восстановителя в положительную. Если скорость электролиза ограничивается концентрационной поляризацией, то при увеличении напряжения быстро достигается предельное значение силы тока и ускорить электрохимическую реакцию повышением напряжения уже не удается. Дальнейшее повышение напряжения делает возможным протекание других электродных реакций, например разложение воды с выделением водорода и кислорода.
Концентрационная поляризация увеличивает напряжение в ванне. Ее можно уменьшить перемешиванием раствора. Однако перемешивание раствора по условиям электролиза часто неприменимо.
7. Падение напряжения на электролите.Переносчиком электричества в растворе являются ионы. При проведении электролиза приходится учитывать сопротивление раствора, так как на нем падает часть напряжения, и расход энергии возрастает.
I = V/r
а для электролитов
I = V- Ер /r
где I — сила тока;
V — напряжение;
r - сопротивление;
Ер — напряжение разложения.
Из закона Ома следует, что при постоянной силе тока требуется тем большее напряжение, чем выше напряжений разложения раствора. Сопротивление раствора при увеличении концентрации электролита снижается до минимальной величины, а при больших концентрациях снова возрастает. Оно связано с подвижностью ионов в растворе. Подвижность ионов зависит от их радиуса, заряда и вязкости среды (табл. 3).
В таблице 4 приведены значения удельного сопротивления (q) для некоторых растворов.
Удельное сопротивление электролита легко снизить, если повышать концентрацию раствора. Часто для повышения электропроводности в раствор вводят вещество, хорошо диссоциировонное на ионы, но не способное восстанавливаться и окисляться из водных растворов, например, сернокислый натрий.
При длительном электролизе в определенных условиях может наблюдаться эффект разделения зарядов.
Если через загущенный агар-агаром раствор хлорной меди пропускать длительное время постоянный ток, то катодное пространство объединится анионами, а анодное – катионами. В результате катодное пространство зарядится положительно, а анодное – отрицательно. Возникает э.д.с. противоположно направленная напряжению, приложенному к ванне. Далее может наступить момент полного разделения зарядов в растворе, а между анионами и катионами возникает “запорный слой” из чистой воды с большим сопротивлением. Электролиз при этом прекратится, а электролизер уподобится конденсатору. Движение ионов можно видеть только, когда катионы и анионы окрашены.
Удельное сопротивление растворов некоторых электролитов при 180 С.
| Электролит | Концентрация (в процентах) | Удельное Сопротивление | |
| Соляная кислота | 10 | 1,58 | |
| Серная кислота | 10 | 2,55 | |
| Азотная кислота | 12,4 | 1,84 | |
| Едкое кали | 8,4 | 3,67 | |
| Едкий натр | 10 | 3,23 | |
| сернокислая медь | 10 | 31,25 | |
| Хлористый калий | 10 | 7,38 | |
| Сернокислый калий | 10 | 11,62 | |
| Уксуснокислый калий | 9,33 | 16 |
Таблица 4.
При напряжении, достигающем напряжение разложения воды, электролизу подвергается и вода. В этом случае также происходит разделение зарядов в ванне с загущенным электролитом. Катодное пространство при длительном электролизе зарядится отрицательно, а анодное – положительно.
8. Кулонометрия.По количеству выделившегося при электролизе вещества можно установить суммарное количество электричества. И наоборот, по количеству протекшего электричества представляется возможным определить содержание веществ в растворе, толщину гальванических покрытий, окислых пленок и др. Если принять во внимание, что потенциалы большинства электродных реакций известны, то по величине потенциала, при котором протекает та или иная реакция, определяют также, какие вещества содержатся в растворе (качественный анализ). Из электрохимических методов анализа в настоящее время применяют полярографию, потенциометрию и кулонометрию.
Метод количественного анализа, основанный на законе Фарадея, называется кулонометрией.
Кулонометры.
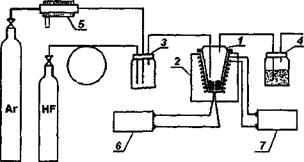
Приборы, применяемые для измерения количества электричества, называют кулонометрами. Широко применяются весовые (серебряный, медный) и объемные (ртутный, газовый) кулонометры. В серебряном кулонометре (рис. 3) анод делают из платины или серебра. Диафрагмой служит пористый сосуд, препятствующий попаданию кислорода на катод. В кулонометр наливают слегка подкисленный раствор азотнокислого серебра. Процесс ведут при катодной плотности тока, не превышающей 0,02 А/см2, и анодной плотности тока не более 0,2 А/см2. По увеличению веса катода определяют количество восстановившегося серебра и рассчитывают количество электричества, прошедшего через раствор. Серебряный кулонометр наиболее точный. Ошибка составляет не более 0,005 процента.
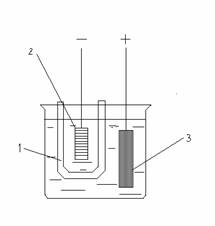
Рис. 3 Весовой кулонометр.
1 – пористый сосуд. 2 – катод.
3 – анод.
В медном кулонометре катод и анод изготавливают из меди. Раствор содержит 50 г/л серной кислоты (уд. в. 1,84), 150 г/л медного купороса и 50 г/л сахара. Сахар необходим для предотвращения реакции, происходящей в электролите:
Сu+ ® Cu2+ +Cu¯
Процесс ведут при плотности тока в электродах 0,002 – 0,02 А/см2. Медный кулонометр не обеспечивает высокой точности (ошибка ~0,2 процента), так как в электродах образуются ионы Cu+ и на катоде восстанавливается кислород, попадающий в раствор из воздуха.
В ртутном кулонометре анодом служит ртуть, катодом – графит, электролитом – раствор, содержащий 225 г/л йодистой ртути и750 г/л йодистого калия. При электролизе металл анода окисляется и переходит в раствор в виде ионов Hg2+. На катоде происходит их восстановление и накапливается металлическая ртуть, которая стекает в градуированную (в кулонах) трубку. Ртутный кулонометр дает большую ошибку (около 1 процента), но удобен при измерении больших количеств вещества и позволяет работать с большими плотностями тока (I < 0.1 А/см2).
В газовом кулонометре электродами служат никелевые пластинки. Электровводы, проходящие через стеклянную стенку кулонометра внутрь ячейки, делают из молибденовой проволоки, которая хорошо впаивается в стекло. Электролитом служит 15-процентный раствор сернокислого натрия или 20-процентный раствор едкого натра. Электролиз ведут при катодной плотности тока не выше 0,04 А/см2. Количество электричества рассчитывают по объёму водорода и кислорода в эвдиометре. Подставив значение g из уравнения Менделеева – Клапейрона в уравнение
g=N*э = (э*I*t)/F, получим
Q = I*t = (g*F)/э = (P*v*M)/R*T * (F/э) * 2/3 =
= 2.064074*(P –PH2O)*v/T (k)
В этом уравнении расчет ведется на водород. Поэтому в уравнении введен коэффициент 2/3, так как водород составляет 2/3 от объёма газовой смеси.
По количеству электричества, пошедшего через кулонометр (Qk), включенного последовательно в цепь с электролизёром, можно определить выход по току (g), если известно количество вещества (g), выделившегося на катоде или аноде электролизера. Для этого из уравнения g=N*э = (э*I*t)/F рассчитывают количество электричества, пошедшего на данную электродную реакцию (Qэ).
Qэ = g*F/э.
И далее находят выход по току в процентах:
g = Qэ / Qk*100%
С помощью кулонометра по количеству электричества, которое необходимо для полного выделения вещества, для электродной реакции
Ох + ne®Red
или
Red - ne®Ox,
Можно определить концентрацию этого вещества в растворе (если известна n) или величину n (если известна концентрация).
При проведении кулонометрического анализа побочные электродные реакции в электролизёре, снижающие выход по току, должны быть исключены.
Так как окислительно-восстановительные потенциалы для большинства веществ известны, то побочных реакций можно избежать, если процесс вести при строго определенном потенциале, при котором другие вещества ещё не выделяются. Непременным условием аналитического определения является обнаружение конца реакции. Если реакция ведется при постоянном потенциале, то на её завершение указывает падение силы тока в цепи до нуля.
А Б
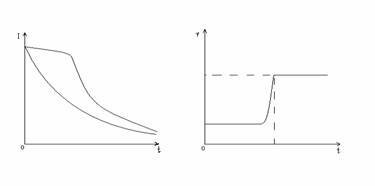
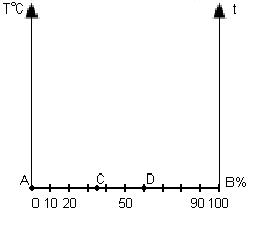
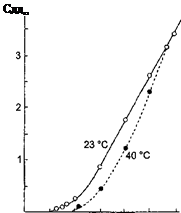
рис. 4 Графики зависимости силы тока и потенциала от времени:
а – изменение силы тока при постоянном потенциале.
б – изменение потенциала при постоянной силе тока.
Однако для достижения полного выделения вещества требуется много времени, так как сила тока во времени уменьшается плавно (рис. 4-а).
При постоянной силе тока на завершение реакции указывает резкое изменение потенциала, например при анодном растворении цинкового покрытия с железного изделия (рис. 4-б).
9. Кулонометрический анализ при постоянном потенциале.
Схема электрической цепи для кулонометрического анализа при постоянном потенциале приведена на рисунке 5. Для поддержания потенциала электрода необходимо чтобы сила тока проходящего через сопротивление r1и r2 была в 10 – 100 раз больше, чем в боковой цепи. Этого можно достигнуть, если сопротивление r1 будет в 10 – 100 раз меньше суммарного сопротивления в боковой цепи, что устанавливается в каждом случае опытным путем.
В качестве источника постоянного тока можно взять батарею аккумуляторов на 12 в или селеновые выпрямители, чтобы ёмкость источника тока была большой. Зарядный потенциал поддерживается с помощью сопротивлений R1 и R2 и контролируется потенциометром. Лучше пользоваться показывающим потенциометром ЛПУ – 01. Можно пользоваться также и другими потенциометрами с высокоомным входом. Электродом сравнения может служить насыщенный каломельный электрод fкалом = 0,243 в. В тех случаях, когда перенос продуктов анодной реакции на катод или продуктов катодной реакции на анод снижает выход по току и недопустим, электрод, по которому не ведут расчет, помещают в пористый сосуд или стеклянную трубку, со стеклянным фильтром, заполненным растворами сернокислого натрия, азотнокислого калия или серной кислоты.
Влияние кислорода по катодному току исключают барбатированием водорода, азота или инертного газа. Мешалка необходима для выравнивания концентрации вещества в полном объеме. Тип кулонометра, включаемого в измерительную цепь, определяется допустимой погрешностью измерений.
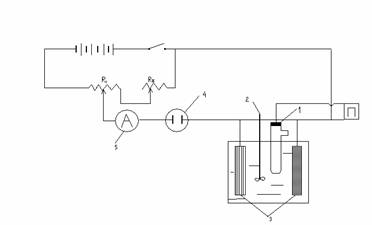
рис. 5 Схема электрической цепи для кулонометрического анализа при постоянном потенциале.
П – потенциометр
1 – электрод сравнения 5 - миллиамперметр
2 – мешалка R1 и R2 – переменные
3 – электроды сопротивления
4 - кулонометр
Работа сводится к наложению на электрод потенциала (при котором возможна лишь одна реакция), к его поддержанию на заданном уровне, к установлению конца реакции и к определению количества протекшего электричества. Так как для достижения 100-процентного выделения вещества из раствора требуется много времени, то электролиз прекращают, когда сила тока уменьшится в 100 – 500 раз. Процесс заканчивается тем быстрее, чем больше площадь электрода, на котором происходит разряд вещества, и чем меньше объём электролита.
Катодное восстановление веществ с аналитической целью часто проводят на ртути. В этом случае перенапряжение водорода так высоко, что оно не мешает определению.
10. Заключение.Теоретическое значение открытых закономерностей было очень велико. Они подтвердили атомистическую природу электричества. Законы, установленные Фарадеем, дали возможность применять процессы электролиза па практике и позволили делать количественные расчеты. Оказалось, что законы Фарадея в полной мере применимы к электродным процессам, происходящим в гальванических элементах при их работе.
Похожие работы
... с кислородом, восстановлением - отнятие кислорода. С введением в химию электронных представлений понятие окислительно-восстановительных реакций было распространено на реакции, в которых кислород не участвует. В неорганической химии окислительно-восстановительные реакции (ОВР) формально могут рассматриваться как перемещение электронов от атома одного реагента (восстановителя) к атому другого ( ...
... пособие по прикладной химии «Задачи по теоретическим основам химической технологии», составленное по материалам представленной работы. 3. Методика решения задач по теоретическим основам химической технологии Одна из главных задач химической науки и промышленности - получение необходимых человеку веществ (продуктов, материалов). Поэтому большинство учебных химических задач снизано с ...
... а в анодное—ионы SO42- . Таким образом, раствор во всех его частях будет оставаться электронейтральным. Однако в катодном пространстве будет накапливаться щелочь, а в анодном—кислота. Схема электролиза раствора сульфата калия: 2K2SO4 Катод ← 4K+ 2SO42- → Анод 4K+ 2SO42- 4Н2О + 4е- =4ОН- + 4Н 2Н2О=4Н+ + 2О + 4e- KОН ...
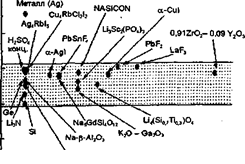
... при изучении синтеза новых материалов и процессов ионного транспорта в них. В чистом виде такие закономерности наиболее четко прослеживаются при исследовании монокристаллических твердых электролитов. В то же время при использовании твердых электролитов в качестве рабочих сред функциональных элементов необходимо учитывать, что нужны материалы заданного вида и формы, например в виде плотной керамики ...


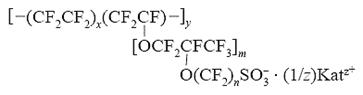
0 комментариев