Навигация
Присоединение аммиака к непредельным кислотам (таким способом получают β-аминокислоты)
3. Присоединение аммиака к непредельным кислотам (таким способом получают β-аминокислоты).
![]()
![]()
![]()
![]() CH2 = CH – C = O + HNH2 CH2 – CH2 – C = O
CH2 = CH – C = O + HNH2 CH2 – CH2 – C = O
OH NH2 OH
акриловая к-та β – оксипропионовая к-та
Присоединение водорода идет против правила Марковникова, так как сопряженные двойные связи.
4.Восстановительное аминирование. Протекает в растительных и животных организмах. Это способ связан с введением аминогруппы в кетокислоту. Протекает в два этапа:
![]()
![]()
![]() ОН
OH ОН
ОН
OH ОН
![]()
![]()
![]()
![]()
![]() С = О +NH3 C = O +2H. С = O
С = О +NH3 C = O +2H. С = O
![]()
![]()
![]() С = О -H2O
C = NH
СH – NH2
С = О -H2O
C = NH
СH – NH2
СН3 CH3 CH3
пировино- иминокислота аланин
градная к-та
Химические свойства аминокислот:
Они зависят от наличия:
1)карбоксильной группы
2)аминогруппы
3)от совместного наличия двух этих групп.
А) Свойства аминокислот, зависящие от наличия карбоксила.
Аминокислоты, как и любые кислоты, способны образовывать: а)соли; б)галогенангидриды; в)сложные эфиры; г)амиды; д)ангидриды; е)подвергаются декарбоксилированию.
![]()
![]() R – CH – C = O + H2O - соль
R – CH – C = O + H2O - соль

![]()
![]() NH2 ONa NH2 CL
NH2 ONa NH2 CL
![]() R – CH – C = O –хлорангидрид
R – CH – C = O –хлорангидрид
![]()
![]()
![]()
![]()
![]() R – CH – C = O R – CH – C = O + H2O
R – CH – C = O R – CH – C = O + H2O
NH2 OH NH2 O – CH3 – сложный эфир
![]()
![]() R – CH – C = O + H2O
R – CH – C = O + H2O
NH2 NH2 – амид
![]() R – CH2 - амин
R – CH2 - амин
NH2
Реакция декарбоксилирования аминокислот протекает в присутствии ферментов декарбоксилаз, а также при разложении белковых соединений, в результате таких реакций образуются амины (низшие амины содержатся в кишечных газах и имеют неприятный запах).
![]()
![]()
![]() NH2 – CH2 – CH2 – CH2 – CH2 – CH – C = O -CO2 NH2 – (CH2)5 – NH2
NH2 – CH2 – CH2 – CH2 – CH2 – CH – C = O -CO2 NH2 – (CH2)5 – NH2
лизин NH2 OH диамин пептаметилендиамин (кадаверин)
Б) Свойства аминокислот, зависящие от наличия аминогруппы.
1) Реакции ацилирования (ацил- радикал кислоты). По этой реакции один водород аминогруппы замещается на радикал кислоты – ацил. Примером может служить реакция обезвреживания бензойной кислоты в организме животных:
![]()
![]()
![]()
![]()
![]() C6H5 – C = O + HNH2 – CH2 – C = O C6H5 – C = O OH
C6H5 – C = O + HNH2 – CH2 – C = O C6H5 – C = O OH
OH OH NH – CH2 – C = O
бензойная к-та глицин гиппуровая к-та
2) Реакция аминирования (амин- углеводородный радикал). По этой реакции один водород аминогруппы замещается на углеводородный радикал – амин (такие реакции проводятся в лаборатории, когда надо протитровать аминокислоту, то есть количественно определить аминокислоту).
![]() OH
OH
![]()
![]()
![]()
![]() CH3 – CH – C = O + CH3 – I HI + CH3 – CH – C = O
CH3 – CH – C = O + CH3 – I HI + CH3 – CH – C = O
NH2 OH NH – CH3
аланин пористый
метил
По этой реакции аминогруппа как бы зажимается в тиски, блокируется и становится нереакционноспособной. Реакционноспособной становится только карбоксильная группа.
3) Реакции дезаминирования. Дезаминирование- это отщепление аминогруппы в виде аммиака. Такие реакции протекают в обменных процессах, а часто и при нарушении обмена. Они ведут к распаду аминокислот. Различают четыре вида дезаминирования:
а) окислительное дезаминирование.
![]()
![]()
![]() OH OH OH
OH OH OH
![]()
![]()
![]()
![]()
![]() C = O +O C = O +H2O C = O + NH3
C = O +O C = O +H2O C = O + NH3
![]()
![]()
![]() CH – NH2 ОКИСЛЕНИЕ C = NH
C = O
CH – NH2 ОКИСЛЕНИЕ C = NH
C = O
CH3 CH3 CH3
аланин иминокислота кетокислота (пировиноградная)
Окислительное дезаминирование – процесс, обратный восстановительному аминированию.
б) восстановительное дезаминирование. Протекает под действием водорода:
![]()
![]() OH OH
OH OH
![]()
![]()
![]() C = O +2H C = O + NH3
C = O +2H C = O + NH3
![]()
![]() CH – NH2 CH2
CH – NH2 CH2
CH3 CH3
аланин пропионовая(предельная) к-та
в) гидролитическое дезаминирование. Протекает под действием воды. При этом из аминокислоты образуются оксикислоты:
![]()
![]() OH OH
OH OH
![]()
![]()
![]() C = O +HOH C = O
+ NH3
C = O +HOH C = O
+ NH3
![]()
![]() CH – NH2 CH – OH
CH – NH2 CH – OH
CH3 CH3
аланин оксикислота (молочная)
г) внутримолекулярное дезаминирование:
![]()
![]() R
R
R
R
![]()
![]()
![]() CH2 CH
CH2 CH
![]()
![]()
![]() CH – NH2ПРОТЕКАЕТ В ОСНОВНОМ В МИКРООРГАНИЗМАХ CH + NH3
CH – NH2ПРОТЕКАЕТ В ОСНОВНОМ В МИКРООРГАНИЗМАХ CH + NH3
![]()
![]() C = O
C = O
C = O
C = O
OH OH
непредельная к-та
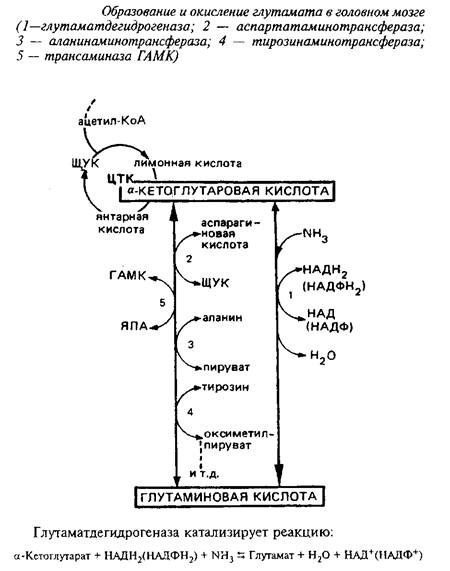
Основной путь дезаминирования – это окислительное дезаминирование. Этот вид дезаминирования преобладает у животных, растений и большинства микроорганизмов. Происходит под действием ферментов дегидрогеназ. Однако, активность дегидрогеназы тканей животных для большинства аминокислот очень низкая. Активна только дегидрогеназа глутаминовой кислоты. Поэтому большинство аминокислот в организме животных дезаминируются непрямым путем. Непрямое окислительное дезаминирование характеризуется предварительным переаминированием аминокислот с α- кетоглутаровой кислотой:
![]()
![]() COOH COOH
COOH COOH
![]()
![]()
![]()
![]() R CH2 R
CH2
R CH2 R
CH2
![]()
![]()
![]()
![]()
![]()
![]() CH – NH2 + CH2 C = O + CH2
CH – NH2 + CH2 C = O + CH2
![]()
![]() COOH
C = O COOH CH – NH2
COOH
C = O COOH CH – NH2
COOH COOH
амино- α-кетоглутаровая кетокис- глутаминовая
кислота к-та лота кислота
Образующаяся при этом глутаминовая кислота затем дезаминируется под действием глутаматдегидрогеназы до α-кетоглутаровой кислоты, которая может снова участвовать в непрямом дезаминировании других аминокислот.
![]()
![]()
![]() COOH COOH COOH
COOH COOH COOH
![]()
![]()
![]() CH2 CH2 CH2
CH2 CH2 CH2
![]()
![]()
![]()
![]()
![]() CH2-2H CH2 +H2O
CH2 + NH3
CH2-2H CH2 +H2O
CH2 + NH3
![]()
![]()
![]() CH – NH2 C = NH C = O
CH – NH2 C = NH C = O
COOH COOH COOH
глутаминовая иминокислота α-кетоглутаовая к-та
к-та
В) Свойства аминокислот, зависящие от совместного наличия карбоксильной и аминогруппы
1)Амфотерные свойства одноосновных моноаминокислот. Реакция водных растворов таких аминокислот на лакмус нейтральна. Это объясняется тем, что карбоксильная группа обладает кислотными свойствами, а аминогруппа – основными. Эти группы взаимодействуют с образованием, так называемых внутренних солей. Внутренние соли – это соли, образующиеся в результате взаимодействия кислотных и основных групп, находящихся в пределах одной и той же молекулы. При образовании внутренних солей аминокислот ион водорода отщепляется от карбоксильной группы и присоединяется к аминогруппе, которая превращается как бы в ион замещенного аммония. Например, для аланина:
![]()
![]()
![]()
![]()
![]() CH3 – CH – C = O CH3 – CH – C = O -
CH3 – CH – C = O CH3 – CH – C = O -
NH2 OH +NH3 O
![]() внутренняя соль (имеет два полюса + и -).
внутренняя соль (имеет два полюса + и -).
ОН
Такие аминокислоты ( с одной – С = О и одной NH2) обладают амфотерными свойствами, они могут реагировать как с кислотами, так и с основаниями, образуя при этом комплексные соли. Взаимодействие аминокислоты с кислотой:
![]()
![]()
![]()
![]()
![]() CH3 – CH – C = O + H+CL- CH3 – CH – C = O +
CH3 – CH – C = O + H+CL- CH3 – CH – C = O +
![]()
![]() +NH3 O- NH3 OH CL-
+NH3 O- NH3 OH CL-
комплексная соль, где аминокислота является катионом
![]()
![]()
![]()
![]() Взаимодействие со щелочью:
Взаимодействие со щелочью:
![]()
![]()
![]()
![]()
![]() CH3 – CH – C = O + NaOH CH3 – CH – C = O –
CH3 – CH – C = O + NaOH CH3 – CH – C = O –
![]()
![]() +NH3 O- NH2
O- Na+ + H2O
+NH3 O- NH2
O- Na+ + H2O
комплексная соль, где аминокислота является анионом
2) Образование ди- три и полипептидов. Эта реакция протекает в организме под действием ферментов пептидаз. Она ведет к образованию первичной структуры белка. При образовании дипептида две аминокислоты связываются пептидной связью. При этом одна аминокислота реагирует карбоксильной группой , а другая – аминогруппой.
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() CH3 – CH – C = O + HNH – CH2 – C = O -H2O CH3 – CH – C – NH – CH2 – C = O
CH3 – CH – C = O + HNH – CH2 – C = O -H2O CH3 – CH – C – NH – CH2 – C = O
NH2 OH OH NH2 O OH
аланин глицин дипептидаланинглицин
![]() – С = О
-пептидная связь
– С = О
-пептидная связь
NH
Та аминокислота, от которой уходит гидроксил карбоксильной группы, то есть остается кислотный радикал – ацил, меняет окончание «ин» на «ил».
3) Особое поведение аминокислот при нагревании, в присутствии водоотнимающих веществ.
а) α- аминокислоты при нагревании образуют циклические амиды – дикетопиперазины. взаимодействуют две молекулы :
![]()
![]() H3C
H3C
H3C
H3C
![]()
![]()
![]()
![]() CH – C = O CH – C = O
CH – C = O CH – C = O
![]()
![]()
![]() H2N
OH -2H2O NH NH
H2N
OH -2H2O NH NH
![]()
![]()
![]() HO NH2 O = C – HC
HO NH2 O = C – HC
![]() O = C – CH CH3
O = C – CH CH3
CH3 дикетопиперазин (2, 5 –диметил – 3, 6 дикетопиперазин)
Для разных кислот радикалы при группе – СН могут быть разными, а ядро дикетопиперазина одно и то же. По мнению русских ученых Землинского, Садикова дикетопиперазины содержатся в полипептидных цепях. Они связывают остатки аминокислот также, как и пептидные связи.
б) β-аминокислоты при нагревании теряют молекулу аммиака и превращаются в непредельные кислоты.
![]()
![]()
![]()
![]() CH3 – CH – CH2 – C = O -NH3 CH3 – CH = CH – C = O
CH3 – CH – CH2 – C = O -NH3 CH3 – CH = CH – C = O
NH2 OH OH
Β-аминомасляная к-та кротоновая к-та
в) γ-аминокислоты при нагревании, выделяя воду , образуют внутримолекулярные циклические амиды, так называемые лактамы:
![]()
![]()
![]()
![]()
![]() CH2 – CH2 – CH2 – C = O H2C – CH2
CH2 – CH2 – CH2 – C = O H2C – CH2
![]()
![]() NH2 OH H2C C = O - лактам γ-аминомасляной к-ты
NH2 OH H2C C = O - лактам γ-аминомасляной к-ты
γ-аминомасляная к-та NH
Лактам капроновой кислоты при полимеризации образует волокно-капрон.
Окислительно-восстановительные процессы, протекающие с участием аминокислот.
Эти процессы протекают в организмах растений и животных. Имеются такие соединения, которые способны либо выделять водород, либо поглощать его (присоединять). При биологическом окислении идет отщепление двух атомов водорода, а при биологическом восстановлении – присоединение двух томов водорода. Рассмотрим это на примере цистеина и цистина.
![]()
![]()
![]()
![]()
![]()
![]() CH2 – CH – C = O CH2 – CH – C = O
CH2 – CH – C = O CH2 – CH – C = O
![]()
![]() HS
NH2 OH -2H S NH2 OH
HS
NH2 OH -2H S NH2 OH
![]()
![]()
![]()
![]()
![]()
![]()
![]() HS
NH2 OH +2H S NH2 OH
HS
NH2 OH +2H S NH2 OH
CH2 – CH – C = O CH2 – CH – C = O
цистеин цистин
восстановленная форма окисленная форма
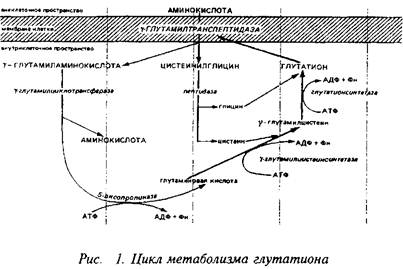
Две молекулы цистина, теряя два атома водорода, образуют окисленную форму – цистеин. Этот процесс обратимый, при присоединении двух атомов водорода к цистину образуется цистеин - восстановленная форма. Аналогично протекает процесс окислительно- восстановительный на примере трипептида – глутатиона, который состоит из трех аминокислот: глутаминовой, глицина и цистеина.
![]() цистеин
цистеин
![]()
![]()
![]()
![]()
![]()
![]() O = C – NH – CH – CH2 – SH O = C – NH – CH – CH2 – S – S –CH2 – CH – NH – C = O
O = C – NH – CH – CH2 – SH O = C – NH – CH – CH2 – S – S –CH2 – CH – NH – C = O
![]()
![]()
![]()
![]()
![]()
![]()
![]() CH2 C = O -2Н CH2 C = O C = O CH2
CH2 C = O -2Н CH2 C = O C = O CH2
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() CH2 NH +2Н CH2 NH NH CH2
CH2 NH +2Н CH2 NH NH CH2
![]()
![]()
![]()
![]()
![]()
![]() CH – NH2 CH2 глицин CH – NH2 CH2 CH2 CH – NH2
CH – NH2 CH2 глицин CH – NH2 CH2 CH2 CH – NH2
![]()
![]()
![]()
![]()
![]()
![]() C = O C = O C = O C = O C = O C = O
C = O C = O C = O C = O C = O C = O
OH OH OH OH OH OH
(2 молекулы)
трипептид восстановленная форма гексапептид – окисленная форма
При окислении отщепляется 2 атома водорода и соединяются две молекулы глутатиона и трипептид превращается в гексапептид, то есть окисляется.
Связывание минерального азота аминокислотами.
У растений при избытке азота в почве аминокислоты (аспарагиновая и глутаминовая) способны связывать его в виде аммиака с образованием амидов – глутамина и аспарагина.
![]()
![]() OH
NH2
OH
NH2
![]()
![]() C = O C = O
C = O C = O
![]()
![]() CH2
CH2
CH2
CH2
![]()
![]()
![]() CH2
+ NH3 CH2
CH2
+ NH3 CH2
![]()
![]() CH – NH2 CH – NH2
CH – NH2 CH – NH2
![]()
![]() C = O C = O
C = O C = O
OH OH
глутаминовая к-та глутамин
Аналогично идет образование аспарагина. В организмах животных также образуются амиды аспарагиновой и глутаминовой кислот, которые являются резервом (депо) азота.
Аммиак, который образуется при дезамиировании аминокислот, может связываться аспарагиновой и глутаминовой кислотами. При этом образуются амиды аспарагин и глутамин.
Список использованной литературы:
1) Овчинников Ю.А. Биоорганическая химия / Ю.А. Овчинников. – М.: Просвещение, 1987.
2) Яковишин Л.А. Избранные главы биоорганической химии / Л.А. Яковишин. – Севастополь: Стрижак-пресс, 2006.
3) Филиппович Ю.В. Основы биохимии. - М., 2007
4) Нейланд О.Я. Органическая химия.- М., 1990
Похожие работы
... стойкое вещество, содержащее много серы. Протеины применяются для изготовления пластических масс, клея. Далее мы приводим таблицу с некоторыми сведениями об аминокислотах и белковых веществах (на следующей странице). Аминоацил-транспортная РНК тРНК с аминоацильной группой, присоединенной к 2'- или 3'- гидроксильной группе концевого остатка аденозина. Аминоацильная группа быстро мигрирует между 2- ...
... - могут. Такие комбинированные продукты питания, которые содержат взаимодополняющие (комплементарные) белки, входят в состав традиционной кухни всех народов мира [5,6]. ГЛАВА 3. ЭКОЛОГИЧЕСКИЕ ОСОБЕННОСТИ ИЗУЧЕНИЯ ТЕМЫ «АМИНОКИСЛОТЫ» Человеческое тело не может запасать белки, поэтому сбалансированное белковое питание требуется человеку каждый день. Взрослому человеку весом 82 кг требуется 79 г ...
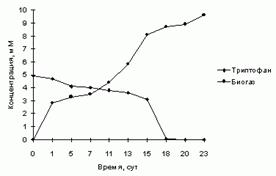
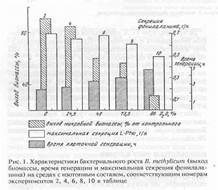
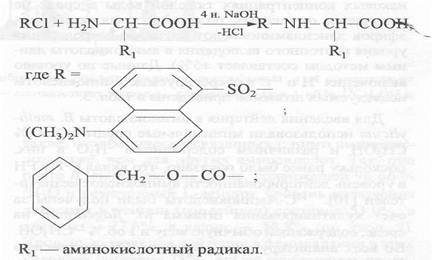
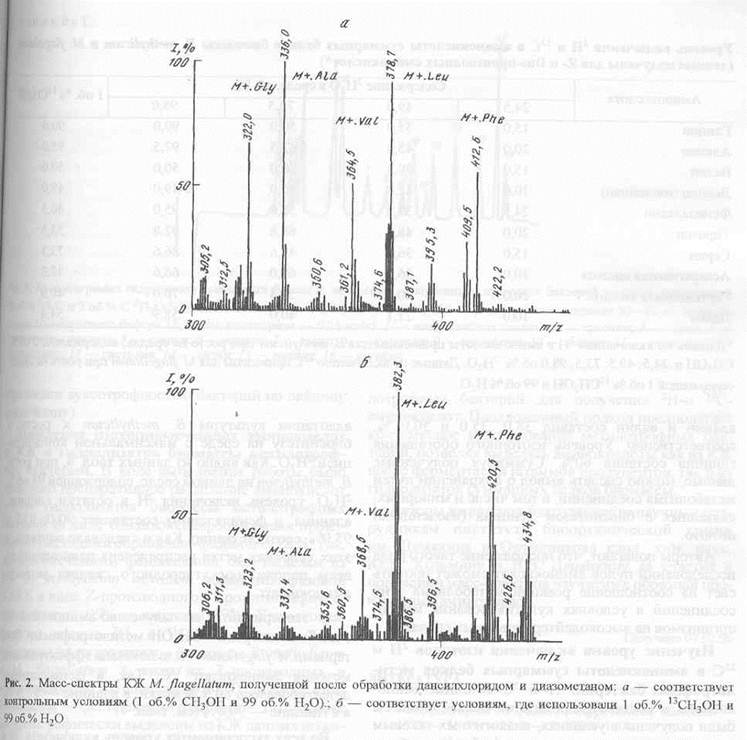
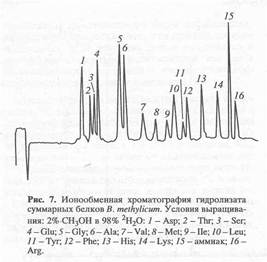
... , низкие уровни включения 2Н- и 13С в остатки лейцина (изолейцина) и метаболически связанные с ним аминокислоты, обусловлены ауксотрофностью бактерий в лейцине (изолейцине). Выделение изотопно-меченных аминокислот из культуральной жидкости и гидролизатов биомассы метилотрофных бактерий. В ходе выполнения работы было проведено препаративное разделение аминокислот культуральной жидкости и ...
... видов животных. Региональные различия в концентрации метионина невелики. Влияние диеты на концентрацию метионина в мозге также незначительно из-за конкурентных отношений с нейтральными аминокислотами за транспортные системы. Метионин в пуле свободных аминокислот утилизируется на 80% для синтеза белка. Метаболизм свободного метионина до цистеина начинается с образования S-аденозилметионина, ...

0 комментариев