Навигация
Все свойства кислотных оксидов
1. Все свойства кислотных оксидов.
P2O3 + 3H2O = 2H3PO3
2. Сильный восстановитель
O2+ P2+3O3 = P2+5O5
Фосфорный ангидрид P2+5O5 (оксид фосфора (V)).
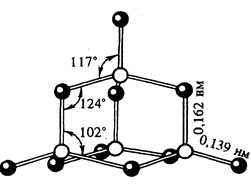
Белые кристаллы, t°пл.= 570°С, t°кип.= 600°C, r = 2,7 г/см3. Имеет несколько модификаций. В парах состоит из молекул P4H10, очень гигроскопичен (используется как осушитель газов и жидкостей).
Получение
4P + 5O2 = 2P2O5
Химические свойства фосфорного ангидрида
Все химические свойства кислотных оксидов: реагирует с водой, основными оксидами и щелочами
1) P2O5 + H2O = 2HPO3 (метафосфорная кислота)
P2O5 + 2H2O = H4P2O7 (пирофосфорная кислота)
P2O5 + 3H2O = 2H3PO4 (ортофосфорная кислота)
2) P2O5 + 3BaO = Ba3(PO4)2
3) P2O5 + 6KOH = 2K3PO4+ 3H2O
P2O5 - сильное водоотнимающее средство:
4) P2O5+ 2HNO3 = 2HPO3 + N2O5
P2O5+ 2HClO4 = 2HPO3+ Cl2O7
4.1.2. Фосфорные кислоты
| Формула | Название |
| HPO3 | Метафосфорная |
| H3PO2 | Фосфорноватистая (Диоксофосфорная) |
| H3PO3 | Ортофосфористая |
| H3PO4 | Ортофосфорная |
| H3PO5 | Мононадфосфорная |
| H4P2O5 | Пирофосфористая (Дифосфористая) |
| H4P2O6 | Фосфорноватная (Гексаоксодифосфорная) |
| H4P2O7 | Пирофосфорная |
| H4P2O8 | Динадфосфорная |
Свойства основных кислот
HP+5O3 Метафосфорная кислота
![]()
Получение
P2O5+ H2O = 2HPO3
Соли метафосфорной кислоты - метафосфаты (KPO3 – метафосфат калия)
Химические свойства
Характерны все свойства кислот.
H3P+5O3 Фосфористая кислота![]()
Бесцветное кристаллическое вещество; t°пл.= 74°С, хорошо растворимое в воде.
Получение
PCl3+ 3H2O = H3PO3+ 3HCl
Химические свойства
1) Водный раствор H3PO3 - двухосновная кислота средней силы (соли – фосфиты):
H3PO3+ 2NaOH = Na2HPO3+ 2H2O
2) При нагревании происходит превращение в ортофосфорную кислоту и фосфин:
4H3PO3 = 3H3PO4+ PH3
3) Восстановительные свойства:
H3PO3+ HgCl2+ H2O = H3PO4+ Hg + 2HCl
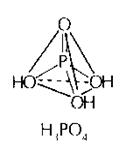 H3P+5O4 Ортофосфорная кислота
H3P+5O4 Ортофосфорная кислота
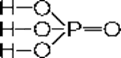
Белое твердое вещество, гигроскопичное, хорошо растворимое в воде; t°пл.= 42°С, r = 1,88 г/см3.
Диссоциация:
H3PO4 ↔ 3H+ + PO4-3
H3PO4+ 3H2O ↔ 3H3O+ + PO43-
H3PO4 ↔ H+ + H2PO4-
H2PO4- ↔ H+ + HPO42-
HPO42- ↔ H+ + PO43-
Ортофосфорная кислота - средней силы, не является окислителем, трехосновная. Она образует средние соли - ортофосфаты (Na3PO4) и два типа кислых солей - дигидрофосфаты (NaH2PO4) и гидрофосфаты (Na2HPO4).
Получение
1)
P2O5+ 3H2O ↔ 2H3PO4
Промышленный способ:
2)
Ca3(PO4)2(твердый) + 3H2SO4(конц.) ↔ 2H3PO4+ 3CaSO4¯
3)
3P + 5HNO3+ 2H2O ↔ 3H3PO4+ 5NO
Химические свойства
Для ортофосфорной кислоты характерны все свойства кислот – неокислителей. При нагревании она превращается в пирофосфорную кислоту:
2H3PO4 –t°↔ H4P2O7 + H2O
Качественная реакция на обнаружение в растворе анионов PO43-
3Ag+ + PO43- = Ag3PO4¯(ярко-желтый осадок)
Ортофосфорная кислота - сильная кислота по первой ступени диссоциации (К1 = 7,6*10-3), довольно слабая (слабее уксусной) по второй (К2 = 6,2*10-8) и очень слабая (слабее угольной) по третьей (К3 = 4,4*10-13).
Похожие работы
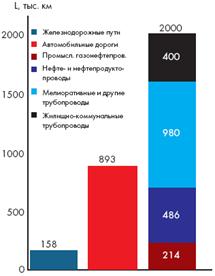
... срок их эксплуатации и необходимость проведения ремонтных и защитных работ после 8-10 лет их использования, проведения дополнительных испытаний, внутритрубной диагностики [18]. Преимущества трубопроводного транспорта: · Возможность повсеместной укладки трубопровода. · Низкая себестоимость транспортировки. · Сохранность качества благодаря полной герметизации трубы. · Меньшая материало ...
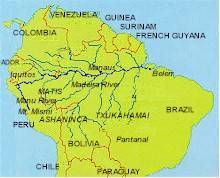
я характеристика, даваемая влажноэкваториальному ландшафту, применима именно к западной части Амазонской низменности. Здесь шире всего (до 1300 км с севера на юг) расступились окружающие ее возвышенности, и прогиб между ними оказался наиболее глубоким. Гранитное основание Гвианского массива выступает по верхней Риу-Негру и Какете, кристаллические же породы фундамента Бразильского нагорья вскры ...
... предыдущего чрезмерного стравления, в восстановлении будут преобладать разновидности сорняков. Глава 3. Проблемы горных территорий и возможные способы их решения. Природные и антропогенные катаклизмы. Природные катаклизмы в горах представляют результат геотектонической природы гор и их экологических характеристик. Однако катаклизмы зачастую вызываются деятельностью человека. Перед ...
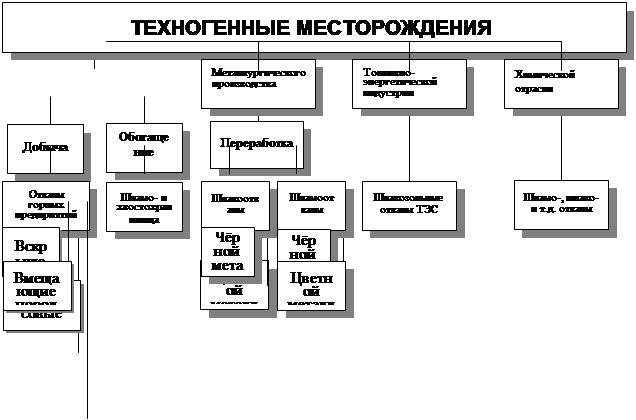
... занижение платежей за загрязнение ОС, складирование отходов и изъятие земель составило по АО «Свердловэнерго» в 1996 г. 2,33 млрд. рублей. 5.1. Технология формирования банка данных по техногенным месторождениям (БД ТМ) Технология построения БД ТМ основана на объединении: информационной базы и математических моделей распространения загрязнений в ОС (воздушном и водном бассейнах, почвах, донных ...






0 комментариев