Навигация
Изучение деструкции жиров методом потенциометрического титрования
3.2 Изучение деструкции жиров методом потенциометрического титрования
Метод основан на исследовании взаимодействия веществ с протонами потенциометрическим титрованием.
Кривые титрования позволяют:
- определить природу и число ионогенных групп в молекуле жира
- изучить влияние добавок щелочей на ионизацию эфирных групп жира
- оценить глубину и специфичность реакций жиров с микроорганизмами
- количественно определить деструкцию жиров.
Кривые титрования показывают зависимость числа связанных протонов омыленными жирами от рН среды. Величина рН измеряется непосредственно на приборе, число связанных протонов вычисляется. Число связанных ионов определяется по разности между общим числом добавленных ионов и числом свободных ионов в растворе.
Для изучения деструкции были выбраны следующие жиры: нерпичий, сульфатированный рыбий, шерстный, свиной и Tanning oil. Навеску жира, около 1г, взвешенную на аналитических весах, помещали в коническую колбу, в которой проводили щелочной гидролиз (п. 2.2.23), количественно переносили в мерную колбу на 250 см3 и объем доводили до метки дистиллированной водой. Затем отбирали пробу разбавленного гидролизованного жира 4 см3, переносили в стакан на 50 см3 и добавляли 33 см3 дистиллированной воды, для того чтобы мембрана стеклянного электрода была погружена в раствор. Измерение проводили на приборе рН-метр «Анион 7051» путем фиксирования значений рН раствора при добавлении по 0,1 см3 0,1 н. раствора соляной кислоты. Параллельно проводили титрование раствора чистой щелочи (5 см3 30% раствора NaOH переносили в мерную колбу на 250 см3, доводили до метки дистиллированной водой, для анализа брали 4 см3 раствора) и воды. При титровании соли жирной кислоты раствором кислоты происходит реакция обмена с образованием кислоты и соли:
RCOONa + HCl → RCOOH + NaCl
При титровании происходит помутнение раствора в момент образования жирной кислоты.
Для построения кривой титрования проводили расчет параметров по следующим формулам:
B = (CН * V1)/(V1+V) * 1000, где (1)
B – объем HCl, который добавлен к 100 см3 воды
CН – нормальная концентрация кислоты
V1 – добавленный объем,см3
V – начальный объем раствора,см3
C = (- lg B) (2)
D – экспериментальное значение рН
Строим график зависимости C от экспериментальных значений рН (находим формулу по линии Тренда, для подстановки в W)
Для изучения деструкции жира микроорганизмами предварительно были приготовлены бактериальные суспензии в колбах Эрленмейера на основе жидкой синтетической среды (п.2.2.8), содержащей около 1 г жира, объемом 200 см3 каждая. Культивирование микроорганизмов проводили в термостате марки (ТС-80М-2) при температуре (37±5)°С, осуществляя переменное механическое воздействие, на встряхивателе «Shaker Type-357», с частотой колебаний 200 об/мин, амплитудой 6 по 1 ч в сутки в течение 48 часов. После чего проводили гидролиз содержимого колбы (п.2.2.23), переносили в мерную колбу на 250 см3, доводили объем до метки дистиллированной водой и тщательно перемешивали. Затем отбирали объем пробы в количестве 4 см3 в стакан на 50 см3, добавляли 33 см3 дистиллированной воды. Титровали 0,1 н раствором соляной кислоты по 0,1 см3 на приборе рН-метр «Анион 7051» при температуре 20,6 ºС. При каждом объеме добавленной кислоты фиксировали значение рН и строили графики зависимости рН от объема и количество функциональных групп (N) от значений рН.
Пример расчета параметров для построения кривых титрования жира при добавлении 3 см3 кислоты (сульфатированный рыбий жир):
B = (0,1 * 3)/(3+33) * 1000 = 8,33
C = (- lg 8,33) =0,9208
D = 12,33 (экспериментальное значение рН)
F = 3мл (количество с известной концентрацией раствора реагента, добавленное к раствору жира, см3)
G = 0,057(объем HCl, который добавлен к водному раствору жира, см3)
H = (-lg G) = 1,243
Строим график зависимости lg B от экспериментальных значений рН для воды (находим формулу по линии Тренда, для подстановки в W)
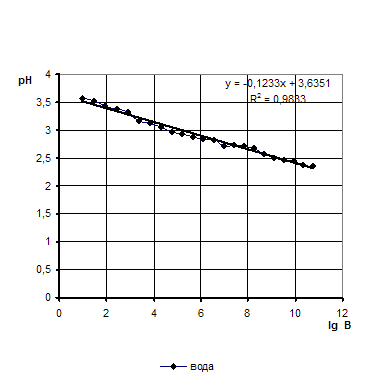
Рисунок 3- Кривая титрования воды 0,1н раствором соляной кислоты
Находим значение W при подстановки значений H в формулу, полученную по линии Тренда, вместо Х
-0,1233Х+3,6351=-0,1233*1,243+3,6351=3, 658
W = 3,658
J = 12,33
K = W- J = 3,658-12,33 = -8,061
L = 8,67
M = 1
N = (0,057*1*10)/0,139 =4,1109
Остальные расчетные данные представлены в таблице 4
Для определения количества групп СООН строим графики в координатах количество функциональных групп – рН.
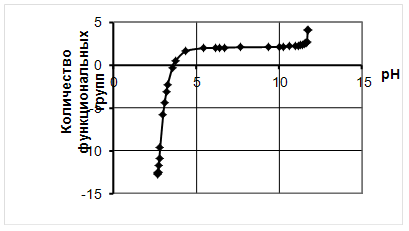
Рисунок 4- График зависимости количества карбоксильных групп от значений рН
Из рисунка 4 видно, что в диапазоне Рн 4,37 до 11,56 кривая представляет собой вид прямой при количестве функциональных групп равных 2. Поэтому данное значение принимаем равным 2.
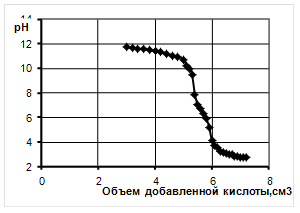
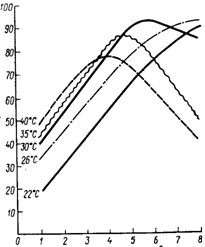
Рисунок 5 - Кривая титрования раствора сульфатированного рыбьего жира соляной кислотой
Кривая титрования омыленного жира характеризуется нейтрализацией избытка щелочи, олеатов и пальмитинатов натрия. Первой вступает в реакцию соль более слабой кислоты, так как полнее идет ее гидролиз. После полного гидролиза соли слабой кислоты в реакцию вступает натриевая соль более сильной кислоты. В результате нейтрализации образуются жирные кислоты, нерастворимые в воде, что сопровождается помутнением раствора. Качественное соотношение жирных кислот в жирах определялось по положению скачка на кривой потенциометрического титрования.
На основании обработки кривых потенциометрического титрования было определено, что исследуемые жиры – нерпичий, свиной, сульфатированный рыбий, шерстный и Tanning oil G могут содержать преимущественно олеиновую пальмитиновую и изомер пальмитиновой кислот. Кроме того в них могут содержаться незначительные количества линолевых кислот, миристиновой, пальмитолеиновой, арахидоновой.
Соли жирных кислот с одинаковым числом углеродных атомов титруются в один скачок - пальмитиновая и пальмитолеиновая. На кривой титрования четко выражены скачки, соответствующие нейтрализации солей жирных кислот. Расчетные данные показали, что количество групп СООН может составлять от 1 до 3 в расчете ммоль на г жира.
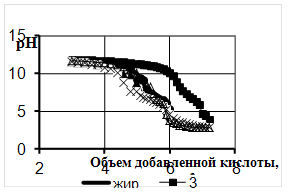
Рисунок 6 – Кривые титрования омыленного сульфатированного рыбьего жира, деструктированного микроорганизмами через 48ч
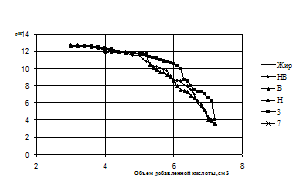
Рисунок 7 – Кривые титрования омыленного нерпичего жира, деструктированного микроорганизмами через 48ч

Рисунок 8 - Кривые титрования омыленного свиного жира, деструктированного микроорганизмами через 48ч

Рисунок 9 - Кривые титрования омыленного шерстного жира, деструктированного микроорганизмами через 48ч

Рисунок 10 - Кривые титрования омыленного Tanning oil G, деструктированного микроорганизмами через 48ч
Деструкция жира под действием микроорганизмов приводит к изменению числа карбонильных групп, то есть происходит расщепление молекулы жирной кислоты, увеличение ее силы, уменьшение длины углеродной цепи, что сопровождается смещением кривой титрования в область меньших значений рН и появлением новых скачков.
Действие микроорганизмов на жир имеет дифференцированный характер. Так штамм 7 дает 3 группы СООН при действии на Tanning oil G, 2- на шерстный жир. Культуры 3 и В полнее всего подвергают деструкции сульфатированный рыбий жир, Нв – свиной жир.
Положение кривой титрования гидролизованного жира, деструктированного микроорганизмами левее, относительно необработанного жира, свидетельствует о том, что деструкция жира проходит замедленно, образованные кислоты расщепляются частично. Количество солей жирных кислот правее кривой титрования необработанного жира свидетельствует об уменьшении количества жирных кислот вследствие их деструкции и превращении в большее число кислот с короткой углеродной цепочкой вплоть до образования альдегидов и выделения углекислого газа.
Таким образом, на основании рисунков 6-10 можно сделать вывод о том, что наиболее активна в отношении деструкции жиров культура 3. Она не только обладает деструктивными свойствами, но и использует жирные кислоты в качестве источника питания в результате своей жизнедеятельности, о чем свидетельствует смещение кривых титрования вправо, относительно необработанного жира и содержание кислот после действия микроорганизмов составило 21,55%.
Похожие работы
... HAC. 3.1 Изучение морфолого-физиологических и культуральных свойств микроорганизмов Целью данного этапа эксперимента являлось выделение, изучение свойств микроорганизмов и определение их видовой принадлежности. Исследуемые культуры были выделены из сточной воды после эмульсионного обезжиривания меховой овчины. Изучаемые культуры были обозначены номерами 3,7, F, G, I, Iў. Получение чистых культур ...
... Охрана окружающей среды Заключение Рисунок 2 – Сетевой график дипломной работы 2.1 Объекты исследования Объектом исследования в дипломной работе являлись микроорганизмы, выделенные из различных природных жиров: нерпичьего (Н), нерпичьего, выращенного на среде с шёрстным жиром (Нв), шерстного (В) и микроорганизмы, выделенные из ...
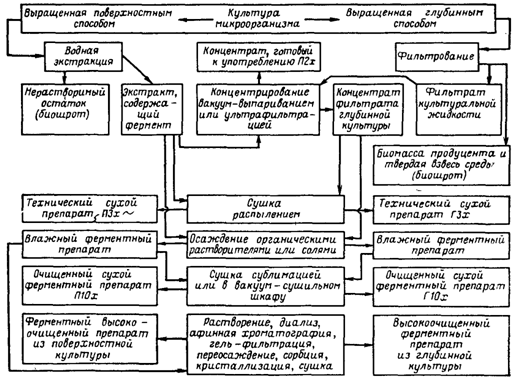
... инактивация ферментов. Из сборника 29 охлажденная жидкость по мере необходимости подается на фильтровальную установку. 1.3 Получение ферментных препаратов из культур микроорганизмов Культура микроорганизмов, выращенная поверхностным способом, и культуральная жидкость после глубинного культивирования содержат большое количество балластных веществ. Выделение и очистка ферментов – трудоёмкий и ...


0 комментариев