Навигация
Скорость образования, расходования компонента и скорость реакции
1.1 Скорость образования, расходования компонента и скорость реакции
Для практических целей важно знать скорость химических реакций. От скорости протекания реакции зависят количество вещества, получаемого в единицу времени, размеры аппарата для производства нужного продукта.
В кинетике химических реакций различают скорости образования и расходования компонентов и скорость реакции
Скоростью образования (расходования) количества данного i-того вещества (компонента) во время химической реакции или скоростью реакции Wi по данному i-тому веществу называется изменение количества этого вещества ni (в молях) в единицу времени т в единице реакционного пространства R:
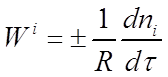
Если реакция гомогенная и протекает в объеме, то реакционным пространством является объем V (R = V) и изменение количества вещества рассматривают в единице объема.
Если реакция гетерогенная и протекает на границе раздела фаз, то реакционным пространством является поверхность S (R = S) и изменение количества вещества относят к единице поверхности.
При этом скорость расходования исходных веществ будет отрицательной (со знаком - ), так как с течением времени количество исходных веществ уменьшается.
Скорость образования продуктов реакции величина положительная (со знаком + ), так как с течением времени количество их увеличивается.
На практике наибольшее значение имеют изотермические реакции (протекающие при Т = const), происходящие в замкнутых (закрытых) или открытых системах.
Замкнутая система не обменивается веществом с окружающей средой, но энергией (теплотой, работой) она может обмениваться. Такой системе в химической технологии соответствует прерывный процесс, например, в закрытых чанах или автоклавах.
В открытой системе происходит обмен с окружающей средой не только энергией, но и веществом. Открытой системе в химической технологии соответствует непрерывный процесс в потоке. Рассмотрим скорость образования (расходования) i-того вещества в замкнутой гомогенной системе
(R = V):
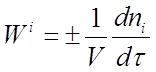 (1)
(1)
Если во время реакции V = const, то его можно внести под знак дифференциала. Так как отношение ni /V = Ci то вместо уравнения (1) получим:
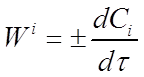 (2)
(2)
где Сi - концентрация рассматриваемого i-того вещества в данный момент времени.
Если химическая реакция формально простая и может быть записана одним уравнением, то скорости расходования исходных веществ и образования продуктов реакции зависят от стехиометрических коэффициентов перед ними, например, для реакции:
А + В = 2АВ. (3)
с учетом этого можно получить соотношение:
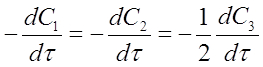
или формально
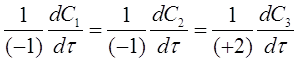
где C1 и С2 - концентрации исходных веществ А и В;
С3 - концентрация продукта реакции АВ
-1,2 - стехиометрические коэффициенты перед веществами реакции с учетом правила знаков (для исходных веществ стехиометрические коэффициенты принимаются отрицательными). С учетом уравнения (2) соотношение (4) примет вид:
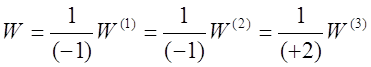 (5)
(5)
где W - скорость реакции, одинаковая для всех веществ, участвующих в данной реакции;
![]() - скорости расходования исходных веществ и образования продукта реакции. В общем виде выражение (5) запишется формулой:
- скорости расходования исходных веществ и образования продукта реакции. В общем виде выражение (5) запишется формулой:
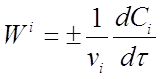 (6)
(6)
где vi - стехиометрические коэффициенты в уравнении реакции.
Таким образом, скорость реакции равна скорости расходования (образования) данного вещества реакции, деленной на его стехиометрический коэффициент с учетом принятых знаков. Она всегда положительна.
Скорость расходования исходных веществ отрицательна, а образования продуктов реакции положительна.
При изучении кинетики химических реакций обычно получают зависимость концентрации какого-либо компонента от времени τ.
Ci=f(τ).
Графическое представление изменения концентрации компонента реакции с течением времени в координатах Сi - и называют кинетической кривой. Кинетические кривые для исходных веществ и продуктов имеют вид (рисунок 1):
1 - кинетическая кривая исходных веществ; 2 - кинетическая кривая продуктов реакции
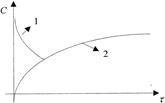
Рисунок 1 - Кинетические кривые для компонентов реакции
Если кинетические кривые мало отличаются от прямых линий, то можно для приближенной оценки определять среднюю скорость реакции:
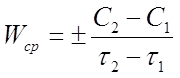
где (τ 2- τ1) - интервал времени, за который в течение реакции концентрация вещества изменяется от С1 до C2.
Похожие работы
... ; VCH3OH=10мл; [MA]0: [CO]0: [O2]0 = 5:3:2. Причины этого эффекта будут изучены в ходе дальнейших исследований. 5. Патентный поиск 5.1. Введение Данная дипломная работа посвящена изучению условий возникновения колебательного режима при окислительном карбонилировании алкинов в присутствии палладиевых катализаторов. Этот процесс представляет большой интерес, поскольку в дальнейшем позволит ...
... образом зависят от их микроструктуры. Контроль размера, распределения по размерам и морфологии отдельных зерен или кристаллитов чрезвычайно важен для получения материалов с заданными свойствами. Химические реакции в микроэмульсиях используют как один из возможных путей получения тонкодисперсных частиц. В таблице 1 приведены примеры областей, в которых используется микроэмульсионный метод получения ...
... для реализации системы бюджетирования Консультационной группы "Воронов и Максимов". Статья о проблемах выбора системы бюджетирования - в проекте "УПРАВЛЕНИЕ 3000". Бюджетный автомат Если вы решитесь на автоматизацию системы бюджетирования компании, перед вами сразу встанут вопросы: что выбрать, сколько платить, как внедрять. Примеряйте! О ЧЕМ РЕЧЬ В “Капитале” на стр. 44, 45 мы рассказали ...
... разовая) – 0,01%. 4 Содержание Введение......................................................................................................................4 Глава 1. Межпредметные связи в курсе школьного предмета химии на примере углерода и его соединений.......................................................................5 1.1 Использование межпредметных связей для формирования у учащихся ...

0 комментариев