Навигация
Химическая термодинамика
Химическая термодинамика
1. Основные понятия и законы химической термодинамики
1.1 Основные понятия
Термодинамической системой называют тело или группу тел, находящихся в энергетическом взаимодействии и мысленно или физически отделённых от окружающих тел, которые называются внешней или окружающей средой.
Классификация систем:
1) по возможности тепло- и массообмена: изолированные, закрытые, открытые. Изолированная система не обменивается с окружающей средой ни веществом, ни энергией. Закрытая система обменивается с окружающей средой энергией, но не обменивается веществом. Открытая система обменивается с окружающей средой и веществом и энергией. Понятие изолированной системы используется в физической химии как теоретическое.
2) по внутренней структуре и свойствам: гомогенные и гетерогенные. Гомогенной называется система, внутри которой нет поверхностей, делящих систему на части, различные по свойствам или химическому составу. Примерами гомогенных систем являются водные растворы кислот, оснований, солей; смеси газов; индивидуальные чистые вещества. Гетерогенные системы содержат внутри себя естественные поверхности. Примерами гетерогенных систем являются системы, состоящие из различных по агрегатному состоянию веществ: металл и кислота, газ и твёрдое вещество, две нерастворимые друг в друге жидкости.
Фаза – это гомогенная часть гетерогенной системы, имеющая одинаковый состав, физические и химические свойства, отделённая от других частей системы поверхностью, при переходе через которую свойства системы меняются скачком. Фазы бывают твёрдые, жидкие и газообразные. Гомогенная система всегда состоит из одной фазы, гетерогенная – из нескольких. По числу фаз системы классифицируются на однофазные, двухфазные, трёхфазные и т.д.
Компонент – всякое вещество, входящее в систему, которое из неё можно выделить и которое может существовать отдельно от системы. По числу компонентов системы классифицируются на однокомпонентные, двухкомпонентные, трёхкомпонентные и т.д.
Свойства системы в физической химии могут быть описаны заданием параметров системы. В качестве параметров чаще всего выступают температура (Т), давление (Р), объём (V), количество вещества (ν) и другие.
Если параметры системы постоянны, говорят, что система находится в состоянии равновесия.
Если параметры системы меняются, то в системе протекает термодинамический процесс. Процесс называют равновесным, если его можно представить как ряд последовательных равновесных состояний системы. В противном случае говорят о неравновесном процессе. Различают обратимые и необратимые процессы. Обратимым называют равновесный процесс, который может в одних и тех же условиях самопроизвольно протекать как в прямом, так и в обратном направлениях. К необратимым процессам относятся неравновесные и несамопроизвольные процессы.
Процессы могут быть: изотермическими (протекают при Т=const), изобарическими (Р=const), изохорическими (V=const), адиабатическими (протекают без теплообмена с окружающей средой). Наибольшее значение в химической термодинамике имеют изобарно-изотермические (Р,Т=const) и изохорно-изотермические (V,Т=const) процессы. Именно в таких условиях протекают все химические реакции.
1.2 Основные величины
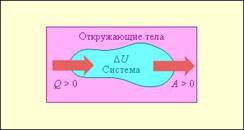
Теплота (Q) – энергия, которая передаётся одной системой другой при их взаимодействии, зависящая только от температур этих систем.
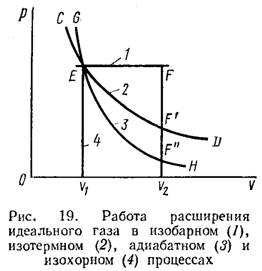
Работа (A) – энергия, передаваемая одной системой другой, зависящая от наличия силового поля или внешнего давления, под действием которого система меняет свой объём. В последнем случае говорят о работе сил расширения.
Правило знаков для теплоты и работы: теплота считается положительной, если она подводится к системе из окружающей среды (поглощённая теплота) и отрицательной в противоположном случае (отданная теплота); работа считается положительной, если она совершается системой над окружающей средой, и отрицательной, если работу совершает окружающая среда над системой.
Внутренняя энергия (U) – запас энергии системы. Включает в себя все виды энергии, связанные со строением системы, и не включает кинетическую и потенциальную энергии системы как целого. Так как абсолютных знаний о строении вещества не существует, абсолютное значение внутренней энергии найти нельзя.
Энтальпия – запас энергии системы в виде теплоты. Связана с внутренней энергией уравнением H = U + PV. Внутренняя энергия, энтальпия, теплота и работа измеряются в Дж/моль. Внутренняя энергия и энтальпия являются, а теплота и работа не являются функцией состояния системы.
Функцией состояния системы называется функция, изменение которой зависит только от начального и конечного состояний системы и не зависит от пути перехода системы из начального в конечное состояние.
Изменения термодинамических функций в химической термодинамике обозначаются по-разному. Если речь идёт о конечном (большом) изменении, то используют греческий символ ∆. Например, ∆Н, ∆U. Бесконечно малые изменения функций, являющихся функциями состояния системы, обозначают латинской буквой d (dU, dH). Если же функция не является функцией состояния системы, то её бесконечно малое изменение обозначается греческой буквой δ (δА, δQ). Изменения функций состояния системы рассчитываются как разность значений данной функции в конечном и исходном состояниях. Например,
∆Н = Н2 – Н1.
Энтропия (S) – термодинамическая функция, количественно характеризующая степень беспорядка в системе. Является функцией состояния системы, измеряется в Дж/моль∙К.
Энергия Гельмгольца (F) – функция состояния системы, характеризующая протекание химических процессов в изохорно-изотермических условиях.
Энергия Гиббса (G) – функция состояния системы, характеризующая протекание химических процессов в изобарно-изотермических условиях. Энергии Гельмгольца и Гиббса измеряются в Дж/моль.
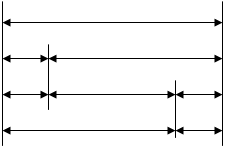
Соотношение между основными термодинамическими функциями представлено на рис.1.
Н
PV U
PV F TS
G TS
Рисунок 1 - Соотношение между термодинамическими функциями
Теплоёмкость (С) – количество сообщённой системе теплоты, отнесённое к наблюдаемому при этом повышению температуры:
С = ![]() .
.
Различают теплоёмкость при постоянном объёме СV и теплоёмкость при постоянном давлении СP:
СV = ![]() , СP =
, СP = ![]() , СP – CV = R,
, СP – CV = R,
где R = 8,314 Дж/моль∙К – универсальная газовая постоянная.
Похожие работы
... и химическим процессам, происходящим в веществе, в различных системах. Важным достижением на пути этого процесса интеграции знаний было открытие фундаментального закона природы - закона сохранения и превращения энергии. Основатель термодинамики С. Карно в своем труде "Размышления о движущей силе огня и о машинах, способах развивать эту силу" пишет: "Тепло - это не что иное, как движущая сила, ...
... газов в результате реакции. Величина Δn может иметь положительное и отрицательное значения, в зависимости от того, увеличивается или уменьшается число молей газов во время процесса. Применение первого начала термодинамики к процессам в любых системах. Закон Гесса Примем, что единственным видом работы, которая совершается системой, является работа расширения. Подставляя уравнение (II, 5) в ...
... , или термодинамическое равновесие, при котором движение частиц хаотично. Максимальная энтропия означает полное термодинамическое равновесие, что эквивалентно хаосу. Часто второе начало термодинамики преподносится как объединенный принцип существования и возрастания энтропии. Принцип существования энтропии формулируется как математическое выражение энтропии термодинамических систем в условиях ...
... в ходе реакции мало, т.е. , тогда ; . При термомеханическом описании реакции опускают , , говорят только об изменении энтальпии : Закон Гесса: тепловой эффект химической реакции протекающий или при или при не зависит от числа промежуточных стадий, а определяется лишь конечным и начальным состоянием системы. Тепловой ...
0 комментариев