Навигация
Исследование кинетики анодного поведения титанового, стального и графитового электродов в разбавленном растворе К2Сг207
3.3 Исследование кинетики анодного поведения титанового, стального и графитового электродов в разбавленном растворе К2Сг207.
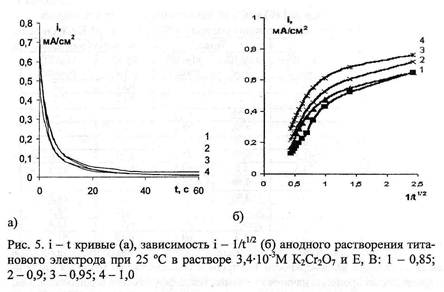
Потенциостатические исследования кинетики анодных процессов на титановом, стальном и на электроде, выполненном из фольги "Графлекс", были проведены при потенциалах, предшествующих потенциалам преимущественного выделения кислорода (рис.5).
Характер i - 1 - кривых позволяет проанализировать начальные участки спада тока в координатах i - 1/V7, с целью выяснения лимитирующей стадии процесса. То, что в начальный момент поляризации (1 - 1,5 с) зависимости i - 1/V7 не идут в начало координат, свидетельствует о протекании на границе раздела фаз электрод - раствор К2Сг207 гетерогенной химической реакции. Такой реакцией может быть конкурирующая адсорбция бихромат-ионов, молекул воды и продуктов взаимодействия бихромат-ионов с поверхностью электрода. На поверхности стального электрода в области потенциалов от 0,2 В до 0,75 В возможно протекание реакций, связанных с переходом железа в оксидное и гидроксидное состояния.
Оксиды и гидроксиды железа (П) взаимодействуют с адсорбированными бихромат-ионами, происходит восстановление Сг (VI) до Сг (III) с потреблением образующихся в реакциях, о чем свидетельствует подщелачивание приэлектродного слоя при изменении потенциалов стального электрода от 0,1 до 1,0 В (pH составляет 5,5-7,1).
На титановом электроде в интервале потенциалов от 0,9 до 1,55 В (до потенциалов выделения кислорода) возможно протекание двух процессов: образование кислородных соединений титана (IV), а также окислительно-восстановительные реакции, происходящие в хроми-хроматной адсорбированной пленке. Исходя из представлений об адсорбции перечисленных частиц на поверхности электрода, был произведен расчет величины адсорбции (ПГ) по уравнению;
Величина адсорбции (пГ) растет с увеличением электродного потенциала. Максимально наблюдаемые величины ПГЕ на стальном и титановом электродах в области потенциалов от 0,65 до 1,2 В могут быть связаны с большей гидрофильностью указанных электродных материалов по сравнению с фольгой "Графлекс". Данные результаты указывают на значительное участие молекул воды в анодных процессах на поверхностях исследуемых электродов.
С увеличением времени поляризации происходит накопление продуктов анодных реакций на поверхности электрода и соответственно меняется лимитирующая стадия процесса: начинают сказываться диффузионные ограничения. Так, анализ потенциостатических кривых в координатах i~t (рис.5, б) на отрезке времени от 1 до 5 с показал, что на титановом и стальном электродах наблюдается замедленность стадии твердофазной диффузии. Согласно представлениям, развиваемым в работах Алексеева, Колотыркина, Попова, анодное растворение металлов протекает за счет диффузии ионов металлов и диффузии ионов кислорода в пассивной пленке, образованной на поверхности электрода Преобладание одного из механизмов диффузии зависит от свойств и состава образующейся пленки. Учитывая, что раствор К2Сг207 разбавлен, и в начальный момент поляризации (1,5 - 5 с) Сг (Ш) присутствует в адсорбционной пленке в малых количествах, можно предположить, что диффузионные процессы связаны с переносом ионов титана в твердой фазе, о чем свидетельствует расчетная величина ZCQ^D, лежащая в пределах (8 - 17) - 10с. При электродном потенциале более (1,2 - 1,55) В (для различных электродных материалов) происходит преимущественное выделение кислорода, сопровождающееся повышением кислотности приэлектродного слоя. Одновременно усиливается окисление поверхности анода. Электрод, выполненный из фольги "Графлекс", обладает меньшей гидрофильностью, чем исследуемые металлические электроды, поэтому диффузионные ограничения скорости анодных процессов на графите в первую очередь связаны с окислительно-восстановительными реакциями, протекающими между анионами Сг (VT) и кислородными соединениями Сг (Ш), адсорбированными на поверхности электрода. Замедленный отвод продуктов реакций приводит к уменьшению количества бихроматионов, способных адсорбироваться на электродах. В результате снижается скорость процесса.
Анализ начальных участков гальваностатических кривых позволил рассчитать величину поляризационной емкости (Спол) анодного процесса на различных электродных материалах согласно уравнению.
Величина С лежит в пределах от 0,3 до 2,7 мФ/см2 и зависит от концентрации электролита, материала анода, плотности поляризующего тока и связана с изменением адсорбции на поверхности электрода под действием указанных факторов. Уменьшение плотности поляризующего тока приводит к снижению поляризационной емкости, что может служить косвенным подтверждением электрохимического механизма адсорбционных процессов на границе раздела фаз.
3.4 Влияние природы раствора и плотности тока на состояние поверхности изучаемых анодных материалов.
Изучение анодного поведения исследуемых материалов показало наличие на их поверхности пассивирующих пленок, которые были проанализированы с помощью микроструктурного анализа и методом вторично-ионной масс-спектрометрии (ВИМС). Согласно полученным микрофотографиям, состояние пассивирующей пленки зависит от материала электрода, плотности тока поляризации, концентрации электролита и наличия в электролите посторонних анионов (промывная вода, содержащая ионы).
Методом ВИМС показано наличие в составе поверхностной пассивирующей пленки соединений хрома различной валентности и оксидов металлов. Наибольшее содержание соединений хрома сосредоточено на поверхности электрода. По мере продвижения в глубь пленки количество соединений хрома уменьшается и к толщине пленки примерно 0,5 мкм достигает постоянного значения. При анодной поляризации электрода в промывной воде в пассивной пленке, образующейся на поверхности, наблюдается увеличение количества хрома по мере продвижения в глубь пленки. Это может быть связано с разрыхлением пассивного слоя за счет высокой растворяющей способности кислого электролита, которым является промывная вода.
Глава 4. Катодное поведение металлов и графита в разбавленных Cr-содержащих растворах.
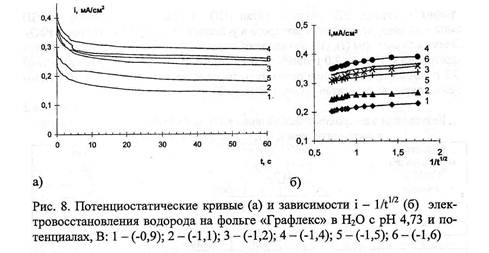
Повышение эффективности электрохимического способа очистки промывных и сточных вод от ионов Сг (VI) предусматривает изучение как анодных, так и катодных процессов в разбавленных хромсодержащих электролитах.Т. к. электровосстановление Сг (VI) на графитовом материале протекает легко, то его использование в качестве катода наиболее целесообразно. Изучались кинетические закономерности электровосстановления Сг (VI) на фольге "Графлекс" в разбавленных растворах К - Характер i, t - кривых парциального выделения водорода и электровосстановления Сг (VI) позволил проанализировать начальные участки потенциостатических кривых в координатах i - 1/л и сделать предположение о протекании химической реакции. Применительно к электровосстановлению водорода и анионов хрома это может быть адсорбция соответствующих ионов. В соответствии с уравнением (8) был произведен расчет величин адсорбции реагентов (ПГЕ). Адсорбция ионов водорода и атомарного водорода на поверхности графитового катода зависит от электродного потенциала и лежит в пределах (1,0 - 10,6) - 10"8 г-экв/см2. При наиболее отрицательном потенциале наблюдается тенденция к уменьшению, что, вероятно, связано с проникновением разрядившихся ионов водорода в глубь материала, насыщением поверхностных слоев, и как, следствие, уменьшением (ПГЕ) и скорости процесса выделения водорода. Величины (ПГЕ) ДЛЯ процесса неполного восстановления Сr (VI) на фольге "Графлекс" составляют (1,1 - 10,6) - 10"8 г-экв/см2. Они сопоставимы с результатами адсорбции СrО) 2' (17,76-10"7 г-экв/см2).
Накопление продуктов катодной реакции на поверхности фольги "Графлекс": хромихроматная пленка, водород, продукты окисления графита должно привести с течением времени к уменьшению скорости процесса. Схему катодного процесса в хромовокислом электролите можно представить совокупностью реакций:
Н20 + е - Надс + ОН
Сг3+ + ЗОН - Сг (ОН) 3
Об участии адсорбционного атомарного водорода в восстановлении Сг (VI), присутствующего на поверхности электрода в составе адсорбционной пленки, свидетельствует малое изменение рН вблизи электрода, отсутствие интенсивного выделения газа, т.е. избыток ОН'-групп, образующийся при разложении воды, связывается в Сг (ОН) 3.
Глава 5. Влияние материала электродных пар.
и режима процесса на качество электрохимической очистки разбавленных хромсодержащих электролитов. Эффективность электрохимической очистки определяется рядом факторов: материалом электродных пар, составом и концентрацией промывной воды, плотностью тока поляризации, расстоянием между электродами, температурой раствора, перемешиванием и др. Среди указанных факторов важнейшее значение имеет выбор электродной пары. При этом могут быть использованы нерастворимые и растворимые аноды.
При выборе электродного материала катода и анода необходимо учитывать перенапряжение выделения водорода и кислорода, адсорбционную способность электродов, их пассивируемость. Согласно данным, полученным ранее на кафедре ТЭП ТИ СГТУ, и приведенным в настоящей работе, результаты по удалению электрохимическим способом загрязняющего компонента зависят от расстояния между электродами - 1. При увеличении расстояния более 5 см качество очистки снижается: оптимальным является 1, равное 1-2 см (таблицы 2,3). Метод потенциодинамических кривых при изучении катодных и анодных процессов в слабокислых разбавленных хромсодержащих электролитах позволил рекомендовать в качестве катода стальной и графитовый электроды (фольга "Графлекс", электроугольный графит). В качестве анодного материала представляло интерес опробовать графит, титан, свинец.
Изучение влияния материала анода, катода и комбинации электродных пар, а также рН раствора, плотности тока на катоде и аноде, температуры электролита на качество очистки промывной воды и разбавленных растворов электролитов от ионов Cr (VI) с нерастворимыми анодами позволило выделить как наиболее перспективные пары: сталь - свинец (I).
Влияние материала электродных пар проявляется в различной скорости электровосстановления Cr (VI) на железе и графите и в воздействии выделяющегося кислорода на поверхность катода и, соответственно, на скорость перехода Cr (VI) в соединения низшей валентности. Можно предположить, что выделяющийся кислород в небольшом электродном пространстве легко достигает поверхности катода, взаимодействует с ней, образуя оксиды и анионы НО, которые свою очередь, участвуют в восстановлении Cr (VI) до Сr (Ш). Кроме того, согласно литературным данным, кислород является стимулятором процесса электровосстановления водорода и наводороживания материала. Накопление адсорбированного водорода на поверхности катода также способствует ускорению разряда Cr (VI) до СП). Рассматривая с данных позиций влияние материала анода на качество очистки хромсодержащих растворов, можно сказать следующее: наибольшие токи, связанные с выделением кислорода, наблюдаются на свинцовом электроде в растворе бихромата калия изучаемых концентраций. И именно для электродной пары, где анодом является свинец, получены лучшие результаты электрохимической очистки промывных вод и модельных растворов. Повышение скорости выделения кислорода на титановом электроде в 3,4-1М K2Gr207 также приводит к повышению качества электрохимической очистки. Следует отметить, что повышение температуры не оказывает значительного влияния на качество очистки (таблица 3). Данное явление можно объяснить тем, что повышение температуры, с одной стороны, увеличивает доставку реагирующих частиц к поверхности электрода и отвод продуктов реакции, с другой стороны, уменьшается адсорбция водорода, снижается выделение кислорода. Следовательно, увеличение температуры нецелесообразно.
Проведение электролиза с нерастворимыми анодами позволило рекомендовать в качестве катодов сталь или электрод, изготовленный из фольги "Графит", в качестве анода - свинец, титан. При этом очистка загрязненных вод может быть проведена до ПДК (Cr (VI) = 0,05 мг/л), или до концентраций Cr (VI), которое не ухудшает качество промывки деталей при замкнутом обороте воды.
Использование растворимых анодов в процессе электрохимической очистки позволяет получить хорошие результаты при содержании загрязняющего компонента - 0,1 г-ион/л (таблица 4,5). Однако значительный расход анодов и, как следствие, шламообразование, а также большое солесодержание ограничивают применение электролиза с растворимыми анодами (электрокоагуляция).
Основные выводы:
1. Установлено, что на поверхности металлических (сталь, титан, свинец) и графитовых электродов в условиях катодной и анодной поляризации и без тока протекают адсорбционные процессы, образующие величину стационарного потенциала электрода. Сформированные адсорбционные слои определяют скорость электродных процессов. Величина ГЕ зависит от материала электрода, электродного потенциала, определяется конкурирующей адсорбцией бихромат-ионов, молекул воды, выделяющегося кислорода и составляет для катодного процесса (1,1 - 10,6) экв/см, для анодного процесса (0,9 - 96).
2. Изучена кинетика анодного растворения стального, титанового, свинцового и графитовых материалов в разбавленных хромсодержащих электролитах, выявлены области потенциалов и соответствующие им токи, представляющие интерес для использования указанных электродов в процессе электрохимической очистки:
для проведения электролиза с нерастворимыми анодами рекомендуется использовать свинцовый и титановый электроды, работающие при плотностях тока не менее (3,0 - 6,0) А/дм2, обеспечивающих интенсивное выделение кислорода;
установлено, что для проведения электрокоагуляционной очистки хромсодержащих промывных вод концентрация Сг (VI) не должна превышать 0,85-10 М, плотность поляризующего тока изменяется от 3,0 до 20 А/дм2. Для интенсификации процесса можно использовать повышение температуры раствора до 50 °С.
3. Методом ВИМС и микроструктурным анализом поверхности подтверждено наличие пассивирующих пленок на поверхности анода, содержащих в своем составе оксидные соединения хрома различной валентности и оксидов металлов.
4. Установлено, что для повышения качества электрохимической очистки необходимо подбирать оптимальные пары электродных материалов, обеспечивающих интенсивное выделение водорода и кислорода.
5. Разработаны технологические параметры для проведения электрохимической очистки хромсодержащих промывных вод с нерастворимыми анодами:
катод - графит (электроугольный графит, фольга "Графлекс"); анод - свинец или титан;
катод - сталь, анод - свинец.
Режим электролиза: iK=iA= 2 А/дм2; t=20 - 25 °С; t=50 мин; расстояние между электродами 2-5 см.
Список публикаций по теме диссертации
1. Шишова М.А. Изучение анодного растворения сплава Fe-Ni методом хронопотенциометрии / Н.Д. Соловьева, В.Н. Целуйкин, М.А. Шишова // Современные проблемы теоретической и экспериментальной химии: Материалы докладов III Всерос. конф. молодых ученых/СГТУ. Саратов, 2001. С.262-263.
2. Шишова М.А. Хроноамперометрическое исследование анодного растворения сплавов Fe-Ni / Н.Д. Соловьева, В.Н. Целуйкин, М.А. Шишова // Перспективные полимерные композиционные материалы. Альтернативные технологии, переработка: Доклады Междунар. конф. "Композит - 2001"/СГТУ Саратов, 2001. С.273-276.
3. Шишова М.А. Влияние природы материала анода на эффективность электрохимической очистки сточных вод от катионов тяжелых металлов / Н.Д. Соловьева, М.А. Шишова // Современные электрохимические технологии: Сб. статей по материалам Всерос. конф. / СГТУ. Саратов, 2002. С.224-228.
Похожие работы
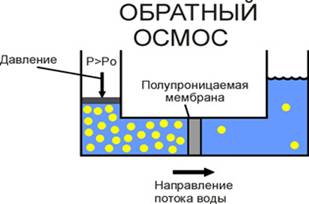
... для этого реагентный метод или мембранные методы обессоливания (обратный осмос, электродиализ). По технологическим процессам и, соответственно, применяемому оборудованию, методам очистки сточных вод гальванического производства можно дать следующую классификацию: · механические / физические (отстаивание, фильтрация, выпаривание); · химические (реагентная обработка); · коагуляционно ...
... в нашей стране с 70-х годов, ее использование для решения экологических проблем гальванотехники ранее не приводилось. В тоже время этот метод является достаточно универсальным, высокоэффективным, экологически безопасным и достаточно экономичным. [8, 20] Проблема с осаждения ионов тяжелых и цветных металлов заключается в том, что оптимальное значение рН для различных ионов не одинаково. Так, ...
... при реагентном способе очистки, по предлагаемой технологии извлекаются в виде элюатов и направляются на повторное использование. Таблица 3.1. Показатели очистки хромсодержащих сточных вод по предлагаемой технологической схеме Наименование Единицы Показатели Показатели ГОСТ Степень ингредиентов измерения до очистки после ...
... Затем детали промывают в горячей проточной воде, производят промывку и активацию. В ванне каскадной промывки происходит противоточная двухступенчатая холодная промывка. Для осаждения цинковых покрытий применяют различные электролиты: кислые, цианистые, аммиакатные, цинкатные и др. В аммиакатном электролите цинк находится в виде комплексных катионов. Аммиакатные соединения цинка получаются при ...








0 комментариев