Навигация
Оборудование и реактивы: Штатив с пробирками, раствор серой кислоты (1:5), цинк (гранулы), медная проволока, шпатель
1. Оборудование и реактивы: Штатив с пробирками, раствор серой кислоты (1:5), цинк (гранулы), медная проволока, шпатель.
Ход работы: В пробирку на 1/3 объема наливают раствор серной кислоты и помещают одну гранулу цинка. Наблюдают выделение газа водорода. Далее дотрагиваются до цинка медной проволокой. Реакция идет более энергично, выделяются более крупные пузырьки газа. Написать соответствующие уравнения реакций, объяснить наблюдаемые явления.
Утилизация. Использовать раствор серной кислоты в следующем опыте.
2. Оборудование и реактивы: Штатив с пробирками, раствор серой кислоты (1:5), цинк (гранулы), раствор сульфата меди массовой долей 5 %.
Ход работы: В пробирку наливают раствор серной кислоты и помешают гранулу цинка. Наблюдают выделение газа водорода. Затем в эту пробирку приливают раствор сульфата меди. Идет бурное выделение пузырьков газа. Написать соответствующие уравнения реакций, объяснить наблюдаемые явления.
Утилизация: Оставить содержимое пробирки до полного обесцвечивания раствора: Zn + CuSO4 ® Cu + ZnSO4. Отделить фильтрованием кусочек цинка с осевшей на нем медью. Промыть, высушить медь и цинк. В фильтрат (H2SO4 и ZnSO4) добавить оксида, гидроксида или карбоната цинка до прекращения их растворения в кислоте. Избыток твердых веществ отделить от раствора сульфата цинка и использовать реактивы в лаборатории.
3. Оборудование и реактивы: Химический стакан на 200 мл, крышка со вставленными в нее электродами (медным и цинковым), гальванометр, раствор серной кислоты (1:5).
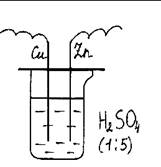
Рис. 29. Электрохимическая коррозия цинка в кислой среде.
Ход работы: В стакан наливают раствор серной кислоты и накрывают крышкой с электродами (медный и цинковый), соединяют электроды с гальванометром, стрелка гальванометра отклоняется. Описать все происходящие процессы, написать уравнения реакций.
Утилизация. Раствор серной кислоты использовать многократно.
4. Оборудование и реактивы: Два химических стакана, медный и цинковый электроды, марлевый жгутик, гальванометр, растворы хлорида меди и хлорида цинка (10 %.)
Ход работы: В один стакан наливают 10 % раствор хлорида меди, в другой – раствор хлорида цинка. В первый стакан помещают медный электрод, а во второй – цинковый. Соединяют их гальванометром. Растворы солей соединяют марлевым жгутиком, смоченным электролитом. Описать все происходящие процессы. Написать уравнения реакций.
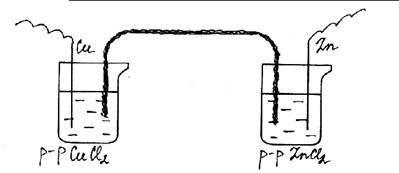
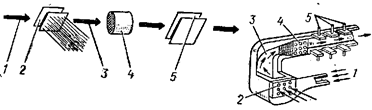
Рис. 30. Медно-цинковый гальванический элемент. Электрохимическая коррозия цинка.
Примечание: Марлевый жгутик не должен касаться электродов, для этого оба конца жгутика помещают в стеклянные трубки.
Утилизация. Растворы сливают в соответствующие склянки и используют многократно.
5.Оборудование и реактивы: Железный нож, наждачная бумага, разбавленные растворы хлорида натрия, красной кровяной соли, фенолфталеин, стакан, пипетка.
Ход работы: Железный нож очищают наждачной бумагой. Пипеткой нанести на нож несколько капель раствора-индикатора, состоящего из хлорида натрия и красной кровяной соли, смешанных в соотношении объемов 10:1, и нескольких капель фенолфталеина. Через некоторое время появляется синяя окраска в центре капли и малиновая на поверхности капли. Дать объяснение происходящим процессам, написать уравнения реакций.
Утилизация: Раствор-индикатор с красной кровяной солью использовать многократно.
Опыт № 6. Ингибирование процесса коррозии в кислой среде
Оборудование и реактивы: Штатив с пробирками, шпатель, раствор серной кислоты (1:5), уротропин (порошок или в таблетке), железные гвозди, наждачная бумага, спирт, вата.
Ход работы: В две пробирки наливают до половины раствор серной кислоты. В первую пробирку помещают 1/3 таблетки уротропина и, помешивая, растворяют ее. Вторая пробирка – контрольная. В каждую пробирку опустить по хорошо очищенному железному гвоздю. В пробирке с ингибитором начавшееся выделение водорода быстро прекращается. В контрольной пробирке водород выделяется энергично.
Утилизация. Растворы использовать многократно.
Опыт № 7. Защита от коррозии покрытием оксидной пленкой
Оборудование и реактивы: Штатив с пробирками, железный гвоздь, концентрированная азотная кислота (ρ=1,48 г/см3), пинцет, раствор серной кислоты (1:5), спирт, вата, наждачная бумага.
Ход работы: Тщательно очищенный наждачной бумагой и обезжиренный спиртом гвоздь помещают на 1-2 мин. в пробирку с холодной концентрированной азотной кислотой. За это время железо пассивируется - покрывается тонким слоем из оксидов железа. Гвоздь промывают в воде и опускают в раствор серной кислоты. Выделение водорода не наблюдается. Для контроля в раствор серной кислоты опускают гвоздь, не обработанный концентрированной азотной кислотой. Происходит выделение водорода.
Техника безопасности. Наливать концентрированную азотную кислоту в пробирку под тягой.
Утилизация. По окончании опыта слить кислоты в соответствующие емкости и использовать многократно.
Опыт № 8. Катодная защита металлов от коррозии
Оборудование и реактивы: Выпрямитель, штатив с лапкой, прокладки резиновые, стакан, U-образная трубка, железные стержни, наждачная бумага, 1 % раствор серной кислоты, разбавленный раствор красной кровяной соли.
Ход работы: В U-образную трубку наливают 1 % раствор серной кислоты с добавкой красной кровяной соли до слабо желтой окраски. Опускают в каждое колено трубки железные стержни – электроды и подсоединяют их к источнику постоянного тока при напряжении 10-12 В. Быстрое посинение наблюдается у стержня, соединенного с положительным полюсом источника тока. А железный стержень, соединенный с отрицательным полюсом (катодом), предохраняется от коррозии (отсутствует или слабо представлена синяя окраска). Объяснить наблюдаемые явления, выразить процессы уравнениями реакций.
Техника безопасности. С электроприбором работать, не касаясь оголенных проводников.
Утилизация. Раствор из U-образной трубки слить в нейтрализатор.
Опыт № 9. Коррозия железа
Оборудование и реактивы: 5 стаканов на 50 мл, 5 лабораторных пробирок, 5 железных гвоздей, вода дистиллированная, раствор хлорида натрия, раствор гидроксида натрия, медная и цинковая проволока.
Ход работы: Поместить железный гвоздь в пробирку, наполнить ее доверху водой и опрокинуть в стакан с водой. Таким же образом заготовить другие пробирки с гвоздями, но в место чистой воды в пробирки и в сосуды, в которые они будут опрокинуты, налить раствор хлорида натрия. В одном случае к этому раствору добавить немного раствора гидроксида натрия. К одному гвоздю заранее прикрепить медную проволоку, к другому - полоску или проволоку цинка. Примерно через сутки наблюдать процесс коррозии железного гвоздя и цинковой полоски. Объяснить наблюдаемые явления. Сравнить результаты опытов. Написать уравнения реакций.
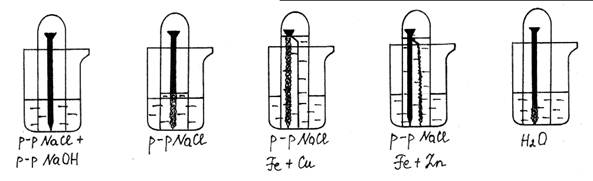
Рис. 31. Электрохимическая коррозия железа.
Утилизация. Все растворы из стаканов сливают в раковину, кроме раствора с соединениями цинка, который помещают в нейтрализатор.
ЛАБОРАТОРНАЯ РАБОТА № 3
ТЕМА: “МЕТАЛЛЫ ГЛАВНЫХ ПОДГРУПП I-III ГРУПП”
Опыт № 1. Горение кальция
Оборудование и реактивы: Плоскогубцы, фильтровальная бумага, спиртовка, спички, напильник, кальций.
Ход работы: Взять кальций плоскогубцами и очистить его при помощи фильтровальной бумаги от масла. Зажечь спиртовку. В правую руку взять напильник и сделать несколько надрезов по кусочку кальция прямо над пламенем спиртовки. Порошок кальция горит, ярко вспыхивая: 2Ca + O2 ® 2CaO.
Техника безопасности. По окончании опыта напильник и все остатки после очистки кальция поместить в кристаллизатор с водой.
Опыт № 2 . Взаимодействие оксида кальция с водой
Оборудование и реактивы: Химический стакан, воронка, оксид кальция, вода дистиллированная.
Ход работы: Кусочки заранее прокаленного и охлажденного оксида кальция поместить на дно химического стакана. Закрыть стакан воронкой и прилить воду. Идет бурная экзотермическая реакция. По окончании взаимодействия в стакан добавляют несколько капель раствора фенолфталеина.
Техника безопасности. Реакция экзотермическая, сопровождается сильным разогреванием раствора, возможно разбрызгивание горячей щелочи. Поэтому воду в стакан приливают через воронку: CaO + H2O ® Ca (OH)2 + Q.
Утилизация. Поместить щелочной раствор в емкость–нейтрализатор.
Опыт № 3. Качественные реакции на ионы калия, натрия, бария, кальция
Оборудование и реактивы: Спиртовка, спички, пробка со вставленной в нее спиралью от электроплитки, кристаллические хлорид калия, натрия, кальция, бария, раствор соляной кислоты (1:1).
Ход работы: Спираль обрабатывают раствором соляной кислоты. Затем вносят спираль в пламя спиртовки и держат до полного выгорания примесей. Вносят спираль в кристаллическую соль, захватывают спиралью кристаллы соли и вносят в пламя спиртовки. Пламя окрашивается в различные цвета: катион калия дает фиолетовый цвет, катион натрия – желтый, катион кальция – красный, катион бария – зеленый. Использовать для каждого анализа чистую нихромовую спираль.
Техника безопасности. Соблюдать правила работы со спиртовкой, выполнять действия в вытяжном шкафу.
Опыт № 4. Устранение жесткости воды
Оборудование и реактивы: Пробирки, спиртовка, спички, пробиркодержатель, вода дистиллированная, разбавленный раствор соды (5-10%), известковая вода, кристаллические хлориды кальция и магния, жесткая вода.
Для приготовления воды с постоянной жесткостью необходимо в дистиллированной воде растворить хлориды кальция и магния или любые другие соли кальция и магния (примерно, 1% растворы).
Воду с временной жесткостью готовят так: через свежеприготовленную и прозрачную известковую воду пропускают углекислый газ до полного растворения выпавшего осадка карбоната кальция. В растворе будет содержаться гидрокарбонат кальция. Этот раствор готовят непосредственно перед демонстрацией опытов.
Ход работы: Устранение карбонатной (временной) жесткости:
а) кипячение, катионы кальция осаждается в виде карбоната:
Ca2+ + 2HCO3- ® CaCO3¯ + H2O + CO2.
б) добавление известковой воды:
Ca (HCO3)2 + Ca(OH)2 ® 2CaCO3¯ + 2 H2O.
Устранение некарбонатной жесткости. Добавить к жесткой воде раствор соды:
CaCl2 + Na2CO3 ® CaCO3¯ + 2 NaCl;
MgSO4 + Na2CO3 ® MgCO3¯ + Na2SO4.
Рассмотреть другие способы устранения жесткости воды. Выразить процессы уравнениями реакций.
Техника безопасности. При кипячении жесткой воды: а) сначала осторожно прогреть всю пробирку, б) затем прогреть всю воду, но не до кипения, в) довести до кипения верхнюю часть жидкости. Отверстие пробирки направить в сторону от себя и учеников. Все растворы слить в раковину, в них нет токсичных веществ.
Опыт № 5. Механическая прочность оксидной пленки алюминия
Оборудование и реактивы: Спиртовка, спички, стеклянная трубочка, штатив, алюминиевая проволока.
Ход работы: В лапке штатива закрепляют алюминиевую проволоку, вставленную в стеклянную трубочку. Так как теплопроводность стекла небольшая, то все тепло будет “концентрироваться” на металле. Нагревают проволоку в пламени спиртовки. Алюминий плавится внутри оксидной пленки.
Техника безопасности. Соблюдать правила работы со спиртовкой.
Похожие работы
... инертны и практически не взаимодействуют ни с какими простыми и сложными веществами. Исключение составляет аморфный кремний, реагирующий с фтором. При нагревании углерод и кремний взаимодействуют с галогенами, с элементами подгруппы серы, азотом, водородом и многими металлами. В последнем случае образуются соединения, называемые карбидами и силицидами. С углеродом и кремнием взаимодействуют ...
... разовая) – 0,01%. 4 Содержание Введение......................................................................................................................4 Глава 1. Межпредметные связи в курсе школьного предмета химии на примере углерода и его соединений.......................................................................5 1.1 Использование межпредметных связей для формирования у учащихся ...
... (вода, спирты, аммиак) за счет притяжения разноименных зарядов. Прочность водородной связи существенно (~20 раз) меньше, чем ионной или ковалентной связи. Билет №4. Классификация химических реакций в неорганической химии. Классификация по составу исходных веществ и продуктов реакции. Реакции соединения — из нескольких веществ (простых или сложных) образуется сложное вещество: Реакции ...
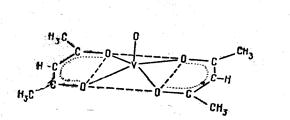
... подгрупп одной группы — химические антиподы: для одних должны быть более характерны свойства металлов, а для других — неметаллов. Но при сравнении членов обеих подгрупп можно заметить, что «противоположности» сближаются. У элементов побочной подгруппы все более усиливаются свойства неметаллов, характерные для главной подгруппы, и наоборот. Ванадий в этом отношении служит примером. В высшей ...


0 комментариев