Навигация
Моль (конц.) (по условию)
1 моль (конц.) (по условию)
Vm=22,4л/моль
2 моль
![]() 1 2 2 Me0 +2
1 2 2 Me0 +2![]()
![]() Me 2+
Me 2+
![]() 2 1 2 NO3— + 2Н+ +
2 1 2 NO3— + 2Н+ + ![]()
![]() NO20+ H2O
NO20+ H2O
![]() Me0 + 2NO3— + 4Н+ Me 2+ +2NO2 0 + 2H2O
Me0 + 2NO3— + 4Н+ Me 2+ +2NO2 0 + 2H2O
+ 2NO3— +2NO3—
в-ль; ок-е
ок-ль; в-е
3) ![]() (NO2) =
(NO2) = ![]()
4) ![]() ;
; ![]() (Me) =
(Me) = ![]() = 0,0025 моль
= 0,0025 моль
5) M(Me) = ![]()
Этот металл – медь (валентность – II), выделяется на катоде из растворов солей, с HNO3 (конец) реагирует с выделением NO2 , что соответствует условию задачи).
Хлорид металла - CuCl2 – хлорид меди (II)
6) m(CuCl2) = ![]() (CuCl2) M(CuCl2)
(CuCl2) M(CuCl2)
![]() (CuCl2) =
(CuCl2) = ![]() (Cu) = 0,0025 моль
(Cu) = 0,0025 моль
m(CuCl2) = 0,0025 моль 135 г/моль = 0,34г
Ответ: CuCl2 ; m(CuCl2) = 0,34г
Задача № 9
1000г 5,1% - ного раствора нитрата серебра подвергнуто электролизу, при этом на катоде выделилось 10,8г вещества. Затем в электролизер добавили 500г 13,5% вещества. Затем в электролизер добавили 500г 13,5% -ного раствора хлорида меди (II). Полученный раствор снова подвергли электролизу до выделения на аноде 8,96л газа (н.у.). Определите массовые доли веществ в конечном растворе.
Решение
mр-ра Ag NO3=1000г
= 5,1%
m(Ag) = 10,8г
mр-ра (CuCl2)=13,5%
![]()
V(Cl2) = 8,96л
н.у.
(в-в) -?
раствор
1) Ag NO3 = Ag ++ NO3–
![]() (H2O)
(H2O)
![]() 4 4 1 Ag+ +1
4 4 1 Ag+ +1![]() Ag 0
Ag 0
1 4 2H2O- 4![]() O2 0 + 4H+
O2 0 + 4H+
![]() 4Ag + + 2 H2O 4Ag 0 +O20 + 4H+
4Ag + + 2 H2O 4Ag 0 +O20 + 4H+
+ 4NO3— + 4NO3—
![]() на катоде : Ag +, H2O
на катоде : Ag +, H2O
на аноде : NO3–, H2O
![]() mр-ра = 1000г
mр-ра = 1000г
![]() m=10,8
m=10,8
ίm= 10,8
4Ag NO3 + 2H2O = 4Ag ↓ + O2↑ + 4HNO3 (1)
раствор М=108г/моль
М=170г/моль
4 моль 4моль
2) ![]() (Ag) =
(Ag) = ![]()
3) ![]() (AgNO3) =
(AgNO3) = ![]() (Ag) = 0,1моль
(Ag) = 0,1моль
4) ![]() (AgNO3) =
(AgNO3) = ![]()
5) ![]() =
= ![]() (AgNO3) –
(AgNO3) – ![]() (AgNO3) = 0,3моль – 0,1моль = 0,2моль
(AgNO3) = 0,3моль – 0,1моль = 0,2моль
Значит после реакции (1) в растворе остается 0,2моль AgNO3
6) Избыток AgNO3 в растворе выступит в реально с добавленным раствором
CuCl2.
mр-ра = 500г
![]()
![]() = 13,5%
= 13,5%
2AgNO3 + CuCl2 = 2AgCl ↓ + Cu(NO3)2 (2)
2моль М=135г/моль
1моль
7) По условию, при электролизе оставшегося раствора на аноде выделился газ
V=8,96л (н.у.)
раствор
CuCl2 = Cu2+ +2Cl–
(H2O)
![]() 1 2 2 Cu2+ +2
1 2 2 Cu2+ +2![]() Cu0
Cu0
![]() 1 2 2 Cl–- 2
1 2 2 Cl–- 2![]() Cl20
Cl20
![]() 2Cl– + Cu2+ Cl2 0 +Cu0
2Cl– + Cu2+ Cl2 0 +Cu0
![]()
![]() на катоде : Cu2+, H2O
на катоде : Cu2+, H2O
на аноде : Cl–, H2O
ί V = 8.96л
CuCl2 = Cu↓ + Cl2↑ (3)
(H2O – раствор) Vm=22,4г/моль М
Похожие работы
... пособие по прикладной химии «Задачи по теоретическим основам химической технологии», составленное по материалам представленной работы. 3. Методика решения задач по теоретическим основам химической технологии Одна из главных задач химической науки и промышленности - получение необходимых человеку веществ (продуктов, материалов). Поэтому большинство учебных химических задач снизано с ...
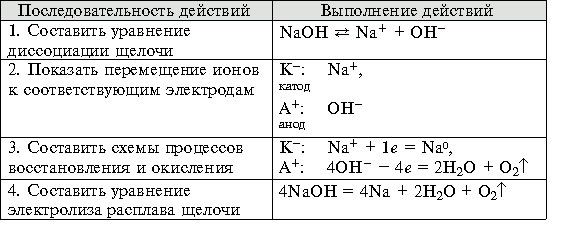
... . - Формирование навыков техники выполнения эксперимента, умения решать расчетные и качественные задачи, составлять уравнения химических реакций, протекающих при электролизе растворов и расплавов электролитов.- Воспитание самостоятельности, организованности, формирование умения работать в группе, развитие творческих способностей, логического мышления, внимания, памяти. Оборудование: компьютер, ...
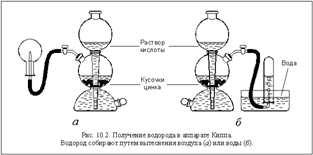
... его с кислородом или воздухом). Глава 3. Методические разработки по "Водород. Кислоты. Соли" Цели урока: Обучающие: создать условия для обобщения и систематизации знаний учащихся по теме: «Водород. Кислоты. Соли», продолжить формировать умение классифицировать неорганические вещества; закрепить основные понятия «оксиды», «кислоты», «соли», «индикатор»; уметь выделять главное. Развивающие: ...
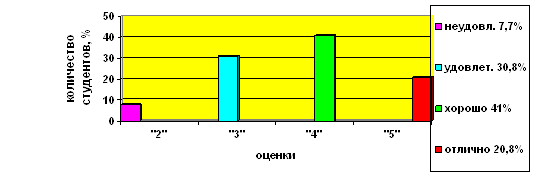
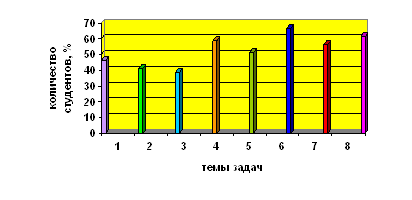
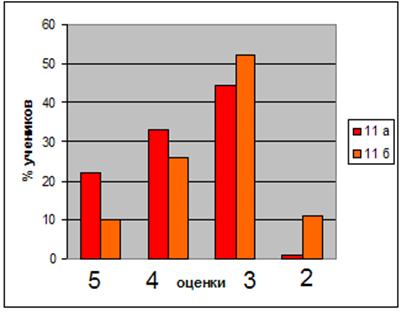
... учащихся Диаграмма 2. Динамика успеваемости и качества обучения Таким образом, можно сделать вывод, что предложенная в работе гипотеза, что разработка и реализация новых методических подходов к изучению темы «Бериллий» позволят заметно повысить уровень знаний, научной культуры, уверенности в своих способностях школьников нашла свое подтверждение в результате наших исследований. ЛИТЕРАТУРА ...




0 комментариев