Навигация
Молекулярно-генетичні маркери раку молочної залози у осіб різних вікових груп
Рассі Хоссейн
УДК 616.19-006.6+575.224.4Молекулярно-генетичні маркери раку молочної залози у осіб різних вікових груп
03.00.15-генетика
Автореферат
дисертації на здобуття вченого ступеня
кандидата біологічних наук
Київ-2008
Дисертацією є рукопис.
Робота виконана в Національній медичній академії післядипломної освіти імені П. Л. Шупіка (м. Київ) МОЗ України і в Національному інституті генетичної інженерії та біотехнології (м. Тегеран) Міністерства науки і дослідницьких технологій Ісламської республіки Іран.Науковий керівник: доктор медичних наук, професор член-кореспондент АМН України Горовенко Наталія Григорівна, Національна медична академія післядипломної освіти імені П.Л. Шупика, завідувач кафедри медичної генетики
Офіційні опоненти: доктор біологічних наук, професор Дьоміна Емілія Анатоліївна, Інститут експериментальної патології, онкології і радіолобіології імені Р.Є. Кавецького НАН України, провідний науковий співробітник відділу радіобіології;
доктор медичних наук, професор Поліщук Людмила Захарівна, Інститут раку МОЗ України, старший науковий співробітник відділу лікарської терапії та малоінвазивної хірургії
Захист відбудеться «__3_____» ______ квітня ________2008 року
о 14 годині на засіданні спеціалізованої вченої ради Д.26.562.02 в Науковому центрі радіаційної медицини АМН України (04050, м. Київ, вул. Мельникова, 53).
З дисертацією можна ознайомитись у бібліотеці Наукового центру радіаційної медицини АМН України (04050, м. Київ, вул. Мельникова, 53).
Автореферат розісланий «__01____»_______березня ______2008 р.
Вчений секретар спеціалізованої вченої ради Г.В. Стефанович
ЗАГАЛЬНА ХАРАКТЕРИСТИКА РОБОТИАктуальність теми. Рак молочної залози (РМЗ) і в Ірані, і в Україні, так само як і в більшості країн світу, займає перше місце в структурі захворюваності злоякісними новоутвореннями у жінок. Статистичні дані останніх років свідчать про неухильне зростання захворюваності і смертності від раку молочної залози в різних країнах (Parkin D.M. et al., 2005). За даними Національного канцер-реєстру України за 2004 рік в Україні злоякісні пухлини молочної залози були виявлені з частотою 38,3 на 100 тис. жіночого населення, стандартизований показник смертності становив 17,3 на 100 тис. (Бюлетень Національного канцер-реєстру України, №7, 2006). Ініціацію розвитку пухлин пов'язують з накопиченням мутацій, які виникають як у ядерній, так і у мітохондріальній ДНК ( Zhu W. et al., 2005; Czarnecka A.M. et al., 2006). Для носіїв мутацій гену BRCA1/2 ризик розвитку РМЗ протягом життя збільшується у десятки разів на відміну від популяційної частоти (Thompson D., Easton D., 2004; Nelson H.D., 2005). Близько 2% населення Європи схильні до розвитку РМЗ тільки за рахунок мутацій 185delAT і 5382insC у гені BRCA1 і 6174delT в гені BRCA2 (Sokolenko A.P. et al., 2006;). Найбільша мутація, що часто зустрічається в мітохондріальній ДНК (делеція мтДНК4977), виявляється у багатьох типах пухлин, включаючи РМЗ, але також зустрічається і в нетрансформованій тканині (Dani M.A. et al., 2004). В світі інтенсивно вивчається спектр мутацій в генах BRCA, який різниться між окремими популяціями. Знання спектру мутацій, характерного для країни або регіону, дозволяє за допомогою ДНК-діагностики виявляти групи ризику розвитку захворювання та визначати прогноз захворювання. Важливим для уточнення ролі мутацій у генах BRCA є порівняння їх частот у хворих на РМЗ різних вікових груп в різних популяціях. Ні в Україні, ні в Ірані роботи по визначенню спектру мутацій у генах BRCA1 та BRCA2 та у мітохондріальній ДНК ще не проводились.
Не всі групи хворих на РМЗ можуть бути обстежені за життя, тому для ретроспективного сімейного аналізу часто буває необхідно провести молекулярно-генетичні дослідження біологічного матеріалу пацієнток, який знаходиться в архіві патологоанатомічного відділення. Використання архівного патологоанатомічного матеріалу дозволяє проводити цілеспрямовані ретроспективні генетичні дослідження навіть при неможливості обстеження самої пацієнтки, проте до теперішнього часу не існує оптимальної методики виділення ДНК з тканин пухлин молочної залози, що зафіксовані у парафінових блоках, для подальшого аналізу ДНК і виявлення мутацій (Inoue T. et al., 1996, Bernstein J.L. et al., 2002, Cooper M. et al., 2004). В той же час, ідентифікація мутацій важлива не тільки для хворих на РМЗ пробандів, але й для їх родичів, у яких ще не виникли або не діаґностовані пухлини. Уважне відношення до стану молочної залози у родичок пробандів з мутаціями у генах BRCA1 та BRCA2 дозволяє набагато раніше виявити і видалити пухлину, що покращує прогноз на майбутнє.
Зв’язок роботи з науковими програмами, планами, темами. Робота виконана в рамках наукової комплексної теми кафедри медичної генетики Національної медичної академії післядипломної освіти імені П.Л.Шупика «Визначення ролі ендогенних та екзогенних факторів у виникненні та перебігу генної і хромосомної патології на різних етапах онтогенезу» (номер державної реєстрації 0101U000231, 2001-2005р.р.), та НДР, що фінансується МОЗ України «Розробка технології ефективного лікування раку молочної залози на основі використання імуногістохімічних та генетичних маркерів», (номер державної реєстрації 0106U002501, 2006-2008 р.р.), гранту Міністерства науки і дослідницьких технологій Ісламської республіки Іран № 13545, 2005 р.
Мета роботи - визначити можливість та доцільність використання мутацій в генах ВRCA1, ВRCA2 та мітохондріальної ДНК у якості молекулярно-генетичних маркерів ризику виникнення раку молочної залози у жінок різних вікових груп з Ірану і України.
Задачі дослідження:
1. Провести клініко-генеалогічне дослідження у пацієнток з раком молочної залози для визначення поширеності сімейного та несімейного раку.
2. Провести аналіз даних офіційної статистики Ірану та України щодо захворюваності на рак молочної залози та визначити відносний ризик розвитку цієї патології для жінок в залежності від віку.
3. Визначити оптимальний спосіб видалення парафіну з гістологічних зрізів пухлин молочної залози та способів виділення ДНК та провести порівняльну оцінку ефективності виявлення мутацій в генах ВRCA1/2 і мтДНК методом полімеразної ланцюгової реакції.
4. Визначити поширеність мутацій в генах ВRCA1/2 у пацієнток з раком молочної залози з Ірану і України в залежності від віку пацієнток, сімейного характеру досліджуваної патології.
5. Визначити частоту мутацій в мтДНК в крові і тканині пухлини молочної залози у пацієнток з Ірану.
Об’єкт дослідження – молекулярно-генетичні маркери ризику розвитку раку молочної залози у осіб різного віку.
Предмет дослідження – клініко-генеалогічні та молекулярно-генетичні маркери ризику розвитку раку молочної залози в залежності від віку жінок.
Методи дослідження – клініко-генеалогічний, молекулярно-генетичні, статистичні.
Наукова новизна одержаних результатів. В роботі вперше показана поширеність сімейного та несімейного раку молочної залози у жінок з Ірану. Вперше одержано дані про частоту мутації 5382insC і 185delAG в гені BRCA1 та 6174delT в гені BRCA2 у хворих на рак молочної залози з Ірану та України. Вперше визначено частоту мутацій у мтДНК в крові і тканині пухлини молочної залози у пацієнток з РМЗ з Ірану. Встановлено вірогідну асоціацію досліджених молекулярно-генетичних маркерів з виникненням РМЗ у осіб різних вікових груп.
Практичне значення одержаних результатів. Доведено, що для молекулярно-генетичних досліджень матеріалу з гістологічних зрізів пухлин молочної залози найкращі результати ПЛР можуть бути отримані при поєднанні способу видалення парафіну нагріванням в мікрохвильовій печі та виділення ДНК з інкубацією тканини при температурі 57єС. Ідентифікація мутантних алелів генів BRCA1/2 у пацієнток з РМЗ дає можливість оцінити ступінь ризику виникнення РМЗ для осіб з родин, обтяжених цією патологією. Встановлено, що мутації в генах ВRCA1/2 і мутації мтДНК4977 можуть виступати в якості молекулярно-генетичних маркерів, які слід використовувати при визначенні ступеня спадкової схильності до РМЗ. Результати роботи були впроваджені в педагогічний процес кафедри медичної генетики Національної медичної академії післядипломної освіти імені П.Л. Шупика МОЗ України та в клінічних відділеннях Національного інституту генетичної інженерії і біотехнології Міністерства науки і техніки Ірану.
Особистий внесок здобувача. Дисертант вивчив сучасну літературу по темі дисертації, обґрунтував актуальність вибраної теми. Самостійно створив карту обстеження хворого на РМЗ і заповнював її для кожного пацієнта, провів клініко-генеалогічні та молекулярно-генетичні дослідження у хворих на РМЗ, узагальнив результати досліджень, провів аналіз і статистичну обробку одержаних результатів, написав усі розділи дисертаційної роботи, підготував наукові публікації. Висновки та практичні рекомендації сформульовані разом з науковим керівником.
Апробація результатів дисертації. Основні положення роботи разом з висновками доповідались на науково-практичній конференції з міжнародною участю «Генетичні аспекти діагностики та лікування в сучасній медицині» (Київ, 2006), VIII конференції молодих онкологів з міжнародною участю «Сучасні проблеми експериментальної та клінічної онкології» (Київ, 2007), науково-практичній конференції з міжнародною участю «Актуальні питання медичної генетики» (Київ, 2007), 17th International Congress on Anti-Cancer Treatment (Paris, France, 2006), VII Madrid Breast Cancer Conference: Changes in the treatment of breast cancer (Madrid, Spain, 2007), European Conference on Cancer and Ageing (Warsaw, Poland, 2007), 9th Iranian Congress of Biochemistry & the 2nd International Congress of Biochemistry and Molecular Biology (Shiraz,Iran,2007), Annual Conference of the German Genetics Society: Genetics of Aging (Jena, Germany, 2007).
Публікації. За матеріалами дисертації опубліковано 10 наукових праць, серед яких 3 статті у фахових виданнях та 6 тез доповідей на конференціях і конгресах.
Обсяг та структура дисертації. Зміст роботи викладено на 120 сторінках друкованого тексту. Дисертація складається зі вступу, огляду літератури, матеріалів та методів дослідження, розділу результатів власних досліджень, обговорення результатів, висновків, списку використаних джерел з 202 найменувань, з них 29 кирилицею.
ОСНОВНИЙ ЗМІСТ РОБОТИ
Об’єкт та методи дослідження. В дослідження були включені 84 пацієнтки з раком молочної залози з Ірану, які лікувались у Іранському центрі раку молочної залози (м.Тегеран), лікарні Хатам (м.Тегеран), лікарні Багіатоллах (м.Тегеран), і 120 пацієнток з України, які були прооперовані у Київській міській онкологічній лікарні. За віком пацієнтки були поділені на групи: 18-30 років, 31-40 років, 41-50 років, 51-60 років, 61-70 років та група жінок, старших за 70 років. Клінічний діагноз РМЗ був підтверджений патоморфологічним дослідженням операційного матеріалу. На момент встановлення діагнозу пухлини були класифіковані як Т1N0-1M0, T2N0-1M0 T3N1-2M0. У всіх пацієнток було проведено рутинне гістологічне дослідження пухлини з виготовленням парафінових блоків і гістологічних препаратів, що були забарвленні гематоксилін-еозином. Імуногістохімічне дослідження виконувалось з застосуванням антитіл для виготовлення антитіл для виявлення рецепторів естрогену та прогестерону. Облік результатів проводився шляхом підрахунку відсотку клітин, що мали забарвлені ядра.
Розподіл хворих за віком на момент встановлення діагнозу, місцем народження і проживання представлено у таблиці 1.
Від усіх пацієнток було отримано інформовану згоду на проведення дослідження, після чого у них брали пробу венозної крові або проводили дослідження пухлини молочної залози.
Для всіх пацієнток складався родовід з подальшим проведенням клініко-генеалогічного аналізу за стандартною методикою (Бочков Н.П., 2002).
Для визначення ризику розвитку РМЗ у жінок з України було проведено аналіз даних Національного канцер-реєстру України за 2004 рік (розділ статево-вікові показники захворюваності на рак молочної залози). Визначення відносного ризику (RR) розвитку РМЗ в залежності від віку здійснювали за допомогою статиcтичної програми EpiCalc2000, v.1.0.
Молекулярно-генетичні дослідження біологічного матеріалу від українських пацієнток виконувались в лабораторії кафедри медичної генетики Національної медичної академії післядипломної освіти імені П.Л.Шупика, іранських пацієнток – в лабораторії Інституту молекулярної генетики та біотехнологій - м. Тегеран, Іран.
При виконанні лабораторної частини роботи були використані різні методи депарафінування гістологічних зрізів пухлин молочної залози та різні методи виділення ДНК з депарафінізованих тканин (Cao W. Et al., 2003; Coura R. et al., 2005). Депарафінізовані тканини ресуспендували у лізуючому буфері з протеїназою К та інкубували до повного розчинення тканини. Виділення ДНК з лейкоцитів периферичної крові здійснювалось близькими за складом комерційними наборами фірм CinaGene (Іран) та АмпліСенс (Росія) згідно рекомендаціям фірми-виробника.
Мутації 5382insC та 185delAG у гені BRCA1, 6174delT у гені BRCA2 виявляли методом мультиплексної полімеразної ланцюгової реакції відповідно до публікації Chan P.C. з співавт. (1999), мутацію мтДНК4977 у мітохондріальній ДНК – відповідно до публікації Zullo S.J. (2000). Використовували наступний режим ампліфікації: денатурація при 94°C протягом 5 хвилин, 35 циклів ампліфікації по наступній програмі: 94°C – 0,5 хв., 55 °C – 1 хв., 72°C – 0,35 хв., завершальний синтез – 5 хвилин при 72°С. Для детекції продуктів ампліфікації застосовували горизонтальний електрофорез у 2% агарозному гелі.
Імуногістохімічне дослідження за допомогою антитіл до рецепторів естрогенів та прогестерону у пухлинах молочної залози проводились в лабораторії патологічної анатомії шпиталів Хатам та Багіатоллах, зав. проф. М.Хашемі та М.Х.Акбарі (м.Тегеран, Іран) для іранських пацієнток та в лабораторії патологоанатомічного відділення Київської міської онкологічної лікарні, зав. канд.мед.наук Л.М.Захарцева.
Статистичний аналіз одержаних результатів включав обчислення значень критерію хі-квадрат (чІ), z-критерію та вирахування відносин шансів (Odds Ratio, OR) за допомогою комп’ютерних програм EpiCalc2000, v.1.0. та Epi Info(ТМ) 2005.
Результати дослідження та їх обговорення
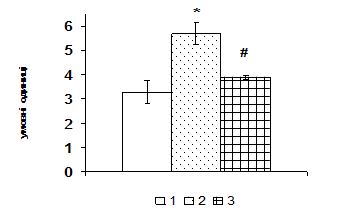
На основі аналізу матеріалів Національного канцер-реєстру України за 2004 рік було розраховано відносний ризик розвитку РМЗ для жінок в залежності від віку. Ці результати представлені на рисунку 1. За досліджуваний період в Україні було зареєстровано 15863 нових випадків РМЗ у жінок у віці від 15 років і більше, стандартизований показник захворюваності склав 38,3 на 100000 жіночого населення. Показник захворюваності у групі дівчат та жінок 15-19 років склав 0.2 на 100000 (RR прийнято за 1), потім зі збільшенням віку показник захворюваності зростав, досягаючи максимуму у вікових групах 55-59 і 65-69 років (148,8 на 100000 и 154,0 на 100000) (RR відповідно становив 263 і 273).
Як показав наш аналіз офіційних статистичних даних, абсолютне число нових випадків РМЗ в Ірані протягом року становило 4742, стандартизований показник захворюваності склав 17,1 на 100000 жіночого населення. При цьому, як і в Україні, в Ірані були відмічені аналогічні рівні зростання частоти захворюваності жінок старших вікових груп, проте особливості формування статистичних даних про частоту онкологічної патології в Ірані не дозволили провести зіставлення коефіцієнту відносного ризику в двох країнах.
Рак молочної залози – це мультифакторіальне захворювання, на виникнення якого впливає комплекс факторів, тиск цих факторів збільшується з віком, і підвищення частоти хворих на РМЗ в старших вікових групах є очікуваним. Проте жінки до 40 років, у яких РМЗ часто має важкий і швидкий перебіг, за віковою ознакою не включаються до групи ризику, яка підлягає плановим профілактичним оглядам. Тому відокремлення цієї групи пацієнток можливе, в першу чергу, за рахунок використання в схемах їх обстеження високоінформативних діагностичних маркерів. Це перш за все проведення клініко-генеалогічного аналізу та застосування молекулярно-генетичних досліджень.
За результатами клініко-генеалогічного аналізу, сімейні випадки захворювання родичів І та ІІ ступеню спорідненості на рак молочної залози (СРМЗ) становили 32,1% у пацієнток з Ірану (рис.2) та 28,6% – з України.
Як було показано вище, ризик розвитку захворювання на РМЗ в загальній популяції збільшується з віком, в той час як для сімейних випадків РМЗ максимальні величини відносного ризику було виявлено нами у віковій групі до 55 років (табл.2). Коефіцієнт RR для жінок до 35 років у 2 рази перевищує такий у порівнянні з особами старше 76 років.
Використання патологоанатомічного архівного матеріалу, який зберігається в блоках, пов’язане з дедалі більш частою потребою ретроспективного аналізу молекулярно-генетичних маркерів. Стандартні методи виділення ДНК з матеріалу гістологічних зрізів пухлин молочної залози, які застосовувались на початку нашої роботи, давали високий відсоток деградованої ДНК, що обмежувало можливості використання гістологічних зрізів тканин пухлин для дослідження молекулярно-генетичних маркерів, що було основною метою роботи.
Для вибору оптимального методу видалення парафіну та оцінки ефективності подальшої реакції ампліфікації було використано 20 зразків гістологічних зрізів товщиною 20 мкм пухлин молочної залози жінок, які були прооперовані з приводу РМЗ. Зрізи розміщували у мікроцентрифужні пробірки, додавали 200 мл буферного розчину (тріс-HCl, pН 9,0, 0,5% Тween-20), паралельно проводили різні процедури видалення парафіну:
1) нагріванням зразка у мікрохвильовій печі протягом 45-60 сек. при потужності 650 w,
2) нагріванням зразка в автоклаві протягом 20 хвилин при температурі 120 °C,
3) експозицією зразка у ксилолі протягом 30, 60 і 120 хвилин (стандартний метод).
Для виділення ДНК після депарафінізації зрізів використовували два варіанти інкубації матеріалу з протеїназою К :
1) при 37 °С протягом 12 годин,
2) при 57 °С протягом 3 годин.
При порівнянні ефективності виділення ДНК з гістологічних зрізів різними методами найкращі результати ПЛР було отримано при поєднанні способу видалення парафіну нагріванням в мікрохвильовій печі з інкубацією тканини при температурі 57 °С (табл. 3).
При порівнянні кількості позитивних результатів ампліфікації генів BRCA 1/2 позитивний результат ПЛР виявлено у 70% випадків (14 з 20).Різниця ефективності склала 35% (P <0,03).
Вибір можливих молекулярно-генетичних маркерів для визначення ризику розвитку РМЗ базувався на відомостях про значну роль мутацій в генах BRCA 1 та BRCA 2 у виникненні цієї патології. Були вибрані мутації 5382insС, 185delAG в гені ВRCA1 і мутація 6174delT в гені ВRCA2, що визнані мажорними для європейських популяцій.
При молекулярно-генетичному обстеженні 120 хворих на РМЗ з України мутації в генах BRCA 1 та BRCA 2 були виявлені у 13 жінок (11,40%). У 10 пацієнток була виявлена мутація 5382ins у гені BRCA 1 (8,33%), у 2 пацієнток з 45 проведених обстежень – мутація 185delAG у гені BRCA 1 (4,44%), у 1 пацієнтки з 49 проведених обстежень – мутація 6174delТ у гені BRCA 2 (2,04%). При вивченні розподілу пацієнток - носіїв мутацій у генах BRCA по віку максимальне число мутацій було виявлено у віковій групі 31-40 років. Це відповідає літературним даним про те, що для BRCA-асоційованих форм злоякісних пухлин характерним є ранній вік початку захворювання [Billack B., Monteiro A., 2005].
При молекулярно-генетичному обстеженні 120 хворих на РМЗ з України мутації в генах BRCA 1 та BRCA 2 були виявлені у 13 жінок (11,40%). У 10 пацієнток була виявлена мутація 5382ins у гені BRCA 1 (8,33%), у 2 пацієнток з 45 проведених обстежень – мутація 185delAG у гені BRCA 1 (4,44%), у 1 пацієнтки з 49 проведених обстежень – мутація 6174delТ у гені BRCA 2 (2,04%). При вивченні розподілу пацієнток - носіїв мутацій у генах BRCA по віку максимальне число мутацій було виявлено у віковій групі 31-40 років. Це відповідає літературним даним про те, що для BRCA-асоційованих форм злоякісних пухлин характерним є ранній вік початку захворювання [Billack B., Monteiro A., 2005].
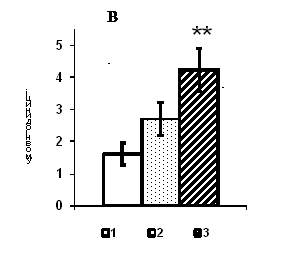
Висновок про те, що наявність мутацій у генах BRCA, може бути використане як молекулярно-генетичний маркер ризику розвитку РМЗ для жінок молодого віку, підтверджує і розрахунок відносного ризику розвитку РМЗ у осіб, що мають мутації у генах BRCA (рис.3). Представлена на рисунку 3 діаграма показує зменшення значень коефіцієнту RR з віком жінок з РМЗ при наявності мутантних алелів генів BRCA, на противагу найбільшим значенням відносного ризику у осіб старших вікових груп при урахуванні лише вікової характеристики пацієнток (рис.2).
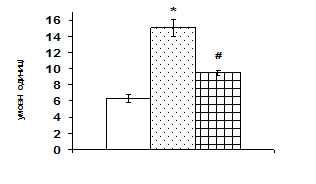
3 з 34 (9%) обстежених молекулярно-генетичними методами пацієнток з РМЗ із Ірану була виявлена мутація 5382insС у гені BRCA 1 (рис.4). При цьому ні в одному випадку мутація 5382insС не була виявлена у осіб з несімейним РМЗ, а частота цієї мутації в групі сімейного РМЗ склала 19%. Вік пацієнток, що мали мутацію в гені BRCA, також не перевищував 45 років. Мутації 185delAG в гені ВRCA1 і 6174delT в гені ВRCA2 не були знайдені ні в одному випадку.
У 69,6% з 120 обстежених українських пацієнток з РМЗ при дослідженні імуногістохімічних маркерів були виявлені рецептори естрогену, у 60% – рецептори прогестерону. При цьому з 13 жінок – носіїв мутацій в генах BRCA1/2 рецептори естрогену та прогестерону в тканині пухлини були виявлені лише в 21,43% зразків, а в групі померлих пацієнток рецептори естрогену було виявлено в 5,8% випадків, рецептори прогестерону – в 11,8% випадків.
Відсутність досліджуваних рецепторів в пухлинах молочної залози, за даними літератури (Lakhani S.R. et al., 2002, Eerola H. et al., 2005, Chen S., 2006) характерні для жінок, що мають мутації в генах BRCA1/2, і за думкою багатьох спеціалістів є ознакою несприятливого прогнозу.
Наявність рецепторів естрогену було виявлено у 15 з 34 (44,1%) обстежених іранських жінок, що хворіють на РМЗ, рецептори прогестерону – у 17 (50%). Низька частота виявлення рецепторів естрогену/прогестерону у пухлинах молочної залози у жінок з Ірану, можливо, пов’язана з малою вибіркою. В той же час слід зазначити, що наявність рецепторів була встановлена в декілька разів частіше у пацієнток з несімейним РМЗ (рецептори естрогену – 61% проти 25% при сімейній формі, рецептори прогестерону - 67% та 31%, відповідно).
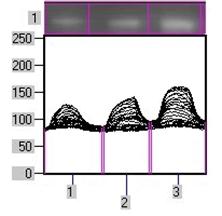
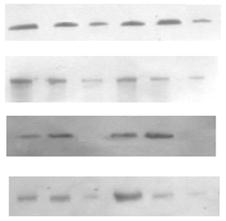
У розвитку пухлин значну роль відіграє процес накопичення мутацій, котрі виникають як у ядерній, так і у мітохондріальній ДНК. Дослідженнями останніх років показано, що при різних видах пухлин, в тому числі і при РМЗ, з високою частотою виявляють мутації мтДНК. Роль мітохондріальних мутацій в процесі онкогенезу на сьогоднішній день вивчена недостатньо. Проте не підлягає сумніву той факт, що порушення функцій мітохондрій внаслідок високої частоти мутацій, які виникають в мітохондріальному геномі, не репаруються і накопичуються, не можуть не вплинути на стан клітин і тканин. . Тому поглиблене вивчення мітохондріальних мутацій як ранніх маркерів пошкодження клітин на молекулярному рівні основане на необхідності виявлення начальних етапів патологічного процесу.При дослідженні наявності делеції мтДНК4977 в мітохондріальній ДНК результати ПЦР було виявлено у всіх 47 зразках – 9 з крові, 34 – з тканини пухлини. При дослідженні 9 зразків крові пацієнтів з РМЗ була виявлена делеція мтДНК4977 в 5 препаратах ДНК (56%), в тканині пухлини від цих же пацієнток мутація в мтДНК виявлена не була (рис.5). В 34 зразках ДНК з гістологічних зрізів мутація мтДНК4977 не була виявлена ні в одному випадку.
Розроблено діагностичний алгоритм, який дозволяє визначати ступінь ризику виникнення РМЗ за допомогою поетапного проведення клініко-генеалогічного та молекулярно-генетичного досліджень. Цей алгоритм суттєво покращить ефективність медико-генетичного консультування.
ВИСНОВКИ
У дисертаційній роботі наведено теоретичне узагальнення і вирішення наукового завдання, що полягає у підвищенні ефективності визначення ризику розвитку раку молочної залози для жінок різних вікових груп на основі визначення молекулярно-генетичних маркерів спадкової схильності та сімейного характеру захворювання. Для визначення ступеню ризику виникнення раку молочної залози запропоновано діагностичний алгоритм.
Похожие работы
... сигналу K+; - зміни активності протеїнкіназ A та С у корі надниркових залоз під впливом іонів калію. Об’єкт дослідження. Внутрішньоклітинні сигнальні системи, залучені до перенесення сигналів регуляторів та модуляторів функції кори надниркових залоз. Регуляція синтезу кортикостероїдів в корі надниркових залоз модуляторами адренокортикальної функції: кортикотропіном, естрогенами, дофамі ...
... рака эндометрия // Матеріали XI з’їзду онкологів України, 29 травня-2 червня 2006 р. – Судак. – 2006. – С.188. Анотація Манжура О.П. Оптимізація комплексного лікування хворих на рак ендометрія з урахуванням біологічних особливостей пухлин. – Рукопис. Дисертація на здобуття наукового ступеня кандидата медичних наук за спеціальністю 14.01.07 – онкологія. - Інститут експериментальної ...
... ів лікування й активаційної терапії (лікування антигомотоксичними препаратами) онкологічних хворих. На підставі проведеного дослідження виявлені особливості окисного стресу (варіанти порушень окисного гомеостазу) у онкологічних хворих залежно від методу післяопераційної терапії й запропоновано вважати їх основними при виборі індивідуального курсу лікування, а також використовувати як критерії ...
... інфаркт міокарда. Діагноз підтверджує підвищення вмісту в крові креатин-фосфокінази (зокрема її МВ-фракції), міоглобіну, С-реактивного протеїну, фібриногену та продуктів його розпаду. 2.2 Методи обстеження хворих при захворюваннях органів дихання Велике значення в діагностиці захворювання легень має топографічна і порівняльна перкусія та аускультація легень. У діагностиці захворювань ...
0 комментариев