Навигация
МЕТОД РАДИАЦИОННОЙ ИНАКТИВАЦИИ
3.3 МЕТОД РАДИАЦИОННОЙ ИНАКТИВАЦИИ
Метод радиационной инактивации для определения размера мишени все чаще применяется при исследовании мембранных белков. Изучать можно как очищенные белки, так и неочищенные препараты, в том числе интактные биомембраны. Суть метода состоит в определении доли белковых молекул, получающих повреждения при облучении. Для этого используют ферментативные методы связывания гормонов или других лигандов или спектральные методы. Процедура состоит в следующем. Образец, обычно замороженный, подвергают высокоэнергетическому облучению. Через разные промежутки времени отбирают пробы, размораживают их и проводят измерения. Повреждения белка под действием излучения выявляют, например, с помощью электрофореза в ПААГ с ДСН. Как показывает опыт, некоторые субъединицы полностью утрачивают биологическую активность при внесении радиационного повреждения в любое место полипептидной цепи. Ключевым моментом является то, что, чем крупнее белковая молекула, тем больше вероятность ее повреждения и, следовательно, вероятность инактивации. Эта вероятность зависит не от формы молекулы, а от ее массы. Обычно для того, чтобы облегчить интерпретацию результатов, параллельно облучают белок с известной молекулярной массой. Если исследуемый белок содержит более одной субъединицы, возникают определенные трудности при анализе результатов. Повреждение одной субъединицы не обязательно сопровождается разрывом ковалентных связей в других субъединицах. Поэтому для ферментов, состоящих из разных субъединиц, обладающих неодинаковыми активностями, могут быть получены разные размеры мишени в зависимости от метода определения степени инактивации.
Примечательной особенностью метода является то, что его можно использовать для изучения интегральных мембранных белков in situ. Возникающие при этом артефакты и проблемы рассмотрены в работе. Одна из очевидных проблем — необходимость использования высокоэнергетического излучения. В связи с этим большинство работ приходится проводить в сотрудничестве с лабораториями, в которых имеются соответствующие источники и освоены специальные методы анализа.
3.4 СПЕКТРАЛЬНЫЕ МЕТОДЫ И ВТОРИЧНАЯ СТРУКТУРА
Для определения содержания а-спиралей и /3-слоев в мембранных белках используют несколько методов. В отсутствие трехмерной организации на их основе можно попытаться построить соответствующие модели. Чаще всего используется метод кругового дихроизма. Все более широкое применение находят инфракрасная и рамановская спектроскопия, а также ЯМР.
1. Метод кругового дихроизма основан на измерении разности поглощения лево- и правополяризованного света; эта оптическая активность является мерой хиральности молекул, или мерой их асимметрии. В дальней ультрафиолетовой области КД определяется в основном поглощением амидов карбонильных групп полипептидного остова. При наличии участков вторичной структуры, например а-спиралей, спектр КД имеет вполне определенные особенности, связанные с особенностями электронного окружения амидиых групп в этих структурах. Анализизуя спектр КД белков, его обычно представляют как сумму компоиеитов, отвечающих поглощению разных участков белковой молекулы: а-спиралей, /3-слоев и случайных клубков. Определив тем или иным способом спектры каждой из этих структур, производят их суммирование, подбирая соответствующие коэффициенты таким образом, чтобы было достигнуто наилучшее соответствие измеренному спектру. Подобранные весовые коэффициенты представляют собой ту долю, которая приходится в молекуле на каждый из типов вторичной структуры.
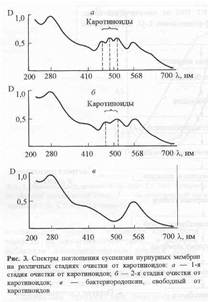
Эти методы были разработаны для растворимых белков, но нет никаких оснований сомневаться, что их можно с успехом применять и для мембранных белков. Скорее всего у последних имеются участки с такими же типами вторичной структуры, как и у растворимых белков, и при их изучении возникнут такие же трудности. Некоторые белки можно изучать in situ, используя суспензии мембран. Примерами такого рода являются бактериородопсин из пурпурной мембраны Halobacterium halobium и Са2+ -АТРаза из мембраны саркоплазмати-ческого ретикулума. Очищенные мембранные белки можно исследовать с помощью КД и в присутствии детергентов, если поглощение последних в дальней УФ-области не слишком велико, или в составе реконструированных везикул. Здесь возникают две проблемы: 1) дифференциальное светорассеяние, когда размер мембранных частиц гораздо больше длины волны света; 2) выравнивание поглощения из-за концентрирования белка в мембранах или везикулах, т. е. из-за негомогенности его распределения в растворе. Эти артефакты могут быть весьма существенными, однако их можно учесть с помощью соответствующих методов.
К сожалению, для внутренних мембранных белков отсутствуют структурные данные высокого разрешения, поэтому точная интерпретация спектров КД невозможна. За исключением нескольких случаев, разные спектральные методы не использовались для изучения одного и того же белка и количественное сравнение результатов не проводилось. Интересно, что для бактериородопсина, который исследовали методами КД, ИК и ЯМР, во всех трех случаях были получены одинаковые результаты, свидетельствующие о значительном содержании в этом белке 3-слоев. Тем не менее у каждого метода имеются существенные недостатки. Так, данные о высоком содержании в бактериородопсине Д-слоев в значительной мере зависят от способа учета оптических артефактов. Судя по данным электронно-микроскопической реконструкции, харатеризующимся относительно низким разрешением, в бактериородопсине 80% приходится на долю а-спира-лей, а 0-слои отсутствуют совсем. Чтобы понять причину этих несоответствий, необходимо провести структурный анализ белка с атомным разрешением. Имеются еще два белка, пронизывающие мембрану, с высоким содержанием, и а-токсин Staphylococcus aureus. Оба этих белка участвуют в образовании пор в бислое.
2. Инфракрасная спектроскопия и спектроскопия комбинационного рассеяния. Эти методы не только позволяют получить сведения о конформации мембранных липидов, но и могут использоваться для исследования вторичной структуры белков. Колебательный спектр полипептидного остова зависит от типа вторичной структуры и дает информацию о содержании в молекуле а-и /3-структур. Этими методами можно исследовать высушенные на воздухе пленки, водные суспензии мембран, а также очищенные белки как в присутствии детергента, так и в составе реконструированных везикул. Например, по данным ИК-спектроскопии с преобразованием Фурье комплекс Са2+ -АТРазы в мембране состоит в основном из а-спиральных участков и участков, имеющих кон-формацию статистического клубка, а гидрофобный белок миелин в реконструированных везикулах имеет как а-, так и /3-участки.
3. ЯМР-спектроскопия также может использоваться для изучения мембранных белков. Однако возможности метода в этом случае ограничены, что связано главным образом с относительно медленными движениями интегральных мембранных белков in situ и в комплексах с детергентом. Поэтому такой мощный метод, как двумерный ЯМР, который может дать детальную картину конформацион-ного состояния сравнительно небольших белков в растворе, пока непригоден для изучения мембранных белков. Более приемлем метод ЯМР твердых образцов. Большими возможностями обладают методы 2Н- и |3С-ЯМР, хотя до сих пор они применялись не очень широко. Получены данные об усредненной конформации остова и динамике боковых цепей. Следует отметить, что методы ЯМР твердого состояния не только не используются широко, но в большинстве случаев их и нельзя использовать. Тем не менее в тех редких ситуациях, когда их применение оказывается возможным, они являются очень ценными.
Похожие работы
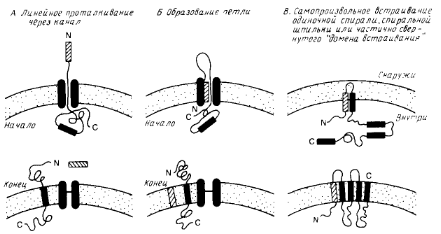
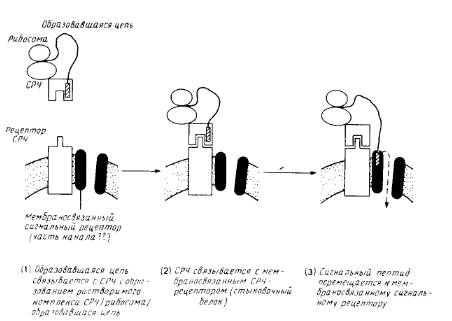
... . О предполагаемом канале, участвующем в переносе, ничего неизвестно; очистка его является довольно сложной задачей. 5. Сборка мультисубъединичных комплексов и обновление мембранных белков После встраивания мембранного полипептида в мембрану он еще должен приобрести правильную конформацию, обеспечивающую его биологическую активность, а если речь идет о мультисубъединичных комплексах, то ...
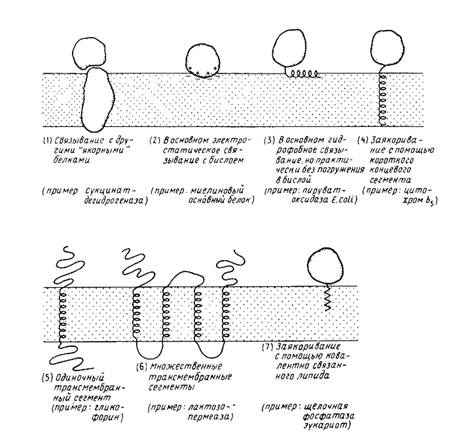
... на N-, либо на С-конце молекулы. N – и С-концы трансмембранных белков (5 и 6) могут находиться как у наружной, так и у внутренней поверхности мембраны. 2. Выделение мембранных белков Очистка и характеристика мембранных белков ставят перед исследователем целый ряд специфических проблем, с которыми он обычно не сталкивается, работая с растворимыми белками. Мембранные белки, как правило, ...
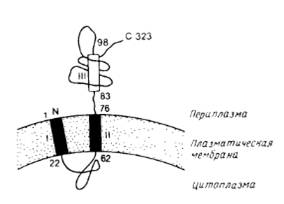
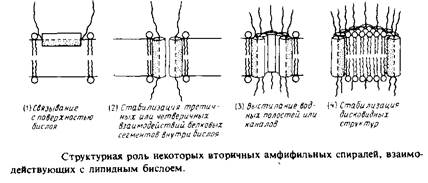
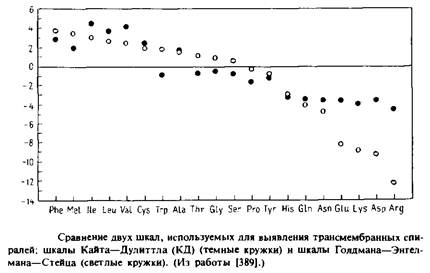
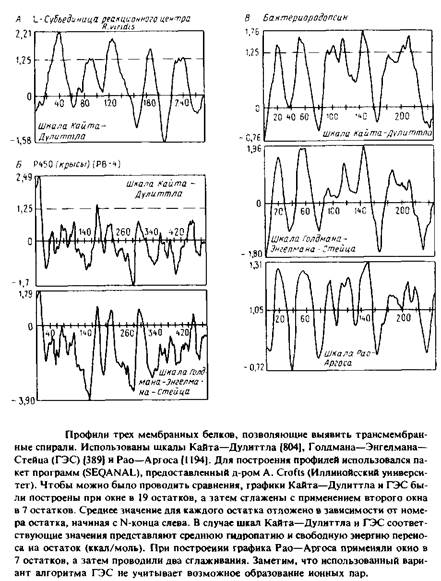
... внутри бислоя могло бы стабилизировать трехмерную структуру мембранных белков. Способы идентификации первичных амфифильных структур Однозначная структурная информация о мембранных белках получена лишь в нескольких случаях, но зато в распоряжении исследователей имеются обширные данные об аминокислотной последовательности, основанные на результатах секвенирования ДНК. Для идентификации ...
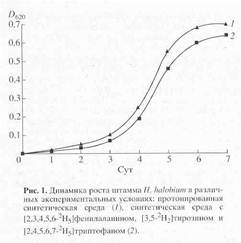
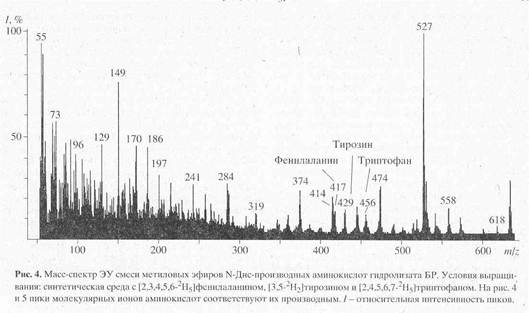
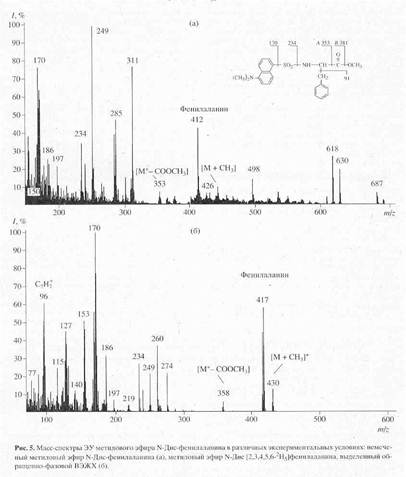
... в его функционировании [10]. Поэтому важно получать подобные модифицированные дейтерием белки в очищенном виде и в препаративных количествах. Целью настоящей работы было получение препаратов бактериородопсина, селективно меченных дейтерием по остаткам ароматических аминокислот - L-фенилаланина, L-тирозина и L-триптофана, а также масс-спектрометрический анализ дейтерий-меченных аминокислот ...
0 комментариев