Навигация
Выбор стабильного сечения тройной системы, продукты реакций
4.2.2. Выбор стабильного сечения тройной системы, продукты реакций
Частичная триангуляция тройной системы W – O – Cl (рис.4.2.2) позволяет в каждом случае определить стабильные сечения, продукты реакций, соответствующие нестабильным сечениям, выделить частные тройные системы и на этой основе выбрать (с учетом данных табл.4.2.2) контролируемые методы синтеза индивидуальных фаз [3].
Таблица 4.2.2.1. Характеристики процессов сублимации, испарения и термического разложения высших (VI и V) галогенидов и оксогалогенидов вольфрама [3]
| Равновесие | Коэффициенты уравнения, Р - [Па] lgP = − А/Т + В | Интервал температур [°C] | Энтальпия парообразования [кДж/моль] | Температура [°С] | ||
| А | В | Tплав. | Tкип. | |||
| α-WCl6(т) → WCl6(п) β-WCl6(т) → WCl6(п) WCl6(ж) → WCl6(п) | 4400 3640 3220 | 12,48 10,98 10,22 | 180 – 231 231 – 291 291 – 300 | 84,4 70,2 62,1 | 270 - 281 | ~ 310 |
| WOCl4(т) → WOCl4(п) WOCl4(ж) → WOCl4(п) | 4789 2250 | 14,95 9,56 | 120 – 211 211 – 250 | 91,7 46,05 | 212 | ~ 300 |
| WO2Cl2(т) → WO2Cl2(п) 2WO2Cl2(т) → WO3(п) + WOCl4(п) | 5043 6514 | 11,67 15,175 | 230 – 290 250 – 350 | 96,6 131,9 | ~ 350 | ~ 350 |
| 2WOCl3(т) | 6660 | 16,95 | 230 – 280 | 136,0 | ~ 400 | |
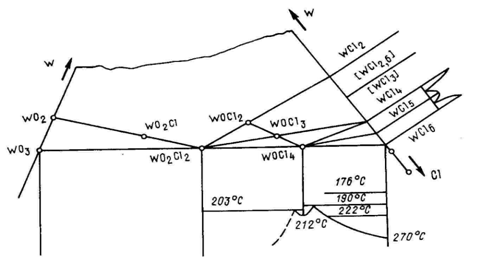
Рис.4.2.2.1. Частичная триангуляция системы вольфрам – кислород – хлор [3]
Хлорирование твердосплавного сырья экономически выгодно провести при использовании анодного хлор-газа (содержание хлора ~ < 85%). Основные компоненты анодного хлор-газа это хлор и кислород. Как было показано в предыдущих разделах работы (4.1) наиболее удобным целевым продуктом при выбранных режимам является WOCl4. При помощи программы TERRA изучим свойства данной системы в приближении локального термодинамического равновесия. Данные для расчёта взяты из таблицы 4.2. Компоненты твердого сплава, количество которых меньше 0,1% не учитывались в расчетах.
При выборе количества кислорода необходимо избежать его избытка, во избежание образования WO2Cl2. Избыток хлора не влияет на показатели процесса.
Кислород расходуется на образование WOCl4 и СО2 (см. стр. № 35 реакции 1 и 3), следовательно, необходимая масса кислорода равна:
![]() кг
кг
Хлор входит во все продукты реакций, и для изучения процесса хлорирования возмём хлор с избытком на 5%. Необходимая стехиометричеческая масса хлора равна:
![]()
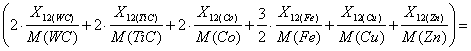
![]() кг
кг
Для моделирования процесса хлорирования твердого сплава возьмем данные из таблицы 4.2.1, 10000 кг хлора и 2443 кг кислорода.
Таблица 4.2.2.2. Результат моделирования процесса хлорирования при помощи прграммы TERRA, при температуре 700°C и давлении 0,1 МПа.
| Химическая формула | Масса [кг] |
| WOCl4 | 12291,53 |
| WO2Cl2 | 5,9 |
| WCl4 | 0,3 |
| WCl6 | 0,6 |
| TiCl4 | 4239,3 |
| CoCl2(c) | 1179,9 |
| FeCl3 | 203,3 |
| CuCl2(c) | 43,2 |
| ZnCl2(c) | 28,4 |
| ZnCl2 | 14,4 |
| CO2 | 2567,6 |
| Cl2 | 904,57 |
| Всего: | 21479 |
0 комментариев