Навигация
Введение. 2
Из истории открытия С-белков. 8
Структура и свойства. 8
Связь с мембраной. 9
Стуктурно-функциональная организация G-белков. 9
Классификация по чувствительности к токеинам.. 10
Сопряжение с эффекторными системами. 10
Регуляция активности G-белков. 11
Аденилатциклаза. 12
Фосфолипазы.. 13
Протеинкиназы.. 14
Фосфодиэстеразы.. 16
Аденилатциклазная система. 17
Влияние бактериальных токсинов на активность аденилатциклазы (АДФ-рибозилирование G-белков) 20
Инозитолфосфатная система. 21
Участие белка кальмодулина в инозитолфосфатной передаче сигнала. 22
Саморегуляция системы.. 23
α-субъединица: общие свойства. 23
β и γ субъединицы: общая характеристика. 24
G-белки: βγ-субъединицы.. 25
ГТФ-связывающие белки образуют два основных семейства G-белков и низкомолекулярных ГТФ-связывающих белков. 28
Литература. 30
Введение
Сигнальные G-белки являются универсальными посредниками при передаче гормональных сигналов от рецепторов клеточной мембраны к эффекторным белкам, вызывающим конечный клеточный ответ. Когда семидоменная рецепторная молекула, локализованная в мембране сенсорной клетки, активируется какими-то изменениями во внешней среде, она претерпевает конформационные изменения. Последние детектируются
G-белками связанными с мембраной, которые, в свою очередь, активируют эффекторные молекулы в мембране. Часто это приводит к выделению вторичных мессенджеров в цитозоль.
Они являются объектом интенсивного изучения в связи с их участием во многих важных физиологических процессах. G-белки, участвующие в передаче сигнала, являются членами большого надсемейства гуанин-связывающих белков. G–белки - это прецизионные регуляторы, включающие или выключающие активность других молекул.
Примерно 80% первичных мессенджеров (гормоны, нейротрансмиттеры, нейромодуляторы) взаимодействуют со специфическими рецепторами, которые связаны с эффекторами через G-белки.
G-белки - белки, связывающие гуанозиновые нуклеотиды. G-белки, ассоциированные с рецепторами, связаны с мембраной. В неактивном состоянии они связаны с GDР. При связывании рецептора с лигандом ГДФ замещается на ГТФ, в результате чего происходит активация. Процесс этот сравнительно медленный, протекающий в течение секунд - десятков секунд.
G-белки биологических мембран имеют гетеротримерную структуру. Они состоят из большой α-субъединиц (около 45 килодальтон - кДа), а также меньших β и γ-субъединиц, α-субъединица обладает ГТФ-азной активностью, в неактивной (выключенной) форме она связывает молекулу ГДФ на активном сайте. Субъединицы β и γ связаны между собой, и в физиологических условиях не могут быть диссоциированы. В неактивном состоянии βγ-комплекс непрочно связан с α-субъединицей. γ-субъединица связана с цитоплазматическим листком биологической мембраны геранил-гераниловой цепью (20 атомов углерода в цепи), близкой по структуре к холестерину. α-субъединица также связана с мембраной жирной кислотой с длиной цепи в 14 атомов углерода (миристоевая кислота). Такие связи обеспечивают то, что комплекс G-белка удерживается в плоскости мембраны, но в то же время способен легко двигаться в этой плоскости. Легко себе представить, как весь комплекс G-белка с присоединенным ГДФ перемещается в плоскости мембраны под действием тепловых сил, два семейства белков - гетеротримерные гуанозиннуклеотид связывающие белки (G-белки) и отдаленно родственные им гуанозинтрифосфатазы (ГТФ-азы) при связывании ГТФ могут включаться и активировать последующие компоненты передачи сигнала от поверхности клетки. Малые ГТФ-азы участвуют в контроле фундаментальных свойств клетки - полярности формы и процессов деления и дифференцировки. G-белки обычно регулируют более специализированные сигналы - продукцию вторичных мессенджеров. И те и другие способны гидролизовать GTР и таким образом выключать сигнал.
Поскольку β - и γ-субъединицы G-белков чрезвычайно консервативны, G-белки принято различать по их α-субъединицам. Кроме ГТФ-связывающего мотива, каждая последовательность Gальфа содержит как минимум один центр связывания дивалентных катионов, а также сайты ковалентной модификации бактериальными токсинами, катализирующими NAD-зависимые АДФ-рибозилтрансферазные реакции. G-белки, стимулирующие аденилатциклазу (Gs) или участвующие в фототрансдукции (Gt, трансдуцин) служат субстратами для АДФ-рибозилирования, катализируемого холерным токсином по одному из остатков аргинина, что приводит к блокированию деактивации этих белков. Gs, G-белок, ингибирующий аденилатциклазу, (Gi) и G-белок с пока еще неизвестной функцией (Go) АДФ-рибозилируются коклюшным токсином по остатку цистеина, расположенному у С-конца. Эта модификация препятствует взаимодействию между G-белком и рецепторами. Определена последовательность G-белка крысы (Gx), который оказался нечувствительным к коклюшному токсину.
G-белки - это регуляторные белки, связывающие при активации ГТФ. Лучше всего изучены G-белки, стимулирующие и ингибирующие аденилатциклазу (Gs - белки и Gi-белки соответственно). βı - адренорецепторы, β2 - адренорецепторы и D1 рецепторы сопряжены с белком Gs, и поэтому стимуляция этих рецепторов сопровождается активацией аденилатциклазы и повышением внутриклеточной концентрации цАМФ - классического второго (внутриклеточного) посредника. Конечный ответ в разных клетках различен и зависит от того, что представляет собой эффекторные фрагменты (фермент, ионный канал и пр) α2– адренорецепторы, М2-холинорецепторы и D2-рецепторы сопряжены с белком Gi, и стимуляция этих рецепторов приводит к снижению активности аденилатциклазы и внутриклеточной концентрации цАМФ. Изменения активности ферментов и других внутриклеточных белков и, соответственно, клеточных функций при этом противоположны тем, что наблюдаются при активации белка Gs. α1-адренорецепторы (как и М1-холинорецепторы), видимо, сопряжены с другим, пока еще мало изученным типом G-белка. Этот белок иногда обозначают Gq. Он активирует фосфолипазу С, катализирующую распад мембранных фосфолипидов, в частности - фосфатидилинозитол-4,5-дифосфата до ИЗФ и ДГА. Оба эти вещества являются вторичными посредниками.
Связывание агониста (гормона, нейромедиатора и др.) с соответствующим рецептором приводит к белок-белковому взаимодействию между рецептором и G-белком и ускоряет диссоциацию ГДФ. В результате образуется короткоживущий комплекс агонист - рецептор - G-белок, не связанный ни с каким нуклеотидом. Связывание с этим комплексом молекулы ГТФ снижает сродство рецептора к G-белку, что приводит к диссоциации комплекса и высвобождению рецептора. Потенциально рецептор может активировать большое количество молекул G-белка, обеспечивая, таким образом, высокий коэффициент усиления внеклеточного сигнала на данном этапе. Активированная α-субъединица G-белка диссоциирует от βγ-субъединиц и вступает во взаимодействие с соответствующим эффектором, оказывая на него активирующее или ингибирующее воздействие.
α-субъeдиница с присоединенным с ней ГТФ способна взаимодействовать с эффектором в мембране - ферментами, такими, как аденилатциклаза, или, возможно, ионными каналами. Фермент может активироваться или ингибироваться, а ионный канал - открываться или закрываться. Конкретные примеры будут рассмотрены в последующих разделах. Взаимодействие с эффектором, однако, длится до тех пор, пока α - субъединица, являющаяся ГТФазой, удерживает ГТФ. Так что, очень вскоре присоединенный ГТФ гидролизуется до ГДФ. Когда это происходит, α - субъединица снова меняет свою конформацию и теряет способность активировать эффектор. После этого α-ГДФ взаимодействует с βγ-комплексом и снова образует тримерный комплекс, завершая, таким образом, цикл. Предполагают также, что комплекс из βγ-субъединиц тоже может (прямо или опосредованно) влиять на эффекторные ферменты.
Такими ферментами являются аденилатциклаза, фосфолипаза С. G-белки также регулируют работу К и Са²+-ионных каналов, К G-белкам относятся полипептид Gs, стимулирующий аденилатциклазу и регулирующий Са²+-ионные каналы, полипептид Gi, ингибирующий аденилатциклазу, и регулирующий К+-каналы в клетках тканей мозга, Gt, трансдуцин, участвующий в передаче светового сигнала, Golf специфичный белок обонятельных ресничек и др. Все G-белки являются гетеротримерами, состоящими из субъединиц α, β‚ и γ в порядке уменьшения молекулярной массы.
Впоследствии ГТФ, связанный с α-субъединицей G-белка, подвергается гидролизу, причем ферментом, катализирующим этот процесс, является сама α-субъединиц. Это приводит к диссоциации α-субъединицы от эффектора и реассоциации комплекса α-ГДФ с βγ - субъединицами. Спонтанная активация G-белка, связанного с ГДФ - весьма маловероятный процесс.
Этот же механизм лежит в основе гормональной регуляции фосфоинозитидспецифичной фосфолипазы С и фосфолипаза А2. Кроме того, было показано, что G-белки могут непосредственно активировать ионные каналы.
Лимитирующей стадией процесса восстановления исходного состояния G-белка является скорость диссоциации ГДФ от α-субъединицы G-белка. Скорость диссоциации увеличивается при взаимодействии G-белок-ГДФ с агонистсвязанным рецептором. Связывание ГТФ G-белком приводит, очевидно, к образованию комплекса агонист-рецептор-G-белок. Аналог GТР-СТР-γ-S и Мg2+ усиливает диссоциацию α-субъединицы из тримера G-белка. Однако следует заметить, что каталитическая субъединица аденилатциклазы из мембран мозга быка хроматографически соочищается с α - и β-субъединицами Gs-белка и вопрос диссоциации α-субъединиц из тримера G-белка для активации эффектора требует уточнения.
G-белки проявляют значительный полиморфизм. Каждая из форм субъединиц G-белка высокогомологична по структуре, близка по функциям, но отличается молекулярной массой и электрофоретической подвижностью. Особенно широк полиморфизм и наиболее изучен для αs и αi G-белков. Так из мозга человека выделено 11 форм ДНК, ответственных за синтез αs-субъединиц, четыре вида которых клонированы и, предполагается, что они определяют синтез четырех изоформ αs, в мозге человека. Для αi найдены, в основном, три изоформы αi1, αi2, αi3. Молекулярные массы изоформы αs находятся в пределах 42-55 кДа, а αi 39-41 кДа. Распределение молекулярных вариантов αi носит тканеспецифический характер: αi1 представлена, в основном, в мозге, αi2 обнаружена в нервной ткани и в клетках крови, αi3 представлена в периферических тканях и отсутствует в мозге. Распределение генов, кодирующих синтез трех изоформ αi по тканям примерно совпадает в ряду: человека, бык, крыса, мышь. Определение аминокислотной последовательности αi и αs показало, что изоформы αs или αi различаются в области С - и N - концевой последовательности, связывающихся с рецептором или эффектором. Предполагается, что полиморфизм α-субьединиц определяется многообразием рецепторов и их подтипов и разнообразием эффекторных систем.
αi-субъединицы Gi кодируются тремя различными структурными генами. Что касается изоформ α-субъединиц Gs-белков, то пока неясно, кодируются ли изоформы разными структурными генами или это продукт одного гена с последующим внутренним альтернативным сплайсингом исходного РНК-транскрипта, или множественность их результат посттрансляционной модификации. В настоящее время известно 9 структурных генов, кодирующих G-белки и 12 продуктов этих генов.
Из истории открытия С-белков
1. 1971г. - впервые показана необходимость ГТФ для стимуляции аденилатциклазы глюкагоном.
2. 1981г. - выделен белок Gt-трансдуцин, связывающий родопсин с фосфодиэстеразой с ГТФ фоторецепторов.
З. 1983г - выделен ГТФ-связываюший белок Gs, сопрягающий стимулирующие рецепторы с аденилатциклазой.
4. 1985-1988гт - показано, что фосфолипаза С и фосфолипаза А2 регулируются гормонами и нейротрансмиттерами через Gp-белки.
5. В настоящее время G-белки разделены на несколько типов: четыре Gs, три Gi, Go, Gz/x (центральная нервная система и селезенка), Gt (трансдуцин), Golf (обонятельные нейроэпителиальные клетки).
Структура и свойства1. G-белки - гетеротримеры, в которых α-субъединица непрочно связана с димером β-γ.
2. Все известные α-субъединицы (мол. масса – 50кДа) гомологичны, и у большинства из них одинаковые (или очень сходные) b-субъединицы (мол. масса З5кДа) и γ-субъединицы (мол. масса 8кДа).
З. α-субъединица определяет специфичность связывания G-белка с рецептором и эффектором, уникальна для каждого G-белка.
4. α-субъединица связывает и гидролизует ГТФ (ГТФ-аза).
5. α-субъединица содержит высоко консервативный домен связывания и гидролиза ГТФ (18 аминокислот из 350-395).
6. Выявлены участки связывания гуаниновых нуклеотидов и участки взаимодействия с рецепторами (С-конец) и βγ-димерами (N-конец).
7. Выявлены участки АDР-рибозилирования (аргинин-202) при действии холерного токсина и коклюшного токсина.
Связь с мембранойG-белки локализованы на внутренней поверхности плазматической мембраны. Первичная структура всех субъединиц G-белков не содержит гидрофобных, пронизывающих мембрану доменов.
1. Ассоциации G-белков с мембраной содействует ацилирование жирнокислотными радикалами. Выявлено два типа липидных модификаций субъединиц G-белков: миристоилирование и изопренилирование белковой цепи.
2. Показано для α-субъединиц Go - и Gi-белков посттрансляционное миристоилирование со стороны N-конца.
З. Для βγ-субъединиц также показаны посттрансляционные модификации (ацилирование).
4. Выявлены три последовательные посттрансляционные модификации, ответственные за связывание ras-белков с мембраной.
5. Очищенные α-субъединицы проявляют гидрофильные свойства (без βγ - комплекса не могут связываться с искусственными фосфолипидными пузырьками).
Стуктурно-функциональная организация G-белковG-белки (ГТФ-связывающие белки) - универсальные посредники при передаче сигналов от рецепторов к ферментам клеточной мембраны, катализирующим образование вторичных посредников гормонального сигнала. G-белки - олигомеры, состоящие из α, β и γ-субъединиц. Состав димеров βγ незначительно различаются в разных тканях, но в пределах одной клетки все G-белки, как правило, имеют одинаковый комплект βγ-субъединиц. Поэтому G-белки принято различать по их α-субъединицам. Выявлено 16 генов, кодирующих различные α-субъединицы G-белков. Некоторые из генов имеют более одного белка, вследствие альтернативного сплайсинга РНК.
Каждая а-субъединица в составе G-белка имеет специфические центры:
связывания ГТФ или ГДФ;
взаимодействия с рецептором;
связывания с βγ-субъединицами;
фосфорилирования под действием протеинкиназы С;
взаимодействия с ферментом аденилатциклазой или фосфолипазой С.
В структуре G-белков отсутствуют α-спиральные, пронизывающие мембрану домены. G-белки относят к группе "заякоренных" белков.
Классификация по чувствительности к токеинамПохожие работы
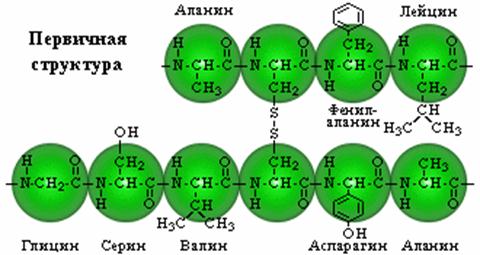
... , вызывает уменьшение количества синтезируемых ферментов. Это последнее явление получило название репрессии синтеза ферментов. Оба явления — индукция и репрессия — взаимосвязаны. Согласно теории Жакоба и Моно в биосинтезе белка у бактерий участвуют по крайней мере три типа генов: структурные гены, ген-регулятор и ген-оператор. Структурные гены определяют первичную структуру синтезируемого белка. ...
... белка - в различных сортах мяса и птицы содержится от 14 до 24% белка. Взаимозаменяемость первой и второй группы. Продукты двух первых групп являются наиболее важными поставщиками полноценного белка, с близкими по их аминокислотному составу и хорошей усвояемости организмом. Продукты первой и второй группы как источники белка в значительной степени могут заменять друг друга. Это означает, что их ...
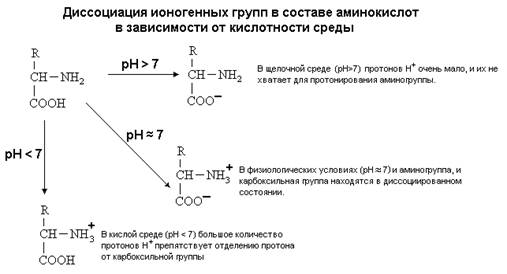
... + щелочная ср. NH2 R R R COOH COO – COO – Катион Амфион Анион Таким образом, фактором, определяющим поведение белка как катиона или аниона, является реакция среды, которая определяется концентрацией водородных ионов и выражается величиной рН. Однако ...
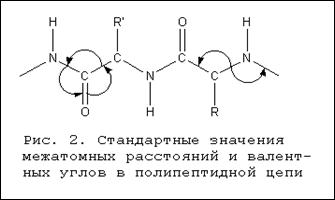
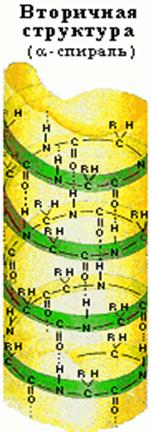
... равен 1/16 массы атома кислорода (кислородная единица массы). КОНФИГУРАЦИЯ И КОНФОРМАЦИЯ БЕЛКОВОЙ МОЛЕКУЛЫ Из всего сказанного можно заключить, что пространственная организация белков очень сложна. В химии существует понятие - пространственная КОНФИГУРАЦИЯ - жестко закрепленное ковалентными связями пространственное взаимное расположение частей молекулы (например: принадлежность к L-ряду ...


0 комментариев