Навигация
Между молекулами полимера существуют поперечные химические связи, и вещество по существу представляет собой пространственную сетку
2. Между молекулами полимера существуют поперечные химические связи, и вещество по существу представляет собой пространственную сетку.
Неограниченное набухание это, когда полимер растворяется в растворителе. Набухание ВМС может прийти к возникновению значительного давления, если что-то препятствует увеличению объема образца (набухание древесины в воде).
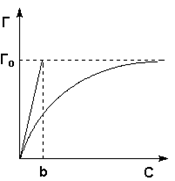
Давление набухания зависит от степени поперечной связанности полимера, что достаточно проявляется лишь при достаточной большой степени набухания. Давление набухания аналогично осмотическому давлению и определяется по уравнению:
![]() ,
,
где ![]() - парциальный мольный объем растворителя;
- парциальный мольный объем растворителя;
![]() - активность растворителя;
- активность растворителя;
![]() - давление насыщенного пара растворителя соответственно над набухшим полимером и чистым растворителем.
- давление насыщенного пара растворителя соответственно над набухшим полимером и чистым растворителем.
Контракция – уменьшение объема системы при набухании вещества в растворителе. Зависимость контракции от степени набухания:
![]() ,
,
где ![]() - константы, зависящие от природы набухающего вещества и растворителя.
- константы, зависящие от природы набухающего вещества и растворителя.
Контракция объясняется взаимодействием (сальватацией) вещества с растворителем, при котором происходит уплотнение системы.
4. Термодинамика растворения ВМС
Процесс растворения ВМС рассматривают как процесс смешения двух жидкостей. ВМС с гибкими макромолекулами должны лучше растворяться, чем с жидкими, поскольку первые могут располагаться в растворе большим числом способов. У жестких макромолекул энергия взаимодействия между отдельными макромолекулами цепочка очень велика, и такие цепи трудно оторвать друг от друга.
Самопроизвольное растворение ВМС сопровождается уменьшением изобарно-изотермического потенциала, согласно второму закону термодинамики:
![]() ,
,
Когда система не изменяет своего объема:
![]() ,
,
При самопроизвольном растворении полимера ![]() . Это может быть в двух случаях:
. Это может быть в двух случаях:
1. если ![]() , т.е. при растворении выделяется тепло;
, т.е. при растворении выделяется тепло;
2. если ![]() , так как некоторые полимеры способны растворяться с поглощением тепла.
, так как некоторые полимеры способны растворяться с поглощением тепла.
5. Особенности осмотического давления и вязкости у растворов ВМС
Осмотическое давление растворов полимеров значительно выше, чем у НМС и не подчиняется закону Вант-Гоффа. Объясняется это тем, что макромолекула благодаря гибкости ведет себя в растворе как несколько коротких молекул. Осмотическое давление увеличивается прямо пропорционально концентрации.
На основании представлений Галлера для описания зависимости осмотического давления от концентрации полимеров было предложено уравнение:
![]() ,
,
где ![]() - второй вириальный коэффициент;
- второй вириальный коэффициент;
![]() - константа, характеризующая отклонения от уравнения Вант-Гоффа, зависящая от природы растворителя и растворенного вещества, но не зависящее от молекулярного веса растворенного вещества.
- константа, характеризующая отклонения от уравнения Вант-Гоффа, зависящая от природы растворителя и растворенного вещества, но не зависящее от молекулярного веса растворенного вещества.
Вязкость растворов, содержащих макромолекулы, обычно выше вязкости растворов НМС и коллоидных растворов тех же концентраций.
Отклонения вязкости растворов ВМС от законов, которым подчиняются растворы НМС, следует объяснить особенностями гидродинамики систем, содержащих вытянутые и гибкие макромолекулы и наличием в них ассоциатов и легко разрушаемых структур.
6. Определение молекулярной массы по вязкости их растворов
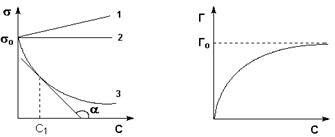
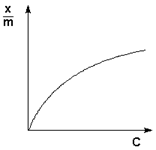
Приведенная вязкость растворов одного и того же полимера обычно возрастает с повышением концентрации, причем это возрастание в интервале небольших концентраций происходит по прямой.
Отрезок, отсекаемый этой прямой отвечает величине характеристической вязкости ![]() , отражающей гидродинамическое сопротивление потоку молекул данного полимера. Характеристическая вязкость представляет собой приведенную вязкость при бесконечно большом разбавлении раствора.
, отражающей гидродинамическое сопротивление потоку молекул данного полимера. Характеристическая вязкость представляет собой приведенную вязкость при бесконечно большом разбавлении раствора.
В настоящее время для определения молекулярного веса предложено уравнение, учитывающее взаимодействие макромолекул даже в разбавленных растворах и изменение константы ![]() с длиной молекулы:
с длиной молекулы:
![]() ,
,
где ![]() - коэффициент постоянный для растворов полимергомологического ряда в данном растворителе;
- коэффициент постоянный для растворов полимергомологического ряда в данном растворителе;
![]() - величина, характеризующая форму макромолекул в растворе и связанная с гибкостью цепи.
- величина, характеризующая форму макромолекул в растворе и связанная с гибкостью цепи.
Похожие работы
... «мицелла» и «мицеллярный раствор». Эти термины были использованы им для обозначения систем, образованных нестехиометрическими соединениями в водной среде. Основная заслуга в становлении коллоидной химии как науки принадлежит Т. Грэму. Как уже отмечалось выше, именно этому ученому принадлежит идея введения термина «коллоид», производного от греческого слова «kolla», обозначающего «клей». Занимаясь ...
... Расстояние, пройденное веществом по сорбенту, прямо пропорционально растворимости данного вещества в пропускаемом растворителе. Даёт возможность полностью разделять вещества, входящие в состав разделяемой смеси. Коллоидная химия Дисперсные системы – это системы, состоящие из множества частиц одной фазы (дисперсной), распределённых в объёме другой фазы – дисперсионной. Дисперсионная среда ...
... и многое другое, без чего немыслима сама жизнь. Все человеческое тело – это мир частиц, находящихся в постоянном движении строго по определенным правилам, подчиняющимся физиологии человека. Коллоидные системы организмов обладают рядом биологических свойств, характеризующих то или иное коллоидное состояние: 2.2 Коллоидная система клеток. С точки зрения коллоидно-химической физиологии ...
... металлов с белками, нуклеиновыми кислотами, липидами. Её практическое применение связано с синтезом фарамакологических препаратов, действие которых обусловленно комплексными ионами металлов. Биоорганическая Химия Изучает связь между строениями органических веществ и их биологическими функциями, использующих в основном методы органической и физической химии, а также физики и математики. ...
0 комментариев