Навигация
Полиэлектролиты и их свойства
7. Полиэлектролиты и их свойства
Полиэлектролиты – это ВМС, молекулы которых содержат гомогенные группы и в растворах способны распадаться на ионы. По природе содержащихся в них ионогенных групп можно разделить на три категории:
1. полиэлектролиты, содержащие кислотную группу ![]() . Первую группу содержат гуммиарабик, альгинаты, растворимый крахмал, а вторую – агар.
. Первую группу содержат гуммиарабик, альгинаты, растворимый крахмал, а вторую – агар.
2. полиэлектролиты, содержащие основную группу ![]() . Такие вещества в природе не встречаются, но могут быть синтезированы.
. Такие вещества в природе не встречаются, но могут быть синтезированы.
3. полиэлектролиты, содержащие одновременно как кислотную, так и основную группу (полиамфолиты). К ним относятся белки, синтетические полиамфолиты – сополимеры акриловой кислоты и винилпиридина, глютаминовой кислоты и лизина.
Полиэлектролиты, за исключением белков, характеризуются высокой плотностью расположения ионогенных групп – обычно на одно звено цепи приходится по одной ионогенной группе. Вследствие этого молекулы полиэлектролитов могут испытывать в растворе значительные электростатические взаимодействия, что приводит к значительной деформации цепей гибких молекул.
Все высокомолекулярные электролиты растворяются в полярных растворителях, т.к. макромолекулы с гомогенными группами взаимодействуют с полярными жидкостями сильнее, чем с неполярными.
Молекулы белков являются амфотерными соединениями, pH белков ниже 7, т.к. они являются более сильной кислотой, чем основанием.
8. Латексы и дисперсии полимеров. Их применение
Натуральные латексы представляют собой млечный сок бразильской гевеи, синтетические латексы получают путем полимеризации в водной среде непредельных углеводородов – бутадиена, хлоропрена и других мономеров.
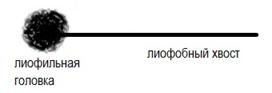
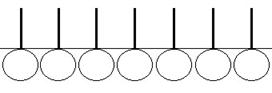
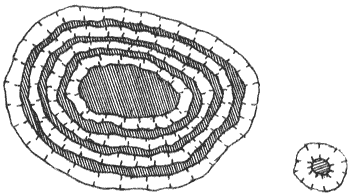
Латексы содержат макроскопические и ультра микроскопические частицы, приближающиеся по формуле к сферическим, на поверхности которых адсорбированы стабилизатор – соединения типа белков для натурального латекса и мыла али другие ПАВ у синтетических латексов. Вещество дисперсной фазы состоит из каучука, макромолекулы которого представляют собой гибкие углеводородные цепи, не содержащие или содержащие полярные группы.
Коллоидные системы с твердой дисперсионной средой называют твердые золи. Их можно разделить на системы с газовой, жидкой и твердой дисперсной фазой.
Системы с твердой дисперсионной средой и газовой дисперсной фазой часто называют твердыми пенами.
Системы с твердой дисперсионной средой и жидкой дисперсной фазой можно считать твердыми эмульсиями.
Наибольшее значение имеют системы твердой дисперсионной средой и твердой дисперсной фазой. Натуральные и синтетические латексы широко применяются для получения эластичных пленок, для изготовления эластичных пористых материалов, заменителей кожи, для пропитки корда в шинной промышленности и др.
V. Раздел «Представители гетерогенно – дисперсных систем»
1. Суспензии. Способы получения и стабилизации. Особенности суспензий и их применение
Суспензии – системы с твердой дисперсной фазой и жидкой дисперсионной средой, размеры частиц которых превышают коллоидные размеры.
Методы получения суспензий делят на физико-механические и физико-химические.
К физико-механическим относятся дробление и измельчение твердых материалов, и распыление жидких сред, т.е. диспергирование. В ходе осуществления этого метода химический состав материала не меняется. При физико-химических методах получения суспензий изменяется химический состав материала. К таким методам относятся восстановление оксидов и других металлов, электролиз водных растворов и расплавов солей и др.
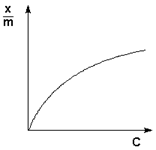
Суспензии одновременно поглощают и рассеивают свет, при этом в отличие от опалесцирующих золей суспензии проявляют мутность не только при боковом освещении, но и в проходящем свете. Суспензии, так же как и золи, способны проявлять двойное лучепреломление в потоке.
Поскольку частицы суспензий обладают сравнительно большими размерами, суспензии седиментационно неустойчивы, если плотность дисперсной фазы не очень близка к плотности дисперсной среды и вязкость этой среды не очень велика.
Для суспензий характерен ряд процессов, не свойственных коллоидным системам или протекающих у последних иначе, чем у суспензии. К таким процессам относятся седиментация, флотация, фильтрация и кольматация.
К суспензиям при достаточном содержании влаги относятся почвы и грунты, цементные и известковые растворы, применяемые в строительстве. Суспензиями являются взвеси пигментов в органических средах, применяющихся в качестве масляных красок и цветных лаков, взвеси графита и угля, используемые для создания центров кристаллизации с целью предотвращения образования накипи в котлах и т.д.
2. Эмульсии. Способы получения и стабилизации. Прямые и обратные эмульсии, обращение фаз в эмульсиях, эмульгаторы и деэмульгаторы. Применение эмульсии
Эмульсии – это дисперсные системы, образованные двумя взаимно нерастворимыми жидкостями. Их получают как конденсационными, так и диспергационными методами.
Отличительной особенностью не слишком концентрированных эмульсий является сферическая форма частиц.
Существуют лиофобные и лиофольные – критические эмульсии.
Критические эмульсии – это системы, образующиеся из двух ограниченно смешивающихся жидкостей при температурах, близких к критической температуре смешения, когда поверхностное натяжение на границе фаз становится весьма малым и тепловое движение молекул уже достаточно для диспергирования одной жидкости в другой.
Лиофобные эмульсии классифицируют:
- по полярности дисперсной фазы и дисперсной среды и различают:
1 эмульсии неполярной или слабополярной жидкости в полярной – эмульсии первого рода (прямые);
2 эмульсии полярной жидкости в неполярной – эмульсии второго рода (обратные).
- по концентрации дисперсной фазы в системе эмульсии делят на:
1 разбавленные эмульсии – системы жидкость-жидкость, содержащие до 0,1% дисперсной фазы, обладающие характерными свойствами;
2 концентрированные эмульсии – система жидкость-жидкость со сравнительно значительным содержанием дисперсной фазы, вплоть до 74 %.
3 Высококонцентрированные (желатинированные) эмульсии – с содержанием дисперсной фазы выше, чем 74 %. Их можно приготовить с очень большим содержанием дисперсной фазы и соответственно с ничтожным содержанием дисперсной среды.
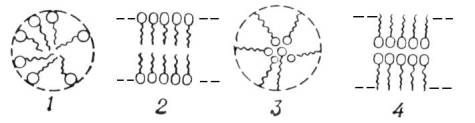
Эмульсии агрегативно неустойчивы из-за избытка свободной энергии на межфазной поверхности. На агрегативную устойчивость эмульсий сильнее всего влияют природа и содержание в системе эмульгатора. Эффективность эмульгатора характеризуется специальным числом – гидофильно-липофильным балансом. Если число ГЛБ лежит в пределах 3-6, образуется эмульсия обратная. Эмульгаторы с числом ГЛБ 8-13 дают прямую эмульсию.
Часто перед технологом стоит задача не получить эмульсию, а наоборот, предупредить ее возникновение или разрушить (деэмульгировать) уже образовавшуюся систему. Разрушение всех эмульсий можно достичь введением в систему ПАВ, вытесняющего из адсорбционного слоя эмульгатор, но неспособного стабилизовать эмульсию. Эмульсии можно также разрушить центрифугированием, фильтрованием, электрофорезом.
В пищевой промышленности к эмульсиям принадлежат молочные продукты, маргарин, майонез, различные соусы. В фармацевтической промышленности многие лекарства применяются в виде эмульсий.
3. Пены. Способы получения и стабилизации. Применение пен. Пеногашение
Пены свободнодисперсные системы, состоящие из газообразной дисперсной фазы и жидкой дисперсной среды.
Пены получают диспергационными и конденсационными методами. Пена получается при диспергировании газа в жидкость из узкого отверстия – струя газа разрывается и разбивается на пузырьки. Пена образуется и при механическом перемешивании газа с жидкостью, что можно наблюдать при флотации, стирки и др. процессах. Устойчивость пен обеспечивается с помощью стабилизаторов, в качестве которых применяется ПАВ.
Пены применяются при флотации, при стирке, в противопожарном деле.
4. Аэрозоли. Способы получения и стабилизации. Особенности аэрозолей и их применение. Необходимость и способы разрушения аэрозолей
Аэрозоли – дисперсные системы с газообразной дисперсной средой и взвешенными или жидкими частицами. По методам получения они подразделяются на:
· диспергационные, образующиеся при измельчении и распылении веществ;
· конденсационные, получаемые конденсацией из пересыщенных паров и в результате реакций, протекающих в газовой фазе.
По агрегатному состоянию и размерам частиц дисперсной фазы аэрозоли делят на:
· туманы – системы с жидкой дисперсной фазой, размер частиц 10-0,1мкм;
· пыли – системы с твердыми частицами размером больше 10мкм;
· дымы – размер твердых частиц, которых находится в пределах 10-0,001мкм.
В практике «дым» означает аэродисперсную систему, возникающую при сгорании топлива и содержащие твердые частицы сажи и золы и жидкие частицы продуктов перегонки топлива и капли воды, образовавшиеся в результате конденсации водяного пара.
Туманы имеют частицы правильной сферической формы, а пыли и дымы содержат твердые частицы самой разнообразной формы.
Аэрозоли – сравнительно сильно разреженные системы, обладающие малым коэффициентом внутреннего трения дисперсионной среды.
Аэрозоли, обладая при высокой дисперсности достаточной седиментационной устойчивостью, обычно являются весьма агрегативно-неустойчивыми системами, и в них всегда идет процесс коагуляции.
На скорость разрушения систем с газовой дисперсионной средой влияют такие факторы, как: частота столкновения частиц, полидисперсность, анизодиаметрическая форма частиц. Разрушение аэрозолей ускоряется при наличии в них противоположно заряженных частиц. Наоборот, если частицы аэрозолей обладают одинаковым по знаку и достаточно большим по величине зарядом, то наблюдается рассеяние частиц.
Природные аэрозоли – это облака и туманы, определяют выпадение осадков и в значительной степени обуславливают климат того или иного района. Пыльца растений, споры бактерий и плесени, а также легкие семена переносятся в природе в форме аэрозоля.
Литература
1. Пасынский А.Г. Коллоидная химия. М.: Высшая школа - 1968.
2. Кузнецов В.В. Физическая и коллоидная химия. М.: Высшая школа - 1968.
3. Воюцкий С.С. Курс коллоидной химии. – М.: Химия, 1975.
4. Фролов Ю.Г. Курс коллоидной химии. – М.: Химия, 1982.
5. Фридрихсберг Д.А. Курс коллоидной химии. – Л.: Химия, 1974.
Похожие работы
... «мицелла» и «мицеллярный раствор». Эти термины были использованы им для обозначения систем, образованных нестехиометрическими соединениями в водной среде. Основная заслуга в становлении коллоидной химии как науки принадлежит Т. Грэму. Как уже отмечалось выше, именно этому ученому принадлежит идея введения термина «коллоид», производного от греческого слова «kolla», обозначающего «клей». Занимаясь ...
... Расстояние, пройденное веществом по сорбенту, прямо пропорционально растворимости данного вещества в пропускаемом растворителе. Даёт возможность полностью разделять вещества, входящие в состав разделяемой смеси. Коллоидная химия Дисперсные системы – это системы, состоящие из множества частиц одной фазы (дисперсной), распределённых в объёме другой фазы – дисперсионной. Дисперсионная среда ...
... и многое другое, без чего немыслима сама жизнь. Все человеческое тело – это мир частиц, находящихся в постоянном движении строго по определенным правилам, подчиняющимся физиологии человека. Коллоидные системы организмов обладают рядом биологических свойств, характеризующих то или иное коллоидное состояние: 2.2 Коллоидная система клеток. С точки зрения коллоидно-химической физиологии ...
... металлов с белками, нуклеиновыми кислотами, липидами. Её практическое применение связано с синтезом фарамакологических препаратов, действие которых обусловленно комплексными ионами металлов. Биоорганическая Химия Изучает связь между строениями органических веществ и их биологическими функциями, использующих в основном методы органической и физической химии, а также физики и математики. ...
0 комментариев