Навигация
100 · 36,5
V конц. HCl =———————————— (4)
W конц. HCL ·р конц. HCL,
, где V конц.. HCL - объем исходной концентрированной соляной кислоты, мл
W конц. HCL - процентная концентрация исходной соляной кислоты, %
рконц. HCL - плотность соляной кислоты, г/мл (кг/л)
Отмерить с помощью цилиндра объемом 100 мл расчетный объем концентрированной соляной кислоты и влить через воронку в термостойкую мерную колбу объемом 1000 мл, предварительно наполненную на 1/3 дистиллированной водой. Содержимое колбы перемешать круговыми движениями в одном направлении. Затем объем раствора довести до метки дистиллированной водой. Закрыть колбу пробкой и перемешать, переворачивая колбу вниз-вверх. /10/
9.2 Приготовление 0,1Н соляной кислоты для титрования
Приготовление ведут из 1Н раствора соляной кислоты путем разбавления в 10 раз. Отмерить с помощью цилиндра 100 мл, приготовленного в п. 9.1., 1Н раствора соляной кислоты. В термостойкую мерную колбу объемом 1000 мл, предварительно наполненную на 1/2 дистиллированной водой. Влить через воронку 100 мл 1Н раствора соляной кислоты и перемешать содержимое круговыми движениями. Затем довести до метки дистиллированной водой, закрыть пробкой и перемешать, переворачивая колбу вверх-вниз. /10/
9.3 Определение точной концентрации приготовленных растворов соляной кислоты
Определение ведут с помощью отстандартизированного раствора 0,1Н гидроксида натрия методом обратного титрования. Пипеткой отобрать 10 мл отстандартизированного раствора 0,1Н гидроксида натрия и перенести в коническую мерную колбу для титрования объемом 100 мл, добавить 20-30 мл дистиллированной воды (отмерить мерным цилиндром или пипеткой) 2-3 капли индикатора (фенолфталеина). Титрование проводить приготовленным в п.9.2. 0,1Н раствором соляной кислоты до обесцвечивания розовой окраски. Титрование повторить не менее 3 раз. Нормальность соляной кислоты определять по формуле 5:
V Na OH · ∙NNa OH
NHCL =——————— (5), где
V HCL
N HCL - нормальность соляной кислоты
V HCL - объем 0,1Н соляной кислоты, пошедшей на титрование, мл
V NaOH - объем аликвоты гидроксида натрия, равный 10 мл
NNaOH- нормальность отстандартизированного раствора гидроксида натрия (используется 0,1Н раствор)
За окончательный результат принимается среднее арифметическое значение из серии проведенных параллельных титрований.
Для оценки концентрации 1Н соляной кислоты предварительно осуществить разведение в мерной колбе в 10 раз. Полученным раствором заполнить бюретку объемом 25 мл.
Титрование проводится аналогично методике, указанной в п. 9.3. Нормальность соляной кислоты определяется по формуле 6:
V NaOH · NNaOH· R
N HCL =———————————(6), где
VHCL
NHCL- нормальность соляной кислоты,
VNaOH- объем аликвоты гидроксида натрия, равный 10 мл,
NNaOH - нормальность отстандартизированного раствора гидроксида натрия (используется 0,1Н раствор)
VHCL - объем разведенной 0,1Н соляной кислоты, пошедший на титрование, мл,
R - число разведений, равное 10.
Содержимое колб перенести в склянки (бутыли) объемом 1000 мл, оформить этикетки, закрыть пробками. /10/
9.4 Приготовление 25% хлорида бария (BaCL2)
Взвесить 62,5 г хлорида бария на технических весах с точностью до 0,01 г. В термостойкую колбу объемом 250 мл налить около 100 мл дистиллированной воды и постепенно через воронку пересыпать навеску хлорида бария. Затем с помощью стеклянной палочки, или круговыми движениями в одном направлении, перемешать содержимое колбы. Полученному раствору дать отстояться, отфильтровать и слить в склянку (бутыль) объемом 300 мл. /5, 8,10,20/
9.5 Приготовление 3% оксалата аммония ((NH4) C2O4)
Взвесить 7,5 г оксалата аммония на технических весах с точностью до 0,01 г. В термостойкую колбу объемом 250 мл налить 100 мл дистиллированной воды и постепенно через воронку пересыпать навеску оксалата аммония. Затем с помощью стеклянной палочки, или круговыми движениями в одном направлении, перемешать содержимое колбы. Полученному раствору дать отстояться, отфильтровать и слить в склянку (бутыль) объемом 300 мл. /5,8,10,20/
9.6 Приготовление 16 % раствора карбоната натрия (Na2CO3)
Взвесить 95,2 г карбоната натрия на технических весах с точностью до 0,01 г. В термостойкую колбу объемом 1000 мл налить300 мл дистиллированной воды и, в несколько приемов (4-5) постепенно при перемешивании стеклянной палочкой добавить карбонат натрия. Затем прилить оставшиеся 200 мл дистиллированной воды. Процесс растворения карбоната натрия в воде является экзотермическим, поэтому его рекомендуется проводить при охлаждении водой на водяной бане или в кристаллизаторе. Полученному раствору дать отстояться, отфильтровать и слить в склянку объемом 500 мл.
Похожие работы
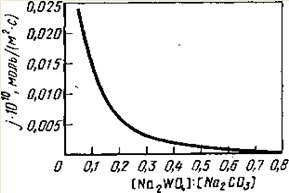
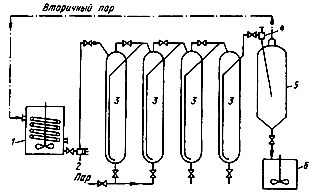
... в автоклавах, щелочи (для вольфрамита) и кислотами. Это позволяет интенсифицировать автоклавно-содовое разложение вольфрамовых концентратов, сократить расходы соды и в ряде случаев проводить процесс в одну стадию. Последнее увеличивает производительность автоклавов[4]. 4. Получение вольфрамового ангидрида 4.1 Переработка растворов вольфрамата натрия Растворы в, содержащие 60—150 г/л ...
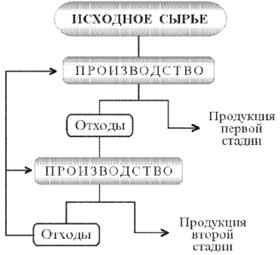
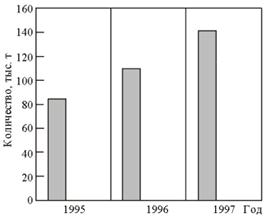
... отходам производства. В докладе «О состоянии окружающей природной среды Российской Федерации в 1997 году» Государственного комитета Российской Федерации по охране окружающей среды отмечается, что на начало 1997 г. на предприятиях различных отраслей промышленности накоплено 1431,7 млн. т токсичных отходов. За 1997 г. на промышленных предприятиях РФ образовалось 89,4 млн т токсичных отходов, из ...

0 комментариев