Навигация
Определение точной концентрации карбоната натрия
9.7 Определение точной концентрации карбоната натрия
Определение ведут с помощью ранее приготовленного и отстандартизированного раствора 1Н соляной кислоты (п. 9.1.). Для разбавления исходного раствора карбоната натрия пипеткой отобрать пробу объемом 20 мл, перенести в коническую мерную колбу объемом 100 мл и довести до метки дистиллированной водой. Колбу закрыть и раствор перемешать. Из разбавленного раствора пипеткой отобрать аликвоту 10 мл и перенести в коническую мерную колбу для титрования объемом 100 мл. Добавить 20-30 мл дистиллированной воды (отмерить мерным цилиндром или пипеткой) и 2-3 капли индикатора фенолфталеина. Титрование проводить 1Н соляной кислотой до перехода розовой окраски в бледно-розовую. Затем к этому титруемому раствору добавить 2-3 капли индикатора метилового - оранжевого и продолжить титрование 1Н соляной кислотой до перехода желто-оранжевой окраски в розовую. Титрование повторить не менее 3 раз.
Концентрация соды определяется по формуле 7:
Vk · Nk Vобщ. MNa2СО3
C Na2CO3 = ———————————— (7) , где
исх. р-рVал.Na2CO3 · V пробы · 2
C Na2 CO3 - концентрация карбоната натрия, г/л
исх. р-р
Nk- нормальность соляной кислоты (1Н)
Vk - общий объем 1Н соляной кислоты пошедшийна титрование аликвоты в присутствии индикаторов фенолфталеина и метилового - оранжевого, мл
V ал.Na2 CO3- объем аликвоты карбоната натрия, равный 10 мл
Vпробы - объем пробы исходного 16 % раствора карбоната натрия, взятый для разбавления, равный 20 мл
Vобщ.- объем приготовленного разбавленного раствора карбоната натрия, равный 100 мл
MNa2 CO3- молярная масса карбоната натрия, равная 106
За окончательный результат принимается среднее арифметическое значение из серии проведенных параллельных титрований. /5,10,17,20/
Данные анализов и расчетов оформить в табл. 2.
Таблица 2.Расчет концентрации исходного раствора карбоната натрия
| Общий объем приготовленного раствора, мл | Разбавление | Объем аликвоты, V ал Na2CO3, мл | Объем титранта соляной кислоты. Vк, мл | Концентрация титранта соляной кислоты, Nк г экв/ л | Концентр ация карбоната натрия, CNa2CO3,г/л исх, р-р | |
| Объем общий V общ., мл | Объем пробы V пробы, мл | |||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 |
Похожие работы
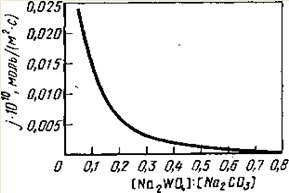
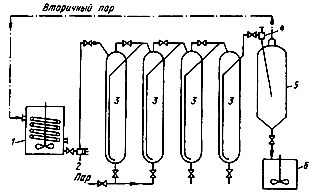
... в автоклавах, щелочи (для вольфрамита) и кислотами. Это позволяет интенсифицировать автоклавно-содовое разложение вольфрамовых концентратов, сократить расходы соды и в ряде случаев проводить процесс в одну стадию. Последнее увеличивает производительность автоклавов[4]. 4. Получение вольфрамового ангидрида 4.1 Переработка растворов вольфрамата натрия Растворы в, содержащие 60—150 г/л ...
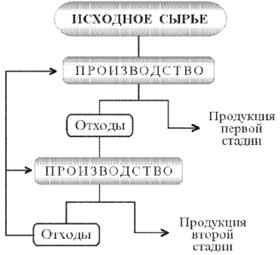
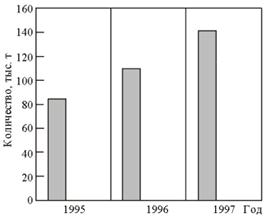
... отходам производства. В докладе «О состоянии окружающей природной среды Российской Федерации в 1997 году» Государственного комитета Российской Федерации по охране окружающей среды отмечается, что на начало 1997 г. на предприятиях различных отраслей промышленности накоплено 1431,7 млн. т токсичных отходов. За 1997 г. на промышленных предприятиях РФ образовалось 89,4 млн т токсичных отходов, из ...

0 комментариев