Навигация
Физические и химические свойства
4. Физические и химические свойства
Титан – металл, элемент IV группы периодической системы Д.И. Менделеева. Порядковый номер 22. Атомная масса 47,88. Изотопы: 48 (основной), 46, 47, 49, 50. Плотность 4,5 г/см3. Существует в двух полиморфных модификациях: ά-Ti – при температурах ниже 882˚С, β-Ti - выше 882˚C. При переходе ά→β изменение объема составляет +5,5%, тепловой коэффициент перехода 0,38 ккал/г-атом. Температура плавления титана 1665+5˚С. Температура кипения 3572˚С. Давление паров при 1200-2000 К:
![]()
Прочность на разрыв чистого (иодидного) титана составляет примерно 20 кГ/мм2, товарного титана 30-40 кГ/мм2, прочность конструкционных сплавов на основе титана равна обычно 100-120 кГ/мм2, в отдельных же случаях достигает 140 кГ/мм2 и выше.
Все элементы периодической системы по отношению к титану по их химическому воздействию можно разделить на четыре группы:
1. Элементы, не взаимодействующие с титаном: Li, Na, K, Rb, Cs, Fr, Mg. Ca, Sr, Ba, Ra и инертные газы.
2. Элементы, образующие с титаном химические соединения с ковалентной связью, не имеющие или имеющие малую растворимость в титане: H, F, Cl, Br, I, At, O, S, Se, Te, Po.
3. Элементы образующие с титаном соединения с металлическим характером связи (металлические соединения) и ограниченные твердые растворы: Cu, Ag, Zn, Cd, Hg, Be, Ga, In, Tl, B, Al, Th, C, Si, Ge, Sn, Pb, N, P, As, Sb, Bi, Mn, Te, Re, Fe, Co, Ni, Ru, Rh, Pd, Os, Ir.
4. Элементы, образующие с титаном β-модификации непрерывных твердых растворов: Zr, Hf, V, Nb, Ta, Cr, Mo, Sc, W.
Таким образом, титан так или иначе взаимодействует с с большинством элементов. Это, с одной стороны, создает значительные трудности при получении чистого титана и его сплавов, а , с другой стороны, дает возможность получать большое количество разнообразных по составу и свойствам сплавов.[7,c.5]
Титан – довольно активный металл; стандартный электродный потенциал системы Ti/Ti2+ равен -1,63 В. Однако благодаря образованию на поверхности металла плотной защитной пленки титан обладает исключительно высокой стойкостью против коррозии, превышающей стойкость нержавеющей стали. Он не окисляется на воздухе, в морской воде и не изменяется в ряде агрессивных химических сред, в частности в разбавленной и концентрированной азотной кислоте и даже царской водке.[1,c.649]
Титан при низкой температуре более устойчив к действию кислорода, чем железо, однако при нагревании на воздухе он сгорает до TiO2. С хлором титан реагирует примерно при 300˚C.[2,c.635]
В отличие от циркония и гафния титан растворяется при нагревании в соляной кислоте, образуя в восстановительной атмосфере аквакомплексы Ti(III):
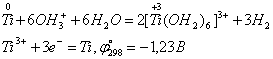
Растворы титана. В водных растворах Ti находится преимущественно в 4-валентном состоянии, но в определенных условиях существуют комплексы, в которых валентность титана равна трем. Малый ионный радиус позволяет ему приобретать заметную долю электронной плотности кислородного донора с образованием прочной ковалентной связи. Значения электроотрицательности для TiOH и TiO – 2,43 и 2,56 соответственно. Сродство ионов Ti+4 настолько велико, что комплексы практически всегда содержат кислород и образуют в растворах титана(IV) цепи с гидроксильными и кислородными мостиками.
Химия титана даже в разбавленных растворах оказывается связанной с процессами полимеризации.
В растворах титан может находиться в форме простых и комплексных ионов, а также в коллоидно-дисперсном состоянии. Превалирование той или иной формы зависит от условий получения и хранения раствора, его концентрации, содержания примесей и других факторов. Способность Ti вступать в типичные ионные реакции, например в окислительно-восстановительные, свидетельствует о том, что в растворах сернокислые соли диссоциирует на катионы и анионы. Так, превращение сульфата в хлорид при добавлении BaCl2:
Ti4++2SO42-+2Ba2++4Cl-=2BaSO4+Ti4++4Cl-
Происходит полно и ион Ti4+ не изменяется. Кристаллизация солей с четко выраженными стехиометрическими отношениями также является доказательством их ионной природы.
В водных сернокислых растворах существование ионов Ti4+ невозможно, так как Ti существует в виде гидратных комплексов Ti(H2O)64+, подвергающихся гидролизу с депротонизацией. С позиций представлений о льдоподобной структуре воды выполненные расчеты по данным кажущихся мольных объемов позволяют предполагать нахождение Ti(H2O)64+ как в каркасе структуры воды, так и в ее пустотах.
Прямых доказательств существования ионов титанила TiO2+ в растворе нет. Однако наличие TiO-группы в ряде соединений не вызывает сомнения. Термохимическим методом показано, что ион титанила обладает в растворе ярко выраженной положительной гидратацией. Гидратные числа, рассчитанные для Ti-форм при мольных соотношениях SO3 : Ti, равных 2 и 1, составляют 9и 5 соответственно, что близко к минимальным величинам для ионов U4+, Na+ и К+, найденным по данным числе переноса электролитов. С ростом концентрации титана гидратные числа уменьшаются и к моменту кристаллизации сульфатов становятся близкими к числу молекул Н2О на атом Ti, прочно связанных в твердой фазе.[6,c.66]
Гидролиз титансодержащих ионов или нейтральных молекул в сернокислых растворах – сложный физико-химический процесс. В нем различают несколько стадий: взаимодействие сульфатов титана с водой с их переходом в основные сульфаты, образование и рост мицелл гидроокиси, коагуляция мицелл с выпадением осадка. Процесс гидролиза сульфатов титана может быть представлен последовательными реакциями:
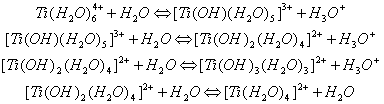
Титановая губка. При металлотермическом восстановлении четыреххлористого титана образуются отдельные кристаллы металла. Размер этих кристаллов колеблется от сотых долей микрона до 10мм и более. В процессе восстановления и при высокотемпературной выдержке отдельные кристаллы срастаются в губчатый блок, сохраняющий размеры и форму реакционного сосуда. Как и всякое пористое тело, титановая губка имеет большую удельную поверхность.
Попадая на воздух, эта поверхность контактирует с газами, входящими в состав воздуха. Титан является химически активным элементом и вступает во взаимодействие с окружающими его газами. Степень этого взаимодействия зависит от величины поверхности губки, характера взаимодействия титана с каждым из газов и температуры.
При дроблении, прессовании и других операциях губка нагревается до 250-300˚С. Это способствует ускорению химического взаимодействия титана с газами. Присутствие хлористых солей в губке делает ее контакт с воздухом более опасным, поскольку хлориды интенсивно поглощают воду. Эти свойства губки при определенных условиях проявляются настолько резко, что из высших сортов металла может быть получено изделие низкого качества или даже брак. Поэтому, явления связанные с загрязнением титановой губки в период ее пребывания на воздухе, требуют тщательного изучения и постоянного внимания.
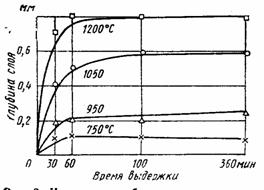
Взаимодействие титановой губки с кислородом. Титан взаимодействует с кислородом при всех температурах. При избытке кислорода образуется TiO2, в иных условиях возможно образование TiO и Ti2O3. Образовавшийся при комнатной температуре адсорбционный слой состоит из химически связанного кислорода и надстройки слабо связанных с поверхностью атомов газов. В начальный период процесса на скорость роста окисной пленки основное влияние оказывает температура. Окисление поверхности титана происходит главным образом в течение 1-2 ч. Дальнейшая выдержка при температурах до 300˚С приводит к незначительному изменению состояния поверхности. Это связано с защитными свойствами окисной пленки.
Процесс окисления титана на воздухе в интервале 20-300˚С можно разделить на три периода:
1. Образование окисной пленки при температуре до 50˚С; при этом увеличения содержания кислорода методом вакуум-плавления не обнаруживается.
2. Окисление титана в диапазоне температур от 60 до 140˚С; в этом интервале температур увеличение содержания кислорода подчиняется линейному уравнению
![]()
3. Окисление титана в диапазоне температур от 140 до 300˚С; в этом интервале температур увеличение содержания кислорода в титане выражается параболической зависимостью
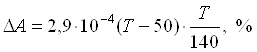
При температурах выше 400˚С структура пленки нарушается, и скорость окисления титана резко возрастает. Это связано с увеличением скорости диффузии ионов кислорода с поверхности в глубь металла. Окисление титана на воздухе протекает более интенсивно, чем в чистом кислороде. Это связано с присутствием азота, который способствует образованию дефектов в решетке окисла и повышает скорость окисления.
Взаимодействие титана с азотом. В результате взаимодействия титана с азотом образуется нитрид титана (TiN). Цвет нитрида титана изменяется от светло-коричневого до бронзово-желтого.
На воздухе до 300˚С титан незначительно взаимодействует с азотом. Этот факт подтверждает, что на воздухе прежде всего образуется окисная пленка, которая в значительной степени защищает титан от взаимодействия с азотом. При повышении температуры до 400˚С начинается некоторое растворение окисной пленки в глубь металла, происходит нарушение структуры поверхностной пленки, в результате чего взаимодействие титана с азотом воздуха интенсифицируется.
В среде азота взаимодействие титана с азотом при 20˚С обнаруживается только по изменению цвета поверхности металла.
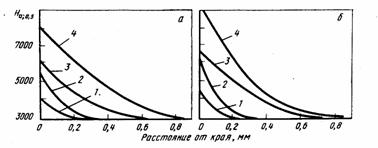
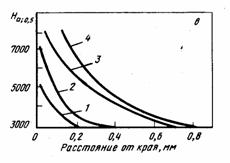
Азот способен растворяться в титане; до 550˚С диффузия ионов азота в глубь металла протекает медленно, но резко активизируется при 700˚С. Даже незначительное содержание азота в титане приводит к заметному увеличению его твердости. Азотирование является эффективным средством повышения износоустойчивости титана.
Взаимодействие титана с водой. При химическом взаимодействии титана с водой по схеме
![]()
Протекают одновременно два процесс: поглощение титаном водорода и образование окисных соединений.
Увеличение содержания кислорода в титановой губке при окислении в воде при температуре до 100˚С пропорционально квадрату температуры
![]()
Окисление титана в воде протекает интенсивно; увеличение содержания кислорода в титане в результате взаимодействия с водой более чем в десять раз превышает окисление на воздухе при тех же температурах, содержание водорода в титане после контакта с водой возрастает в 3-4 раза.
Взаимодействие титана с водородом. При взаимодействии титана с водородом образуется гидрид титана (TiH2). Кроме того, титан поглощает около 30% (ат.) водорода, который занимает октаэдрические пустоты решетки. Если адсорбировано незначительное количество водорода, то наблюдается только расширение кристаллической решетки без изменения типа ее структуры. Дальнейшая адсорбция создает значительное напряжение. Более богатой водородом фазе соответствует формула TiH2.
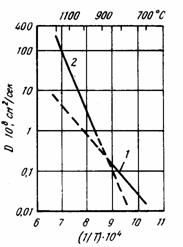
Адсорбированный при повышенных температурах водород не остается только на поверхности. Водород диффундирует в титан с очень большими скоростями. Так, например, при 500˚С коэффициент диффузии водорода в ά-титане составляет 1,5·10-5 см2/сек.
Высокая скорость диффузии водорода в титане определяет высокую интенсивность их взаимодействия. Диффузия водорода в титан происходит через щели и другие места нарушения структуры металла. За этим быстрым процессом следует медленная диффузия водорода и его растворение в металле с образованием твердого раствора. После того как образование твердого раствора будет закончено, значительное количество водорода может быть адсорбировано на поверхности межкристаллитных щелей, что приведет к поглощению водорода в количестве, большем стехиометрического.
Поглощение титаном водорода – процесс обратимый, при температуре выше 800˚С водород может быть полностью удален из титана.
Тщательная дегазация позволяет устранить один из продуктов реакции титана с водой, однако окисные соединения полностью остаются в металле и приводят к ухудшению его качества. В связи с тем, что первым этапом взаимодействия титана с водой является физическая адсорбция паров воды из воздуха, этому процессу должно быть уделено особое внимание.[7,c.236]
Похожие работы
... при больших значениях пленки получаются несплошные, легко отделяющиеся от поверхности металла (железная окалина) в результате возникающих внутренних напряжений. Поведение титана и его сплавов в различных агрессивных средах Реакции титана со многими элементами происходят только при высоких температурах. При обычных температурах химическая активность титана чрезвычайно мала и он практически ...
... были обнаружены в парах. Известен ряд двойных карбидов галлия различного состава с марганцем, железом, платиной, ниобием, хромом и некоторыми другими металлами. Соединения галлия с кремнием и бором не получены. 6. ОСОБЫЕ СВОЙСТВА ЭЛЕМЕНТА И ЕГО СОЕДИНЕНИЙ, ИХ ПРИМЕНЕНИЕ. Не стоит брать этот элемент в руки - тепла человеческого тела достаточно, чтобы этот серебристый мягкий (его можно резать ...
... и азота образуются нитриды железа состава Fe2N и Fe4N (N2+6Fe=Fe2N+Fe4N). При нагревании азота с ацетиленом C2H2 может быть получен цианистый водород HCN (N2+C2H2=2HCN). Из сложных неорганических соединений азота наибольшее значение имеют азотная кислота HNO3, ее соли нитраты, а также азотистая кислота HNO2 и ее соли нитриты. Получение В промышленности азот получают из воздуха. Для этого воздух ...
... выше сохранность поголовья на 4,6%, прирост живой массы на 7,0%, ниже затраты корма и себестоимость 1 кг прироста. Выводы На основании проведенных исследований по изучению влияния разных дозировок комплексоната титана на продуктивность цыплят-бройлеров можно сделать следующие выводы: Оптимальной дозой кормовой добавки комплексоната титана в рационе цыплят-бройлеров является 0,1 мг/кг живой ...
0 комментариев