Навигация
Классификация износостойких покрытий для режущего инструмента
6. Классификация износостойких покрытий для режущего инструмента.
6.1. Основные положения.
Все элементы Периодической системы подразделяются на группы электронных аналогов, атомы которых имеют аналогичные строения электронных оболочек:
- s-элементы, имеющие полностью заполненные внешние s-оболочки
- d- и f-элементы, имеющие незаполненные d- и f-оболочки
- sp-элементы, имеющие валентные s,p-электроны (неметаллы)
Данной классификация поясняет деление всех тугоплавких соединений, применяемых в качестве покрытий, на три группы:
- металлоподобные тугоплавкие соединения, образуемые d- и f-переходными металлами (бориды, карбиды, нитриды)
- металлоподобные тугоплавкие соединения, образуемые между собой в основном d- и f-переходными металлами, а также вырожденными металлами из sp-групп электронных аналогов
- неметаллические тугоплавкие соединения, образуемые взаимным сочетанием неметаллов (оксиды)
Наиболее широко в качестве износостойких покрытий применяются соединения тугоплавких d-переходных металлов IV-VI Периодической системы элементов с кислородом, углеродом и азотом [5]. Это связано с особенностями их кристаллохимического строения:
- Во-первых, эти металлы имеют недостаток электронов на внутренних s, p и d орбиталях, и это приводит к тому, что они с достаточной легкостью могут приобретать электроны из любого источника, которым может служить междоузельные атомы углерода, азота и кислорода.
- Во-вторых, большинство переходных металлов имеют достаточно большие атомные радиусы и при образовании соединений с атомами C,N и O могут подчинятся правилу Хэгга, согласно которому отношение радиуса атома неметалла к радиусу атома металла меньше критического значения 0.59. Для соединений металлов IV группы (Ti,Zr,Hf) достаточно точно выдерживается правило Хэгга, что приводит к образованию простых структур, в которых превалирует связь металл-металл, а атомы C,H,O можно рассматривать как вставленные в решетку атомов металла.
- В-третьих, большинство переходных металлов имеют широкие области гомогенности, что позволяет в зависимости от содержания кислорода, азота и углерода достаточно сильно изменять физико-механические свойства их карбидов, нитридов и оксидов.
- В-четвертых, переходные металлы и некоторые их соединения, в первую очередь соединения с простой кубической структурой типа NaCl (ZrC,ZrN,TiN,VC,TaC), отличаются очень высокими температурами плавления.
Соединения металлов IV-VI групп с кислородом, углеродом и азотом можно рассматривать и как наиболее устойчивый (в термодинамическом отношении) материал для покрытий, способный противостоять твердо- и жидкофазным диффузионным реакциям, коррозии и окислению при высоких температурах. Ниже будет показано, что свойства соединений тугоплавких металлов с О,N и С при обычных и повышенных температурах сильно зависят от многих факторов: состава (стехиометрии), наличия примесей, микроструктуры и текстуры, пористости и т.д.
6.2. Одноэлементные, однослойные покрытия.
6.2.1. Соединения, используемые в качестве покрытий.
Карбиды. Карбиды обладают рядом противоречивых свойств, что осложняет детальное изучение их физической природы. В частности, строение монокарбидов с кубической решеткой соответствует структуре типа NaCl , вместе с тем электропроводность карбидов сравнима с электропроводностью металлов. Высокая твердость карбидов проявляется за счет ковалентной связи атома углерода с атомом метала.
Наибольшая склонность к образованию энергетически стабильных конфигураций sp3 проявляются у карбидов металлов IV группы (Ti, Zr, Hf ). Это обусловлено большей донорской способностью этих металлов (особенно Ti) при относительно высоком содержании углерода в карбиде (до 20%). Стабильные конфигурации карбидов атомов металлов IV группы объясняется уменьшением общего числа нелокализованных электронов sp-переходов, смещения равновесия вправо и уменьшения общего числа нелокализованных электронов: sp2 + p « sp3. Поэтому карбиды обладают повышенной жесткостью кристаллической решетки, определяющей их высокую твердость, теплостойкость и хрупкость [5].
При переходе к карбидам V группы донорская способность металлов этой группы снижается, что приводит к снижению статистического веса устойчивости sp3-конфигурации карбидов и соответственно уменьшает соответственно твердость этих карбидов. Область их гомогенности сужается, в составе наряду с карбидами МС образуются низшие карбиды М2С с гексагональной структурой. Так например, твердость TiC равна 31.7 ГПа, а твердость TaC – 17.4 ГПа, Nb2C – 21 Гпа [5].
У карбидов тугоплавких металлов VI группы (Cr, Mo,W) содержание углерода падает до 6%, снижается число обобществленных электронов, поэтому статический вес атомов наиболее стабильной электронной конфигурации sp3 оказывается очень низким, а свойства карбидов определяются главным образом свойствами d5-конфигурации. Связи d5 более гибкие, чем sp3, допускают упругий прогиб решетки, более свободное движение в ней дислокаций. Поэтому карбиды металлов VI группы имеют меньшую твердость и хрупкость (CrC, MoC, WC), чем твердость и хрупкость карбидов IV группы (TiC, ZrC, HfC). Так твердость CrC равна 29.5 ГПа, а твердость ZrC – 29.5 ГПа [5] . Карбиды тугоплавких металлов V группы занимают промежуточное положение.
У карбидов VI группы имеются узкие области гомогенности. Образование карбидов таких металлов связано с сильными искажениями кристаллической решетки металла (Cr) либо с нарушением порядка упаковки (Mo, W). В следствии этого, у карбидов VI могут возникать и прямые связи C-C (MoC, CrC) [5].
Нитриды. По своим свойствам и строению нитриды весьма похожи на карбиды, однако, между ними существуют определенные различия. Главное различие состоит в сильном снижении связи металл – неметалл из-за уменьшения ковалентности азота (трехвалентный) по сравнению с валентностью углерода (четырехвалентный).
Атом азота в нитридах, имеющий в изолированном состоянии конфигурацию валентных электронов s2p6 , может быть как донором, так и акцептором электронов. Акцепторная способность азота преимущественно проявляется при образовании нитридов металла IV-VI групп, у которых преобладает ковалентно-металлическая ионная связь. Донорские способности тугоплавких металлов IV группы (особенно Ti) в результате присоединения трех атомов азота приводят к образованию энергетически очень устойчивых конфигураций s2p6: s2p3 + 3p « s2p6 [5].
Вследствие резкого снижения донорской и роста акцепторной способности металлов VI группы (Cr, Mo, W) для этой группы может проявляться и донорская способность азота (s2p3 ® sp4 ® sp3 + p ) с образованием избыточных (не участвующих в химической связи) электронов, которые снижают температуру плавления этих нитридов.
Хотя особенность конфигурационного строения нитридов переходных металлов (s2p6) свидетельствует о их высокой коррозионной стойкости (снижение склонности к твердо- и жидкофазным диффузионным реакциям), необходимо отметить меньшую термодинамическую устойчивость нитридов, по сравнению с карбидами. Практически это означает, что нитриды имеют более низкую по сравнению с карбидами сопротивляемость к высокотемпературному окислению, коррозии. Причем, при переходе нитридов металлов IV группы (TiN, ZrN, HfN) к нитридам металлов V (VN, NbN, TaN) и особенно VI группы (CrN, MoN, WN) сопротивляемость к высокотемпературному окислению снижается. Вместе с тем нитриды имеют и свои преимущества. Они более пластичны и менее хрупки, чем карбиды. Так например, предел прочности при изгибе TiN равен 240 МПа, а TiC – 15 МПа [5].
Оксиды. Оксиды обладают твердостью, сравнимой с твердостью нитридов. Так например, твердость TiN равна 20.5 ГПа, а твердость Al2O3 – 19.9 ГПа. Между тем, по коррозийным свойствам оксиды превосходят нитриды. Хрупкость оксидов сравнима с хрупкостью карбидов.
Похожие работы
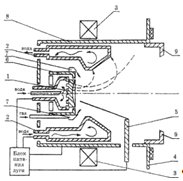
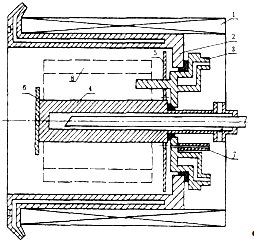
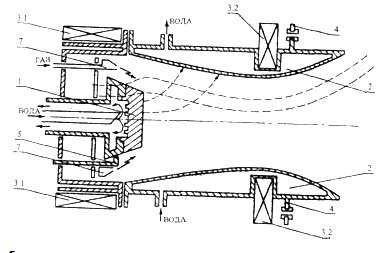
... даже по сравнению с ускорителем "Пуск-КуАИ" при существенном росте степени ионизации потока и кинетической энергии ионов. Рисунок 1.3 - Схема плазменного генератора с магнитной ловушкой электронов "Пуск-Мэл": 1 - катод; 2 - профилированный анод; 3.1 и 3.2 - соленоиды; 4 - фланец крепления генератора к вакуумной камере; 5 - электрод поджига дуги; 7 - канал подачи реакционных газов. Пунктиром ...
... отпуска может быть на 10–20оС ниже, а его продолжительность на 20–25% меньше, чем первого отпуска. Охлаждение после отпуска проводится на воздухе. 1.1.5 Влияние термической обработки на свойства штамповых сталей Служебные свойства штампового инструмента и его стойкость в значительной степени определяются соответствующим назначением марки стали, ее термообработкой и условиями эксплуатации ...
... ? 25. В чем сущность биохимических, фотохимических, радиационно-химических, плазмохимических процессов? Указать области их применения. 26. Какие основные группы физических процессов используют в системах технологий? 27. Дать определение машиностроению как комплексной области. Какова структура машиностроительного предприятия? 28. Раскрыть сущность понятий «изделие», «деталь», «сборочная единица ...
... ремонт оборудования. Защита от шума Борьба с шумом посредством уменьшения его в источнике является наиболее рациональной. Уменьшение механического шума может быть достигнуто путем совершенствования технологических процессов и оборудования. Расчет допустимого уровня шума Расчетная формула для определения уровня шума, если источник шума находится в помещении, будет иметь вид: , (4.1) где В ...






0 комментариев