Навигация
Федеральное агентство по образованию РФ
Государственное образовательное учреждение высшего профессионального образования
Тульский государственный университет
Кафедра химии
Курсовая работа
по неорганической химии
«Синтез тиоцианата ртути(ΙΙ)»
Выполнила студентка гр. 430481:
Родичева А. С.
Научный руководитель:
доцент кафедры химии Бородина Л. П.
Тула 2009 г.
Содержание
1. Введение
2. Литературный обзор
3. 2.1. Общая характеристика ртути
4. 2.1.1. Важнейшие характеристики ртути
5. 2.1.2. Получение ртути
6. 2.1.3. Применение ртути
7. 2.1.4. Отравление ртутью и ее соединениями
8. 2.2. Родан (SCN)2
9. 2.3. Тиоциановая кислота
10. 2.3.1. Важнейшие характеристики тиоциановой кислоты
11. 2.3.2. Получение HCSN
12. 2.3.3. Применение роданистоводородной кислоты
13. 2.4. Тиоцианаты не органические
14. 2.4.1. Общая характеристика некоторых тиоцианатов
15. 2.4.2. Получение тиоцианатов
16. 2.4.3. Комплексные соединения тиоцианатов
17. 2.4.4. Применение тиоцианатов
18. 2.5. Тиоцианат (роданид) ртути (ΙΙ
19. 2.5.1. Историческая справка
20. 2.5.2. Получение Hg(SCN)2
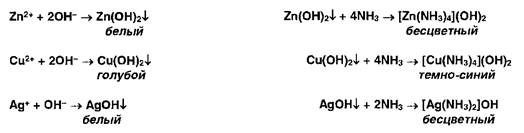
21. 2.5.3. Реакции характерные для Hg(SCN)2
22. 2.5.4. Применение тиоцианата ртути (ΙΙ
23. 2.6 Токсикологический аспект
3. Экспериментальная часть.
Выводы
5. Список используемой литературы
1. Введение
Целью данной курсовой работы является изучение способов синтеза тиоцианатов, в частности тиоцианат ртути (ΙΙ). Свойства соединений ртути(II) специфичны, поэтому они интересны для изучения.
Задачей данной работы является синтез тиоцианата ртути(II) и изучение его свойств.
Тиоцианаты щелочных металлов и аммония получают при улавливании цианистых соединений, содержащихся в коксовом газе, растворами соответствующих полисульфидов. Кроме того, NH4NCS получают взаимодействием NH3 с CS2, a KNCS и NaNCS получают сплавлением KCN или NaCN с серой. Другие тиоцианаты синтезируют обменной реакцией сульфатов, нитратов или галогенидов металлов с тиоцианатом Ba, К или Na, или взаимодействием гидроксидов или карбонатов металлов с HNCS. CuSCN получаются из тиоцианатов щелочных металлов, гидросульфита натрия и сульфата меди. Ca(SCN)2*3H2O получают действием оксида кальция на тиоцианат аммония.
2. Литературный обзор
2.1. Общая характеристика ртути
Ртуть – один из семи металлов, известных с древнейших времен. В металлическом состоянии Hg - серебристо-белого цвета и при комнатной температуре находится в жидком состоянии и при небольшом нагревании легко переходит в пар. [1]
Ртуть принадлежит к числу весьма редких элементов (в земной коре ее 4,5*10-6%. Примерно столько же Hg содержится в изверженных горных породах.) В земной коре Hg преимущественно рассеяна; осаждается из горячих вод, образуя ртутные руды (содержание в них ртути примерно 5-7%), известно 35 рудных минералов. В свободном виде она встречается в виде вкраплений в горные породы, но крайне редко, выделяется из морской воды. [2]
2.1.1 Важнейшие характеристики ртути
| Атомная масса | 200,59 |
| Валентные электроны | 5d106s2 |
| Радиус атома Э, нм | 0,160 |
| Радиус иона Э2+, нм | 0,112 |
| Энергия ионизации эВ | |
| Э→Э+ | 10,44 |
| Э+→Э2+ | 18,75 |
| Э2+→ Э3+ | 32,4 |
| Сродство к электрону эВ | 1,53 |
| Стандартная энтольпия атомизации | 61,5 (при 250С) |
| Плотность | 13,546 |
| Температура плавления 0С | - 38,89 |
| Температура кипения0С | 356,66 [3] |
| ΔH0возг,298, кДж/моль | 61 |
| S0298, Дж/(К*моль) | 75,9 [4] |
Особенностью электронного строения атома ртути является полностью сформированная «подвнешняя» d10 оболочка. Наличие замкнутой и поэтому очень стабильной d10 электронной оболочки обуславливается несклонностью ртути проявлять в своих гетерогенных соединениях более высокую степень окисления, чем 2+. Вместе с тем валентные возможности ртути очень обширны, благодаря легкой деформируемости все той же d10 электронной оболочки. Возникающий в результате деформации дополнительный эффект поляризации делает возможным образование ковалентных связей, что резко расширяет круг реализуемых реакций и соединений.[4]
Похожие работы
... вплоть до состояния sp3. Однако получить макроскопическое количество кристаллического нитрида углерода до настоящего времени таким способом не удавалось [3]. Сложность термобарического синтеза кристаллического нитрида углерода заключается в том, что неизвестна область его термодинамической стабильности. Иными словами неизвестно, насколько велики должны быть давление и температура синтеза для ...
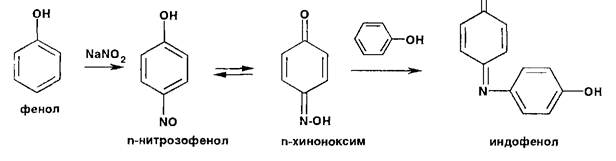
... , а затем строят калибровочный график, с помощью которого выполняют расчеты. Спектрофотометрия в УФ- и видимой областях — один из наиболее широко используемых физико-химических методов в фармацевтическом анализе. Анализируемые ЛВ должны иметь в структуре молекулы хромофорные группы (сопряженные связи, ароматическое ядро и др.), обусловливающие различные электронные переходы в молекулах и ...
... и, конечно же, за многими другими, которые будут получены, — будущее. В этом направлении и работают многие НИИ и исследователи. Аспекты поиска новых лекарств, изыскание новых лекарственных веществ состоит из трех основных этапов: химический синтез, установление фармакологической активности и безвредности (токсичности). Такая стратегия поиска с большой затратой времени, реактивов, животных, труда ...
... , основанной на поглощении атомами рентгеновского излучения. Ультрафиолетовая спектрофотометрия — наиболее простой и широко применяемый в фармации абсорбционный метод анализа. Его используют на всех этапах фармацевтического анализа лекарственных препаратов (испытания подлинности, чистоты, количественное определение). Разработано большое число способов качественного и количественного анализа ...
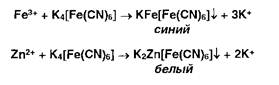

0 комментариев