Навигация
Определяем степени окисления элементов, которые изменили ее в процессе реакции
2. Определяем степени окисления элементов, которые изменили ее в процессе реакции
Sb2S2-5 + HN5+O3 = H3SbO4+N2+O+H2S6+O4 .
3.Определяем изменения, происшедшие в значениях степени окисления и устанавливаем окислитель и восстановитель.
В данной реакции степень окисления атомов серы S2- повысилась с 2- до 6+; следовательно, S2- является восстановителем. А степень окисления атомов азота N5+ понизилась с 5+ до 2+; следовательно, N5+ является окислителем. На основании этого составляем схему электронного баланса реакции:
N5+ + 3e® N2+ │ 40 окислитель, процесс восстановления
S2- - 40e ® S6+ │ 3 восстановитель, процесс окисления
Пользуясь правилом электронного баланса, определяем общее число перемещающихся электронов нахождения наименьшего кратного. В данном случае оно равно 120.
4. Находим основные коэффициенты, то есть коэффициенты при окислителе и восстановителе
3 Sb2S5 + 40 HNO3 = H3SbO4 + NO + H2SO4 .
5. Согласно закону сохранения массы расставляем коэффициенты в правой части уравнения (продукты реакции) перед окисленной и восстановленной формами:
3 Sb2S5 + 40 HNO3 = H3SbO4 + 40 NO + 15 H2SO4 .
6. Проверяем число атомов каждого элемента (кроме водорода и кислорода) в исходных веществах и продуктах реакции и подводим баланс по этим элементам, расставляя коэффициенты:
3 Sb2S5 + 40 HNO3 = 6 H3SbO4 + 40 NO + 15 H2SO4 .
7. Проверяем число атомов водорода в левой и правой частях уравнения и определяем число участвующих в реакции молекул воды
3 Sb2S5 + 40 HNO3 + 4 Н2О = H3SbO4 + 40 NO + 15 H2SO4 .
8. Проверяем сумму атомов кислорода в левой и правой частях уравнения. Если баланс по кислороду сходится, то уравнение реакции составлено правильно.
Все вышеописанные операции производятся последовательно с одним и тем же уравнением и переписывать реакцию несколько раз не имеет смысла. Уравнение реакции окисления сульфида сурьмы азотной кислотой, с учетом схемы электронного баланса, запишется следующим образом:
3 Sb2S5 + 40 HNO3 + 4 Н2О = H3SbO4 + 40 NO + 15 H2SO4 .
| 3 | 5S2- - 40ē = 5S6+ | восстановитель (окисление) |
| 40 | N5+ + 3ē = N2+ | окислитель (восстановление) |
Особые случаи составления уравнений окислительно-восстановительных реакций
Рассмотренная методика составления окислительно-восстановительных реакций применима к большинству простых и сложных процессов. Но в некоторых специальных случаях необходимы дополнительные пояснения.
1. Если число электронов, отдаваемое восстановителем, и число электронов, присоединяемое окислителем, имеют общий наибольший делитель, то при нахождении коэффициентов оба числа делят на него. Например, в реакции
HCl7+O4 + 4S4+O2 + 4H2O = 4H2S6+O4 + HCl1-
основными коэффициентами для восстановителя и окислителя будут не 6 и 2, а 4 и 1.
Если число участвующих в реакции электронов нечетно, а в результате получается четное число атомов, то коэффициенты удваиваются. Например, в реакции
2Fe3+Cl3 + 2HJ1- = J20 + 2Fe2+Cl2 + 2HCl
основными коэффициентами будут не 1 и 1, а 2 и 2.
2. Окислитель или восстановитель иногда дополнительно расходуется на связывание получающихся продуктов (солеобразование).
Например, в реакции
Cu + 2HNO3 + 6HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
на окисление на связывание на 3 атома восстановителя Сu0 требуется для окисления 2 молекулы окислителя HNO3; кроме того, на образование нитрата меди - трех молекул - требуется еще 6 молекул HNO3 для связывания трех атомов меди. Таким образом, общий расход азотной кислоты: 2 молекулы на окисление плюс 6 молекул на связывание (солеобразование), то есть всего 8 молекул HNO3. И окончательно уравнение примет вид:
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O.
З. Если в реакции число элементов, изменяющих свою степень окисления, больше двух, то устанавливают общее число электронов, отдаваемых восстановителями, и общее число электронов, присоединяемых окислителями, а в остальном соблюдается общий порядок составления уравнения реакции. Например,
3As3+2S2-3 + 28HN5+O3 + 4H2O ® 6H3As5+O4 + 9H2S6+O4 + 28N2+O
![]()
![]() 2As3+ - 4e ® 2As5+ -28e 3
2As3+ - 4e ® 2As5+ -28e 3
![]() 3S2- - 24 ® 3S6+
3S2- - 24 ® 3S6+
N5+ + 3e ® N2+ +3e 28
4. Оба элемента – и окислитель, и восстановитель – находятся в одной и той же молекуле. Это реакция внутримолекулярного окисления-восстановления и реакции диспропорционирования. Для удобства подбора коэффициентов в этом случае иногда можно рассматривать процесс как бы идущим справа налево. Например,
3HN3+O2 ® HN5+O3 + 2 N2+O + H2O
![]() N3+ + e ® N2+ 2
N3+ + e ® N2+ 2
N3+ - 2e ® N5+ 1
Классификация окислительно-восстановительных реакций
Реакции межмолекулярного окисления-восстановления – это реакции, в которых атом-окислитель и атом-восстановитель принадлежат разным веществам. Эти вещества могут быть как простыми, так и сложными.
4N3-H3 + 3O02 ® 2N02 + 6H2O2-
![]() 2N3- - 6e ® N02 2 восстановитель
2N3- - 6e ® N02 2 восстановитель
O02+ 4e ® 2O2- 3 окислитель
Реакции внутримолекулярного окисления-восстановления – это реакции, в которых атом-окислитель и атом-восстановитель входят в состав одной и той же молекулы или одного и того же иона.
Например, разложение хлората калия2KCl5+O2-3 ® 2KCl- + 3O02
![]() Cl5+ + 6e ® Cl- 2 окислитель
Cl5+ + 6e ® Cl- 2 окислитель
2O2- -4e ® O02 3 восстановитель
Реакции диспропорционирования (самоокисление– самовосстановление) - это реакции, в которых функцию окислителя и восстановителя выполняет один и тот же атом молекулы или иона, находящийся в промежуточной степени окисления. Например:
![]()
![]() 4KCl5+O3 ® 3 KCl7+O4 + KCl-
4KCl5+O3 ® 3 KCl7+O4 + KCl-
Cl5+ - 2e ® Cl7+ 6 3 восстановитель
Cl5+ +6e ® Cl- 2 1 окислитель
Реакции конмутации – реакции внутримолекулярного окисления- восстановления, в результате которых происходит выравнивание степеней окисления атомов одного и того же элемента. Например:
N3-H4N5+O3 = N21+O + 2H2O
Влияние среды на протекание окислительно-восстановительных реакций
Реакции окисления-восстановления могут протекать в различных средах (кислой, нейтральной и щелочной), при этом в зависимости от среды может изменяться характер протекания реакции между одними и теми же веществами. Рассмотрим взаимодействие перманганата калия с сульфитом калия в различных средах.
а) Кислая среда:
2KMn7+O4 + 5K2S4+O3 + 3H2SO4 ® 2Mn2+SO4 + 6K2S6+O4 + 3H2O
![]() Mn7+ + 5e ® Mn2+ 2
Mn7+ + 5e ® Mn2+ 2
S4+ - 2e ® S6+ 5
б) Нейтральная среда:
2KMn7+O4 + 3K2S4+O3 + H2O ® 2Mn4+O2 + 3K2S6+O4 + 2KOH
![]() Mn7+ + 3e ® Mn4+ 2
Mn7+ + 3e ® Mn4+ 2
S4+ - 2e ® S6+ 3
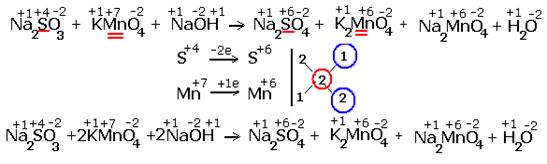
в) Щелочная среда:
2KMn7+O4 + K2S4+O3 + 2KOH ® K2Mn6+O4 + 2K2S6+O4 +H2O
![]() Mn7+ + e ® Mn6+ 2
Mn7+ + e ® Mn6+ 2
S4+ - 2e ® S6+ 1
Схематически это можно представить следующим образом:
Окисленная Восстановленная форма
Форма
![]()
![]() Mn2+ - бесцветный
Mn2+ - бесцветный
![]() Mn7+ ®MnО2- бурый осадок
Mn7+ ®MnО2- бурый осадок
![]() MnО42- - зеленый
MnО42- - зеленый
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Опыт 1. Окислительные свойства перманганата калия в разных средах.
а) Окисление сульфита натрия (Na2SO3) перманганатом калия (KMnO4) в кислой среде.
Налить в пробирку несколько капель (2 – 3) раствора перманганата калия, такой же объем 2Н раствора H2SO4, затем по каплям прибавлять сульфит натрия до полного обесцвечивания раствора.
В какую степень окисления переходит Mn+7 в кислой среде? Написать уравнение реакции, расставить коэффициенты и указать какую функцию выполняет в ней сульфит натрия и серная кислота.
б) Окисление сульфита натрия (Na2SO3) перманганатом калия (KMnO4) в нейтральной среде.
Налить в пробирку несколько капель (3 – 5) раствора перманганата калия и примерно такой же объем сульфита натрия. Как меняется в этом случае цвет раствора? Какое соединение образовалось в осадке? Какая степень окисления марганца устойчива в щелочной и слабоосновной среде? Написать уравнение реакции и расставить коэффициенты.
в) Окисление сульфита натрия (Na2SO3) перманганатом калия (KMnO4) в щелочной среде.
Налить в пробирку 3 - 4 капли концентрированного раствора NaOH или KOH, такой же объем сульфита натрия (Na2SO3), затем 2 – 3 капли раствора KMnO4. Как изменилась окраска раствора? Какой ион придает раствору такую окраску? Напишите уравнение реакции и расставьте коэффициенты.
На основании опытов а, б, в сделать общий вывод о характере продуктов восстановления перманганат-иона в зависимости от рН среды. В какой среде перманганат-ион проявляет более высокую окислительную активность?
Опыт 2. Окислительные свойства дихромата калия (K2Cr2O7).
а) Окисление сульфата железа (II) дихроматом калия.
Налить в пробирку 2 – 3 капли раствора дихромата калия (K2Cr2O7) и столько же 3Н раствора H2SO4, после чего по каплям приливать раствор сульфата железа (FeSO4). Пока дихромат-ионы полностью не прореагируют, оранжевый их цвет в сочетании с цветом образовавшихся гидратированных ионов хрома (III), образует бурый раствор. Поэтому добавление по каплям раствора сульфата железа (II) следует вести до достижения устойчивой окраски. В какой цвет окрашен раствор? Какую функцию выполняет в этой реакции сульфат железа (II)?
Написать уравнение реакции и расставить коэффициенты.
б) Окисление сульфита натрия (Na2SO3) дихроматом калия (K2Cr2O7).
Приготовить в пробирке, как в предыдущем опыте, раствор дихромата калия (K2Cr2O7), подкисленный серной кислотой, и прибавлять к нему по каплям раствор сульфита натрия (Na2SO3) до достижения устойчивой окраски. Написать уравнение реакции, расставить коэффициенты и указать окислитель и восстановитель.
Опыт 3. Окислительно-восстановительные свойства соединений элементов, находящихся в промежуточной степени окисления.
Для того чтобы убедиться в окислительно-восстановительной двойственности нитрита натрия (NaNO2), надо:
а) в одну пробирку поместить 3 – 4 капли раствора перманганата калия (KMnO4), подкислить раствор разбавленным раствором серной кислоты и добавить раствор нитрита натрия (NaNO2) до обесцвечивания раствора;
б) в другую пробирку внести 3 – 4 капли раствора иодида калия (KI), подкислить разбавленным раствором серной кислоты и добавить раствор NaNO2 до изменения окраски.
Как объяснить наблюдаемые явления? Написать уравнения реакций. В каком случае нитрит-ионы проявляют восстановительные и в каком окислительные свойства? При восстановлении нитрит-ионов выделяется азот, а при их окислении образуются нитрат-ионы.
Опыт 4. Внутримолекулярные окислительно-восстановительные процессы
а) Внутримолекулярное окисление-восстановление дихромата аммония ((NH4)2Cr2O7).
На железную или керамическую пластинку поместить 2 – 3 грамма дихромата аммония ((NH4)2Cr2O7), для начала реакции нагреть, после чего прекратить нагревание. Обратить внимание на особенности протекания реакции и ее продукты – газообразные (азот и пары воды) и твердый (Cr2O3 его цвет).
Написать уравнение реакции, расставить коэффициенты и указать окислитель и восстановитель.
б) Внутримолекулярное окисление-восстановление нитрата меди (II).
В пробирку внести несколько кристаллов нитрата меди (Cu(NO3)2∙3H2O). Закрепить пробирку в штативе и осторожно нагревать, наблюдая изменение цвета кристаллов и цвета выделяющегося газа. Написать уравнение реакции разложения нитрата меди (II), учитывая окраску возможных продуктов реакции: безводный Cu(NO3)2 – белый; Cu(NO2)2 – не существует; CuO – черный; Cu – красный; N2, NO, и О2 – бесцветные газы; NO2 – бурый газ.
Указать окислитель и восстановитель в молекуле нитрата меди (II).
КОНТРОЛЬНЫЕ ЗАДАНИЯ
Подберите коэффициенты методом электронного баланса в уравнениях реакций, укажите окислитель и восстановитель.
1. K2MnO4 + H2O = KMnO4 +MnO2 +KOH
2. PbS + H2O2 = PbSO4 + H2O
3. NaBrO3 +NaBr + H2SO4 = Br2 + Na2SO4 + H2O
4. CuI +H2SO4 +KMnO4 = CuSO4 + I2 +MnSO4 +K2SO4 +H2O
5. CaH2+ H2O = Ca(OH)2 + H2
6. Na3[Cr(OH)6] + NaOH +PbO2 = Na2CrO4 +H2O + Na2[ Pb(OH)4]
7. Cr(NO3)3 = Cr2O3 + NO2 + O2
8. Fe2O3 + KNO3 + KOH = K2FeO4 + KNO2 +H2O
9. Cr2O3 + Na2CO3 + O2 = Na2CrO4 + CO2
10. Na2SO3 = Na2S + Na2SO4
11. Cr2O3 + NaNO3 + NaOH = Na2CrO4 + NaNO2 + H2O
12. K2Cr2O7 +H2S + H2SO4 = Cr2(SO4)3 + S + K2SO4 + H2O
13. Br2 + SO2 + H2O = HBr + H2SO4
14. H2S + H2SO3 = S + H2O
15. KMnO4 + NaNO2 + H2O = MnO2 + NaNO3 + KOH
16. NaBr + NaBrO3 + H2SO4 = Na2SO4 + Br2 + H2O
17. As + Cl2 + H2O = H3AsO4 + HCl
18. K2Cr2O7 + HBr = Br2 + CrBr3 + KBr + H2O
19. KClO3 + HCl = KCl + Cl2 + H2O
20. FeCl2 + KClO3 + HCl = FeCl3 + KCl + H2O
21. Cr2(SO4)3 + H2O2 + NaOH = Na2CrO4 + Na2SO4 + H2O
22. Mg + HNO3 = Mg(NO3)2 + N2 + H2O
23. KMnO4 + H2S + H2SO4 = MnSO4 + S + K2SO4 + H2O
24. Zn + H2SO4 = H2S + ZnSO4 + H2O
25. KMnO4 + H3PO3 + H2SO4 = MnSO4 + H3PO4 + K2SO4 + H2O
ЛИТЕРАТУРА
1. Глинка Н.Л. Общая химия. / Н.Л. Глинка. М.: Химия, 1985. 740 с.
2. Ахметов Н.С. Общая и неорганическая химия./ Н.С.Ахметов. М.: Высшая школа, 1988. 446 с.
3. Степин Б.Д. Неорганическая химия. / Б.Д. Степин, А.А. Цветков. М.: Высшая школа, 1994. 608 с.
4. Потапова С.А. Окислительно-восстановительные реакции: – учеб. пособие по химии для слушателей фак-та довузовской подготовки. Саратов: изд-во СГТУ, 1997. 23 с.
Похожие работы
... , а в нейтральных и щелочных растворах ионы О реагируют с образованием гидроксид-ионов НОН + О = 2ОН . Применяются в основном два метода составления уравнений окислительно-восстановительных реакций: 1) электронного баланса – основан на определении общего количества электронов, перемещающихся от восстановителя к окислителю; 2) ионно-электронный – предусматривает раздельное ...
... окисления химических элементов. Подчёркнуты химические элементы, в которых изменились степени окисления. 2.Составляем электронные уравнения, в которых указываем число отданных и принятых электронов. За вертикальной чертой ставим число электронов, перешедших при окислительном и восстановительном процессах. Находим наименьшее общее кратное ( взято в красный кружок). Делим это ...
... электроны, понижает свою степень окисления, восстанавливается, а вещество Red2 с меньшим сродством к электрону (восстановитель) окисляется. Окисленная и восстановленная формы реагирующих в ОВР веществ образуют окислительно-восстановительные (оксред-, редокс-) пары ОХ1/Red1 и OX2/Red2, а превращения типа OX+ze - Red называют оксред - (редокс) - переходами или окислительно-восстановительными ...
... - + 14H+ → 2MnO4- + 5Bi3+ + 7H2O №37: 3HNO2 = HNO3 + 2NO + H2O Восстановитель: HNO2 Окислитель: HNO2 Данная окислительно-восстановительная реакция относится к реакциям диспропорционирования, т.к. молекулы одного и того же вещества (HNO2) способны окислять и восстанавливать друг друга. Это происходит потому, что вещество HNO2 содержит в своем составе атомы азота в промежуточной ...
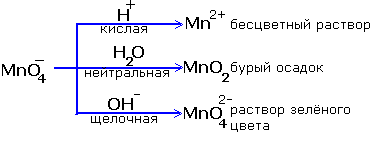
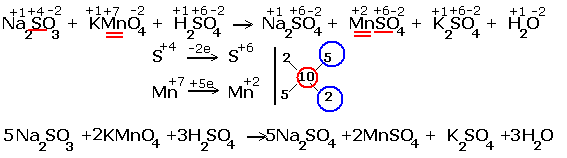
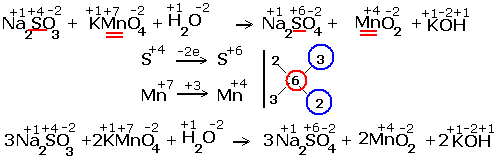
0 комментариев