Навигация
2. Нормативные ссылки
В настоящем стандарте использованы ссылки на следующие стандарты, методические указания и федеральные законы:
Федеральный закон N 85-ФЗ "О лекарственных средствах" от 22.06.98.
ГОСТ 17527-86. Упаковка. Термины и определения.
ОСТ 64-504-96. Контроль качества лекарственных средств на промышленных предприятиях и организациях. Основные положения.
ОСТ 42-510-98. Правила организации производства и контроля качества лекарственных средств (GMP).
ОСТ 91500.05.001-00. Стандарты качества лекарственных средств. Основные положения
МУ 64-01-001-2002. Производство лекарственных средств. Термины и определения.
ГОСТ Р 52249-2004. Правила производства и контроля качества лекарственных средств.
Примечание – При пользовании настоящим стандартом целесообразно проверить действие ссылочных документов.
Если ссылочный документ заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться замененным (измененным) документом.
Если ссылочный документ отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3. Термины и определения
В настоящем документе применяют следующие термины с соответствующими определениями:
3.1 Фармацевтическое предприятие - промышленное предприятие по производству лекарственных веществ, лекарственных средств и/или лекарственных форм.
3.2 Лекарственное вещество - вещество, обладающее лечебными или профилактическими свойствами и предназначенное для изготовления лекарственных средств
3.3 Полупродукт - частично обработанное сырье или лекарственные вещества, которые должны пройти дальнейшие стадии производственного процесса, прежде чем они станут лекарственным средством
3.4 Готовый продукт (finished product) - лекарственное вещество, прошедшее все стадии производственного процесса, включая упаковку и маркировку
3.5 Готовое лекарственное средство - лекарственное средство, предназначенное для отпуска индивидуальному потребителю в удобной для применения (дозированной) форме.
Брак (забракованная продукция) - продукт, изготовленный с нарушением требований технологической документации и/или не соответствующий требованиям нормативной документации
3.6 Отходы - побочные продукты, получаемые в процессе производства готового продукта
3.7 Сырье - исходные вещества и материалы, используемые для получения готового продукта, за исключением упаковочных и маркировочных материалов
3.8 Вспомогательные материалы - вещества и материалы, используемые в процессе производства готового продукта, но не предназначенные для отдельного использования как лекарственные средства.
3.9 Упаковочный материал (packaging material) - любой материал, используемый для упаковки или дозировки, а также для хранения готовых лекарственных средств (за исключением транспортной тары).
Упаковочные материалы подразделяются на:
-материалы первичной упаковки, непосредственно соприкасающиеся с лекарственными формами (ампулы, флаконы, пробки, крышки, банки, тубы, прокладки и др.);
-материалы вторичной упаковки, используемые для упаковывания готовых лекарственных форм (коробки, картон, пленка, фольга и др.)
3.10 Серия (batch, lot) - определенное количество однородного готового продукта, изготовленного за один производственный цикл при постоянных условиях
3.11 Номер серии - цифровое, буквенное или буквенно-цифровое обозначение, которое специфически идентифицирует серию и позволяет определить всю последовательность производственных и контрольных операций, ведущих к получению данной серии
3.12 Срок годности - период времени, в течение которого гарантируется соответствие качества готового лекарственного средства требованиям нормативной документации.
Кроме того, в соответствии со сроком годности, маркировка должна содержать указание об истечении срока годности (expiry date)
3.13 Кодирование - система записи, обеспечивающая автоматизированную идентификацию готового продукта
3.14 Качество (quality) - совокупность признаков, определяющих свойства готового продукта, его соответствие предназначенному применению и основным параметрам технологического процесса, включенным в регистрационные материалы
3.15 Карантин (quarantine) - статус сырья, вспомогательных, упаковочных, маркировочных материалов, полупродуктов и готового продукта, который предполагает их хранение отдельно или каким-либо иным эффективным способом исключает их применение или реализацию до тех пор, пока не будет принято решение о выдаче разрешения на их использование: реализацию, отбраковку или переработку
3.16 Производство (производственный процесс; manufacture) - все операции по производству готовых лекарственных средств, начиная от приобретения сырья, вспомогательных, упаковочных и маркировочных материалов и полупродуктов, до изготовления и упаковки, включая выдачу разрешения на реализацию, хранение, реализацию и транспортирование готовых лекарственных средств и относящиеся к этому виды контроля, включая контроль качества готового продукта
3.17 Упаковка (packaging) - все технологические стадии и операции по заполнению упаковочных материалов и маркировке, которые должен пройти полупродукт, чтобы стать готовым продуктом.
Заполнение первичной упаковки при производстве стерильных лекарственных средств (фасовка или розлив в материалы первичной упаковки), как правило, не относится к стадии упаковки.
Наполненные, но окончательно не упакованные материалы первичной упаковки, следует считать полупродуктами
3.18 Контроль процесса производства (in-process control) - виды контроля, включая постадийный контроль, выполняемые во время производства с целью наблюдения за производственным процессом и при необходимости корректировки технологических параметров для обеспечения соответствия качества готового продукта требованиям нормативной документации
Контроль окружающей среды и чистоты оборудования являются также частью контроля процесса производства
3.19 Валидация (validation) - документированное подтверждение соответствия оборудования, условий производства, технологического процесса, качества полупродукта и готового продукта действующим регламентам и/или требованиям нормативной документации
4. Общие положения
4.1 На предприятии должно быть необходимое количество персонала, имеющего соответствующее образование и способного выполнять производственные операции или операции по контролю качества, что является одним из условий создания и поддерживания на должном уровне системы обеспечения качества.
Весь персонал должен быть заинтересован в получении готового продукта высокого качества
4.2 В должностных инструкциях предприятия должны быть отражены производственные задачи (права и обязанности) всех сотрудников, в том числе руководящего персонала, и области их ответственности
4.3 Каждый сотрудник должен быть знаком с основными положениями “Правил...”, непосредственно относящимися к его производственной деятельности.
В начале и в течение дальнейшей работы каждый сотрудник должен пройти курс обучения основам “Правил...”, включающий в себя также необходимые знания по гигиене
Похожие работы
... и контролирует правильность оформления прописей для индивидуального производства лекарств. Ведет текущую и отчетную документацию. Проводит целевое фармацевтическое исследование аптек, других учреждений с целью оценки состояния контроля качества лекарственных средств при их изготовлении, транспортировке, хранении и отпуске. Экспресс-анализ лекарственных форм. Необходимость внутриаптечного ...
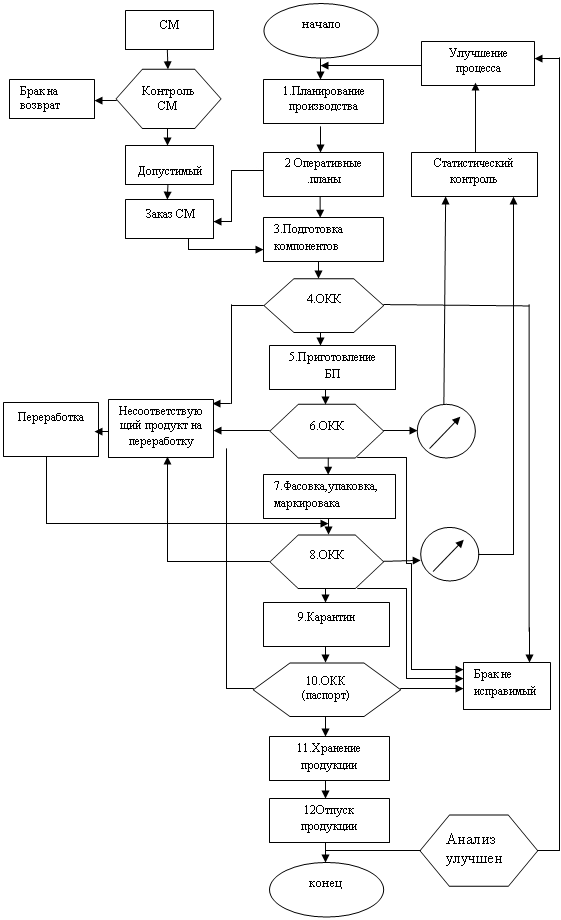
... настоящего стандарта обязательны для исполнения всеми участками процесса. Требования настоящего СТО распространяются на действия по производству лекарственного препарата Нитокс 200 и область возможного его улучшения. Сознательное нарушение требований настоящего стандарта организации является нарушением исполнительской дисциплины и может быть основанием для административного взыскания. 2. ...
... показателей и методов контроля качества Л С. Он должен обеспечивать разработку эффективного и безопасного Л С. Новый ОСТ предусматривает наличие двух категорий стандартов качества: I. Государственные стандарты качества лекарственных средств (ГСКЛС), к которым относятся: общая фармакопейная статья (ОФС) и фармакопейная статья (ФС); II. Стандарт качества (СКЛС); фармакопейная ...
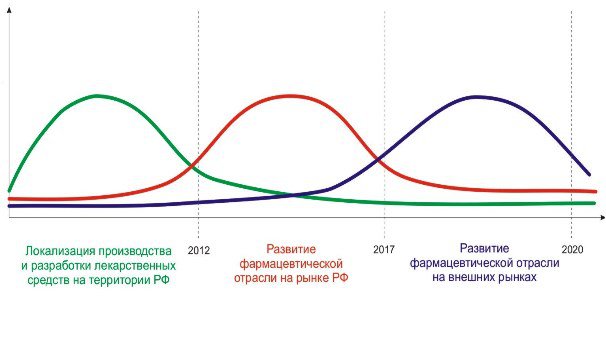
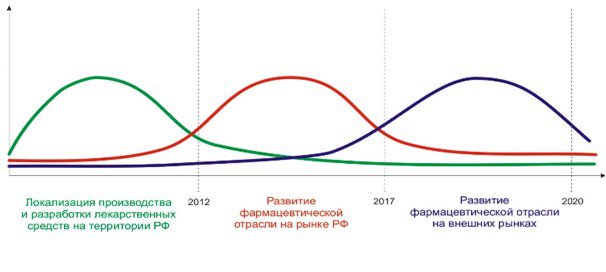
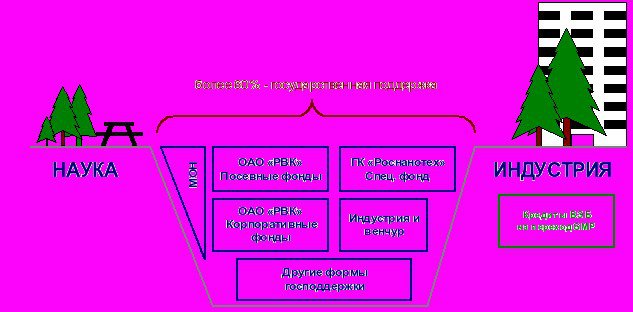
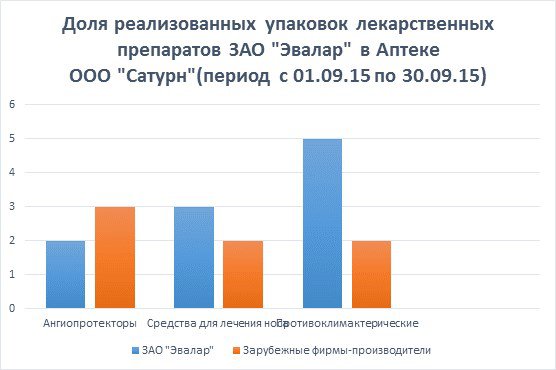
... стратегические цели, принципы и задачи развития фармацевтической промышленности, ситуацию в отрасли, проблемы отрасли, способы и пути решения указанных проблем.[12] 7.Исследование доли выпускаемой продукции отечественных производителей в ассортименте товаров аптек базы практики. 7.1.Анализ доли препаратов ЗАО «Эвалар» В Аптеке ООО «Сатурн», расположенной по адресу: Республика Марий Эл, пгт. ...

0 комментариев