Навигация
Термодинамические функции бинарных соединений (интерполяционная формула Лагранжа)
1.5 Термодинамические функции бинарных соединений (интерполяционная формула Лагранжа)
В литературе приводятся термодинамические данные далеко не для всех бинарных соединений, а некоторые из имеющихся констант нуждаются в уточнении и согласовании.
И. Г. Горичевым с помощью интерполяционной формулы Лагранжа, термодинамических соотношений эмпирической закономерности о постоянстве приведённого химического потенциала атомов кислорода в оксидах MeOx в некотором интервале х и уравнения Гиббса – Дюгема получена приближённая функциональная связь между стандартной энергией Гиббса образования оксидов металла из элементов и стехиометрическим составом оксидов:
![]() ().
().
Здесь i и j – степени окисленности оксидов металла, для которых существуют наиболее достоверные термодинамические данные, х – степень окисленности оксида, для которого производится прогнозирование энергии Гиббса образования. При расчётах по данной формуле следует иметь в виду, что величины ![]() должны быть выражены в Дж/г-атом О.
должны быть выражены в Дж/г-атом О.
Данная формула может быть применена для оценки термодинамических свойств не только оксидов, но и других бинарных соединений металла с электроотрицательными атомами [].
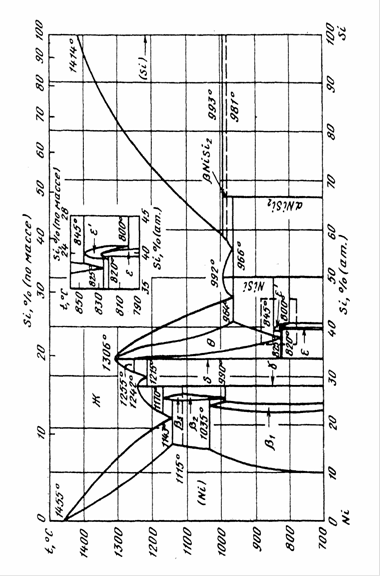
В данной работе интерполяционная формула Лагранжа использована для оценки термодинамических свойств силицидов марганца.
1.6 Общие принципы термодинамического описания химической устойчивости металлов
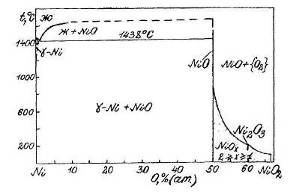
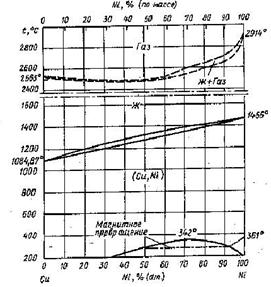
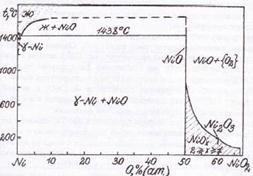
Химическая устойчивость металлов в окислительной газовой среде, например, на воздухе, определяется их стойкостью к окислению кислородом. Лучшим способом представления термодинамической информации об окислении металлических материалов являются фазовые диаграммы состояния систем металл-кислород.
На фазовых диаграммах Ме-О представлены различные химические равновесия, играющие роль в процессе окисления металла. Они характеризуют растворимость кислорода в данном металле, состав оксидных форм, образующихся в результате окислении металла кислородом, и устойчивость фаз в зависимости от различных параметров системы: температуры, давления, состава и др.
Состав системы выражается содержанием металла и кислорода в атомных процентах, либо в процентах по массе.
Для более сложных систем, содержащих третий компонент- другой металл, существуют аналогичные диаграммы состояния Ме1-Ме2-О. Они позволяют разобраться в вопросах состава и структуры окалины (слоев окислов) на поверхности бинарных сплавов. В литературе накоплен огромный справочный материал по термодинамическим свойствам неорганических веществ, сформулированы общие принципы фазовых равновесий в гетерогенных системах (правило фаз Гиббса), предложены различные модели, интерполирующие свойства компонентов и металлических, и оксидных растворов (теории совершенных и «регулярных» растворов) и т.п. Все это позволило расчетным путем выявить вид и характерные особенности интересующих нас диаграмм состояния [6].
Согласно закону равновесия фаз - правилу фаз Гиббса, в трехкомпонентной системе при постоянных внешних параметрах (P,T=const):
f=3-Ф ()
где f- число термодинамических степеней свободы, или вариантность системы, то есть количество параметров (температура, давление, концентрации компонентов в фазах), которые являются независимыми,
Ф – количество фаз в системе, находящихся в равновесии.
Из физических соображений следует, что f![]() 0. Таким образом, в указанной системе возможны равновесия с участием одной, двух или максимум трех фаз:
0. Таким образом, в указанной системе возможны равновесия с участием одной, двух или максимум трех фаз:
- однофазные равновесия (f=2); отдельные фазы (вещества) термодинамически устойчивы в определенном интервале составов и, соответственно, парциальных давлений кислорода;
- двухфазные (моновариантные) равновесия (f=1);
- трехфазные (инвариантные) равновесия (f=0).
В условиях трехфазного равновесия система не имеет степеней свободы, т.е. данное состояние системы полностью описывается законами действующих масс гетерогенных химических реакций и условиями нормировки составов фаз. Для однозначного расчета составов фаз в условиях двухфазового равновесия необходимо задаваться одним из параметров системы.
Для записи законов действующих масс (выражений для констант равновесий) химических реакций необходимо определить активности компонентов в фазах. Активность кислорода в газовой фазе при давлении 1 атм может быть принята его парциальному давлению. Для конденсированных фаз в рамках модели регулярных растворов справедливо выражение:
![]() ; ()
; ()
где ![]() - активность компонента в растворе;
- активность компонента в растворе;
![]() - мольная (атомная) доля компонента в растворе;
- мольная (атомная) доля компонента в растворе;
![]() - энергия смешения компонентов при образовании раствора.
- энергия смешения компонентов при образовании раствора.
Формула применима к двухкомпонентным растворам.
Для конденсированных фаз в рамках модели идеального (совершенного раствора) ![]() .
.
Валовый состав тройной системы Ме1-Ме2-О можно записать как
![]() ;
;
где ![]() – атомная доля металла
– атомная доля металла ![]() ;
;
![]() - степень окисленности системы (
- степень окисленности системы (![]() .)
.)
Тогда изотермические сечения диаграммы состояния этой системы удобно представить графически на плоскости в координатах ![]() .
.
В соответствии с теорией химического сродства Вант-Гоффа термодинамическим критерием возможности окисления элементов в сплаве служит стандартное изменение свободной энергии Гиббса ![]() для реакции:
для реакции:
![]() ; (1.24)
; (1.24)
или давление кислорода ![]() . Эти показатели взаимосвязаны уравнением:
. Эти показатели взаимосвязаны уравнением:
![]() ; (1.25)
; (1.25)
Чем отрицательнее величина изобарно-изотермического потенциала реакции (1.24), или ниже ![]() , тем выше избирательность окисления данного металла.
, тем выше избирательность окисления данного металла.
Итак, представление фазовых диаграмм вида Ме-О, Ме1-Ме2-О может быть различно и зависеть от выбора термодинамических параметров как координат (Р, Т составов и др.) Но в любом случае эти диаграммы могут служить термодинамической основой при изучении вопросов об устойчивости систем, в частности, при рассмотрении вопросов об окислении металлов [7].
Похожие работы
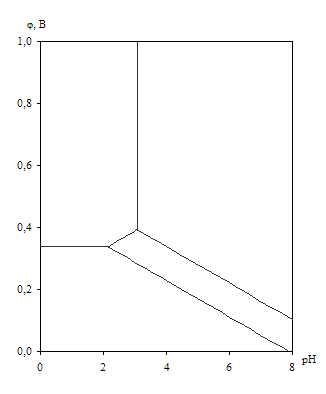
... устойчивость металлов и сплавов определяется их стойкостью к коррозии в водной среде. Лучшим способом представления термодинамической информации о химической и электрохимической устойчивости металлических систем в водных растворах являются диаграммы рН-потенциал. Впервые такие диаграммы в системе элемент-вода для чистых металлов при температуре 250С были построены Марселем Пурбе и использованы им ...
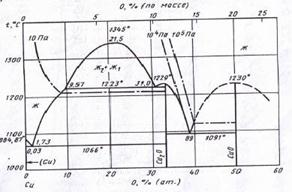
... VIII – CuO + NiO2 + {O2}. Области I и V очень малы и в масштабе диаграммы вырождаются в линии. Анализируя диаграмму Cu – Ni – O можно сделать следующие выводы о химической устойчивости медно-никелевых сплавов: 1) Окисление сплавов начинается уже при давлениях кислорода в газовой фазе над сплавами большем чем атм. Поэтому медно-никелевые сплавы будут окисляться кислородом воздуха при 25оС. 2) ...
... пособие по прикладной химии «Задачи по теоретическим основам химической технологии», составленное по материалам представленной работы. 3. Методика решения задач по теоретическим основам химической технологии Одна из главных задач химической науки и промышленности - получение необходимых человеку веществ (продуктов, материалов). Поэтому большинство учебных химических задач снизано с ...
абсолютно чистые минералы, расплавленные и сублимированные горные породы. Гетерогенной это такая термодинамическая система, которая состоит из двух и более гомогенных областей. Внутри такой системы имеются поверхности раздела фаз, при переходе через которые химический состав и физические свойства вещества изменяются скачкообразно. Фазой гетерогенной системы называется гомогенная область, которая ...


0 комментариев