Навигация
Ионное взаимодействие
1. Ионное взаимодействие.
взаимодействие между двумя ионами с зарядами l1 и l2 . Потенциальная энергия в данном случае находится по формуле:
Uион=(l1 + l2)/e*R,
R – расстояние между ионами,
e – диэлектрическая проницаемость среды,
l1 и l2 – заряды ионов.
Величина Uион зависит от зарядов ионов. Если заряды противоположны, то Uион<0 – притяжение, если заряды имеют одинаковый знак – силы отталкивания преобладают.
Ионные взаимодействия: между ионогенными группами белков, малыми противоионами, фосф группами нуклеиновых кислот и катионами.
2. Ион-дипольные взаимодействия.
взаимодействия между ионами и полярными группами молекул.
Энтропия этого взаимодействия определяется зарядом иона, дипольным моментом взаимодействующей с ним атомной группы, а так же расстоянием между ними.
P = e*l → U = e*P/ε*R
P – дипольный момент,
l – расстояние между центрами диполя.
3. Ориентационное взаимодействие
взаимодействие между двумя диполями или группой диполей, присутствующих в некоем участке пространства Рисунок
a) между двумя диполями:
P1 = e1*l1,
P2 = e2*l2,
e – заряд электрона, l – расстояние м/д центрами диполя.
Uориент= 2P1*P2/R3.
б) группа диполей не может выстроиться в антипараллельное положение, будет наблюдаться некоторое усреднение взаимодействия между ними.
Uсред=2P12P22/3kTR6,
k – постоянная Больцмана,
Т – абсолютная температура.
4. Индукционное взаимодействие
постоянные дипольные молекулы или атомные группы (Р1) индуцируют в другой молекуле или атоме дипольный момент (Р2), с которым он и взаимодейтвует.
Способность индуцировать диполи в других молекулах определяется напряденностью электромагритного поля первого диполя. Р2 дипольный момент будет зависеть от Е1 напряженности поля.
Р2 = а*Е1, а – поляризуемость.
Поляризуемость – это способность электронной оболочки смещаться под действием электронного поля. а = 10–24 см3 (размер самой электронной оболочки)
Uинд=2aP2/R6
индукционное взаимодействие не зависит от температуры.
Если в среде существует первый диполь, наводящие другие, то он вряд ли будет единственым, следовательно индукционные взаимодействия в значительной мере усредняются и компенсируются друг другом.
5. Дисперсионные взаимодействия
взаимодействия валентно насыщенных электронных оболочек атомов и молекул.Существует между молекулами газов (N2, CO2, O2). И именно дисперсионными взаимодействиями объясняется непредельность поведения этих газов. Дисперсионные взаимодействия лежат в основе структуры молекул кристаллов.
Любой электрон является своеобразным гармоническим осциллятором (когда электрон движется по своей орбите, он является источником волн). Если электрон не взаимодействует с другими электронами, то длину его волны можно рассчитать W0 – исходная частота осцилляции. Во время дисперсионных взаимодействий происходит взаимодействие между двумя такими осцилляторами, при этом длина волны первоначального колебания начинает изменяться, то есть возникает как бы два различных колебания с частотами, отличающимися от первоначальной тем, чем больше взаимодействие.
Uдис. = - ¾* ћ*W0*a2/R6
ћ – постоянная Планка,
R – расстояние между взаимодействующими частицами,
а – поляризуемость.
В основе дисперсионного взаимодействия лежат не электростатические, а квантовомеханические силы. Это доказал Лондон.
Ориентационное, индукционное и дисперсионное взаимодействие называется ВанДер-Ваальсовым взаимодействием. ВанДер-Ваальсовы силы ответственны за образование конденсированной жидкости, а так же они описывают взаимодействие на разделе фаз (твердый и жидкий).
6. Водородные связи –
специфическая связь, которая создается атомом Н, который находится в группах ОН, NH, FH, ClH и иногда SH, причем Н связывает эти группы с валентно насыщенными атомами N2, O2 и F.
Водородные связи определяют структуру и свойства воды, как самого главного и основного расворителя в биосистемах. Водородные связи участвуют в формировании макромолекул, биополимеров, а так же связях с малыми молекулами.
Uвод = 4-29 кДж/моль
Основной вклад в водородные связи вносят электростатические взаимодействия, но они не сводятся к ним. Протон движется вдоль прямой, соединяющей экектоотрицательные атомы и испытывает различное влияние со стороны этих атомов.
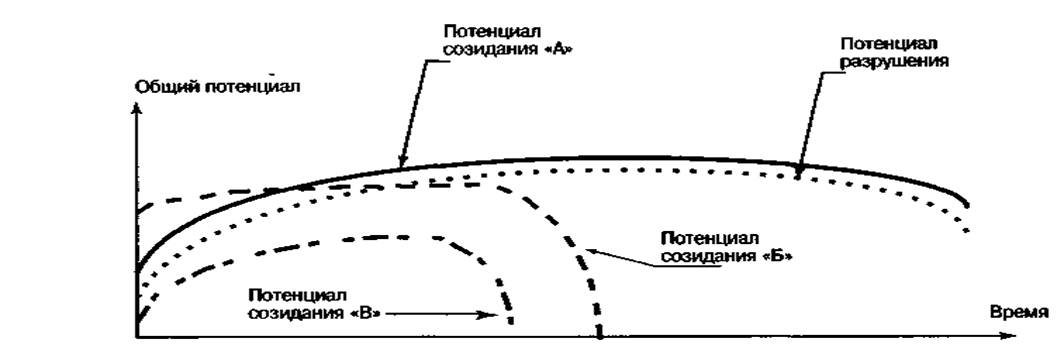
Рисунок
Этот график – частный случай, связь между N-H...N и N...H-N. R – расстояние между взаимодействующими частицами. 2 минимума свободной энергии располагаются возле первого или второго взаимодействующего атома N.
Похожие работы
... Во времена, например, Платона. Они были одни, а на современном этапе они другие. По мнению Карпекова К.С.(2).(который по моему мнению наиболее полно обозначил современную концепцию происхождения объектов Вселенной.). В.И. Вернадский впервые поставил вопрос о рациональном контроле над окружающей средой. Ноосфера Вернадского – это сфера материального, в котором в качестве управляющего, регулирующего ...
... или технологических процессов; – при выборе технического решения обеспечить малоотходность производства и максимальную эффективность использования энергоресурсов. Задачи специалиста в области безопасности жизнедеятельности сводятся к следующему; – контроль и поддержание допустимых условий (параметры микроклимата, освещение и др.) жизнедеятельности человека в техносфере; – идентификация ...
... не знают о законе. Второй вариант. Руководитель знает о законе, а его подчиненные нет. Третий вариант. Руководитель и подчиненные знают о законе», единства анализа и синтеза Список использованной литературы 1. Алиев В.Г., Варфоломеев В.П. Теория организации, курс лекций. «Самоорганизация в природе и обществе», Махачкала ИПЦ ДГУ, 1998. 2. Доблаев В.Л. Теория организаций. — М.: Институт ...
... не тепловая энергия. Вероятно, для выяснения истины необходимо более широкое, чем термодинамическое или статистическое, определение энтропии. Поэтому-то мы рассматриваем этот вопрос здесь, в разделе биологических концепций. Энтропия и эволюция. Вероятно, зарождение проблемы взаимосвязи между энтропией и эволюцией произошло в 1854 г., когда Гельмгольц и Больцман первыми обратили внимание на ...

0 комментариев