Навигация
Исследование совместного электровосстановления фторалюминат-иона и галогенидных комплексов гадолиния на фоне хлоридных и хлоридно-фторидных расплавов
3.2. Исследование совместного электровосстановления фторалюминат-иона и галогенидных комплексов гадолиния на фоне хлоридных и хлоридно-фторидных расплавов.
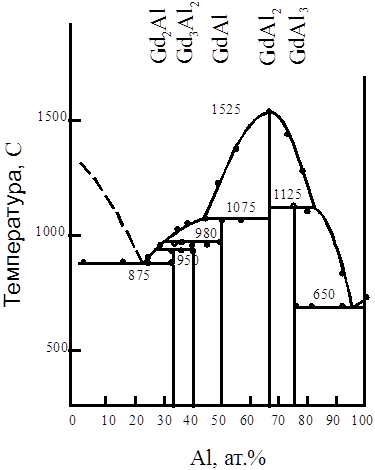 |
|
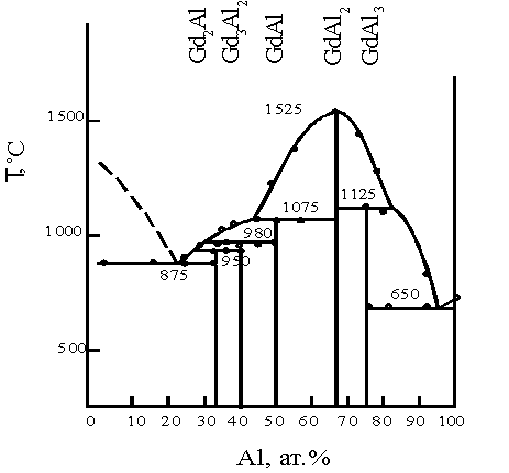
В работе [64] исследована система алюминий – гадолиний методами микроскопического, термического и рентгеновского анализов (рис3.2.). В сплавах системы образуются 5 интерметаллических соединений, из них только одно – GdAl2 плавится с открытым максимумом при 1525˚С. Остальные 4 – Gd2Al, Gd3Al2, GdAl и GdAl3 – образуются по перитектическим реакциям при температурах 950, 980, 1075 и 1125˚С соответственно. Кроме того, в сплавах системы кристаллизуются две эвтектики: одна со стороны гадолиния при 875˚С, вторая со стороны алюминия при 650˚С. Сплавы изготовляли методом дуговой плавки в атмосфере очищенного аргона.
Что касается совместного электровыделения и механизма этого процесса, то в литературе практически нет этой информации.
В нашей работе исследование совместного электровосстановления гадолиния и алюминия проводили вольтамперометрическим методом на фоне хлоридных и хлоридно-фторидных расплавов с использованием серебряного электрода. Как показано выше, при электровосстановлении фторалюминат-иона, а также проведенных ранее на кафедре неорганической и физической химии работ по электровосстановлению различных комплексов гадолиния на фоне хлоридных и хлоридно-фторидных расплавов серебряный электрод наиболее индифферентен к этим двум металлам.
На рис. 3.3. приведены результаты вольтамперометрических измерений совместного электровосстановления комплексов алюминия и гадолиния. Кривые (2) и (3) соответствуют электровосстановлению фторалюминат-иона при потенциалах 1,5 – 1,55 В относительно платинового квазиобратимого электрода сравнения.
Введение трихлорида гадолиния в хлоридный расплав NaCl – KCl, содержащий фторалюминат-ионы, приводит к изменению формы вольтамперных кривых,- на катодной части вольтамперограмм при потенциалах, отрицательнее электровосстановления фторалюминат-ионов появляются волны восстановления хлоридных комплексов гадолиния. Первые, в этом случае, ока
Рис. 3.3. Циклические хроновольтамперограммы процесса совместного электровосстановления Na3AlF6 и GdCl3 на фоне NaCl – KCl. С(GdCl3)=1,89.10-4моль/см3(3). С(Na3AlF6), моль/см3.104: 1, 2 – 0,945; 4 – 1,89. Т = 973К; V = 0,1В/с.
Рис. 3.4. Циклические хроновольтамперограммы процесса совместного электровосстановления Na3AlF6 и GdCl3 на фоне NaCl – KCl - NaF. С(GdCl3)=1,855.10-4моль/см3(3). С(Na3AlF6), моль/см3.104: 1 – 0; 2 – 0,928; 3 – 1,855; 4 – 3,71; 5 – 9,28. Т = 973К; V = 0,1В/с.
зываются более растянутыми по оси потенциалов, чем в системах в отсутствии хлоридных комплексов гадолиния (гадолиний и алюминий дают сплав).
На анодных участках циклической вольтамперограммы наблюдаются две волны окисления катодных продуктов (волны С и D).
Отличительной особенностью анодной волны окисления при совместном присутствии комплексов гадолиния и алюминия является то, что волны анодного растворения смещаются в более отрицательную область потенциалов и значительно растягиваются по оси потенциалов.
Появление двух волн (С и Д) на анодной части мы связываем с растворением гадолиния и сплавов гадолиний - алюминий разных соотношений.
На рис. 3.4. представлены циклические хроновольтамперограммы расплава NaCl-KCl-NaF(10 вес.%) - GdCl3при последовательном добавлении Na3AlF6. Сравнивая данные зависимости с аналогичными в хлоридном расплаве можно заметить, что волны совместного электровосстановления GdCl63- и AlF63- во фторидном расплаве имеют более четко выраженный пик и менее растянуты по оси потенциалов. К тому же, анодная часть вольтамперограмм в этих условиях сливается в одну волну и становится более воспроизводимой. Эти процессы обусловлены избытком фторид–иона, уменьшающего число частиц, участвующих в электродном процессе. Как видно из рис. 3.4 (кривые 4 и 5), при большом избытке криолита волны восстановления гадолиния и алюминия сливаются в одну растянутую по оси потенциалов волну,- происходит электровосстановление частиц различного состава (AlXGdY).
Таким образом, результаты вольтамперных измерений в расплаве NaCl-KCl-GdCl3-Na3AlF6говорят о возможности электрохимического получения сплавов Gd-Al в различных соотношениях. С нашей точки зрения, механизм электрохимического получения сплавов можно представить следующим образом: электровыделение алюминия из фторалюминат-иона происходит при более положительном потенциале, чем выделение гадолиния из хлоридных комплексов. Разность потенциалов выделения составляет 350 – 400 мВ. Уменьшение разности потенциалов возможно за счет энергии сплавообразования гадолиния и алюминия, а также при увеличении концентрации фторалюминат-иона в расплаве и при определенных соотношениях удается совмещение волн выделения гадолиния и алюминия в одну растянутую волну. Однако электрохимическое получение сплава необходимо проводить при плотностях тока выше предельного тока электровосстановления фторалюминат-иона.
Электрохимические процессы, происходящие при образовании сплава можно представить следующим уравнением:
GdCl63- + AlF6-xClx3- + 6e → GdAl(спл) + (6-x)F- + xCl-
Выводы
Методом линейной циклической вольтамперометрии исследовано совместное восстановление ионов гадолиния и алюминия в хлоридных и хлоридно-фторидных расплавах на серебряном и платиновом электродах.
1. Изучен процесс электровосстановления фторалюминат-иона на фоне хлоридных и хлоридно-фторидных расплавов. Показано, что серебряный электрод является индифферентным по отношению к алюминию и может быть использован для получения более надежных данных.
2. Установлен необратимый характер электровосстановления фторалюминат-иона на фоне эквимолярного расплава NaCl-KCl.
3. Показано влияние анионного состава (фторид-иона) на процесс электровосстановления фторалюминат-иона на фоне хлоридно-фторидных расплавов.
4. Изучено совместное электровосстановление фторалюминат-иона и хлоридных комплексов гадолиния на фоне хлоридных и хлоридно-фторидных расплавов.
Показано, что при определенных соотношениях концентраций ионов алюминия и гадолиния и анионного состава расплава можно осуществить процесс совместного электровосстановления и получения гадолиний-алюминий сплавов.
Литература.
1. AN INVESTIGATION on MELTING POINT and ELECTRICAL CONDUCTIVITY OF FLUORIDE – LANTANA MELT. Wei Xujun, Mu Xiuzhi, Liu Xuliang, Zhao Yifa. “New Front. Rare Earth Sci. And Appl. Proc. Jnt. Conf., Beijing, Sept. 10-14, 1985. Vol. 2”. Beijing, 1985, 1176-1179.
2. Д.Браун. Галогениды лантаноидов и актиноидов. Под ред. академика И.В.Тананаева, перевод с англ. к.х.н. С.С.Родина. Москва, Атомиздат, 1972
3. Поляченок О.Г., Новиков Г.И. «ЖНХ», 8, 2818-2819. (1963)
4. Прикладная химия ионных расплавов / Делимарский Ю.К., Барчук Л.П.- Киев: Наук. думка, 1988. с. 8-10
5. J.MOCHINAGA. EDITORIAL. Structure of molten salts. Molten Salts Bulletin Sels Fondus./ France, 1997
6. Строение расплавленных солей /Под ред. Е.А.Укше.- М.: Мир, 1966.- 432 с.
7. Крюкова А.И., Коршунов И.А. Исследование комплексообразования празеодима, неодима и прометия в растворах хлоридах и нитратов щелочных металлов. Тезисы докладов V Всесоюзной конференции по физической химии и электрохимии ионных расплавов и твердых электролитов, 1974
8. A.Matsuoka, K.Fukushima, J.Mochinaga, Y.Iwadate, M.Tomita and R.Takagi. Proceedings of the 25th Symposium on Molten Salt Chemistry, p.19, (1993)
9. Д.В.Дробот, Б.Г.Коршунов, З.М.Шевцова. Некоторые закономерности комплексообразования в расплавах, содержащих хлориды редкоземельных и щелочных металлов./ В кн.: Физическая химия расплавленных солей. Труды 2-го Всесоюзного Совещания по физической химии расплавленных солей. 15 – 20 октября 1963 г. Изд-во «Металлургия», М.,1965, с. 48-54
10. H.B.Kushchov, A.S.Usdenova. The Investigation of the Electrochemical Behaviour of the Ions of gadolinium and Samarium in Chloride and Chloride-Fluoride Melts /EUCHEM CONFERENCE of MOLTEN SALTS,France, 1998
11. В. М.Смирнов. Электродные потенциалы в расплавленных хлоридах./ Из-во «Наука», М., 1973г
12. Координационная химия РЗЭ. Под ред. В.И.Спицына и Л.И.Мартыненко; М., Из-во МГУ, 1979г
13. Thoma R.E.et.al. Inorg. Chem., 1963
14. Thoma R.E., Insley H., Herbert G.M. Ibid, 1966
15. Thoma R.E., Karraker R.H. Ibid, 1966
16. Дергунов Е.П. Доклад АН СССР, 1952
17. Букалов Г.А., Бабаева Е.П. ЖНХ, 1954
18. Дергунов Е.П. Доклад АН СССР, 1958
19. Thoma R.E.et.al.J. Phis. Chem., 1961
20. Barton C.J., Redman J.P., Stehlow R.A./ J.Inorg. Nucl. Chem., 1961
21. Thoma R.E. US Report ORNL, 1959
22. Zachariasen W.H. Amer. Chem. Soc., 1958
23. Roy P.M., Roy R.G. Electrochem. Soc., 1964
24. Keller C.Z. Naturforsch, 1964
25. Zachariasen W.H. Acta. Cryst., 1958
26. Thoma R.E. In: Progress in the Science and Technology of the Rare Earths (L. Eyring, Ed.), Vol. 2. Pergamon Press, London, 1966
27. Bode H., Voss E.Z. Anorg. Chem., 1957
28. Zachariasen W.H. Ibid., 1959
29. Sears D.R. US Report ORNL, 1966
30. Е.М.Простаков и др. Комплексообразование в расплавленных смесях фторидов калия, иттрия, лантана, неодима и гадолиния. Тезисы докладов VI Всесоюзной конференции по физической химии ионных расплавов и твердых электролитов, 1976
31. J.Electrochem. Soc., Vol.142, № 7. July 1995
32. В.В. Серебренников. Химия РЗЭ. Т.1, Изд. Томского университета, 1959г
33. Du Senlin, Tang Dingxiang. New Front Rare Earth Sci. and Appl. Pros. Int. Conf. Biejng, Sept 10-14, 1985. Vol.2, Biejng, 1985, 1117-1126
34. Morzice Edwar New Front Rare Earth Sci. and Appl. Pros. Int. Conf. Biejng, Sept 10-14, 1985. Vol.2, Biejng, 1985, 1099-1106
35. Хасэгава Иосисукэ. Кондзуку, Metals and Technal, 1988, 58, №1, 52-57
36. В.С.Купцев, В.Х.Новичков, Н.Л.Ополченова, Р.Д.Рыбкина, Н.Н.Степарева, Е.Р.Томашленская. Физико-химические исследования фазовых превращений в электролите для электрохимического получения РЗМ./ Кольский семинар по электрохимии редких и цветных металлов. Тез.докл. Аппатиты, 1989, с 30-31.
37. Ф.Спеддинг, А.Даан. Редкоземельные металлы. М., Металлургия, 1965
38. Powder diffraction fine search manual alhabetical listing inorganic. 1978 (ASTM) USA.
39. Y.Katayama, R.Hagiwara and Y.Ito. Precipitationof rare earth comounds in LiCl-KCl eutectic./ J. Electrochem. Soc., 142, 7, 2174-2178, 1995
40. Masatoshi Iizuka. Diffusion Coefficient of Cerium and Gadolinium in Molten LiCL-KCl./ J.Electrochem. Soc., Vol. 145, No. 1, January 1998
41. В.П.Колесников, Г.Н.Казанцев, Е.В.Устюгов, А.А.Хаматшин. Катодные процессы при осаждении гадолиния на твердых и жидких электродах из хлоридных расплавов. VI Всесоюзная конференция по физической химии ионных расплавов и твердых электролитов. Ч. 2
42. Balasubrahmanim K., Nahis L. Raman Spectra of Liquid AlCl3-KCl and AlCl3-NaCl // J.Chem. Phys.- 1965.- V. 42.- P. 676-680.
43. Begun G.Ms., Bosion G.R., Toris G., Mamontov G.A. The Raman Spectra of molten Aluminium & halide-alkali.
44. Torsi G., Mamontov G.A., Begun G.Ms. Raman Spectra of the AlCl3-NaCl Sustem // Inorg. Nucl. Chem. Lett.- 1970. V. 6.- P. 553-560.
45. Cyrin S.J., Klaboe P., Rutter E., Oye H.A. Spectral Eviadensi for Al2Cl7 in chloride melts // J.Chem. Phys.- 1970.- N 52 - P. 2776-2779.
46. Rutter E., Oye H.A. Raman Spectra of the AlCl3-KCl and trends in species Formation. // Inorg. Nucl. Chem.- 1973. V. 35.- P. 1185-1198.
47. Solomons G., Clarce J.H.P., Bokris J.O.M. Intensification of the complections in liquidicryolite // J.Chem. Phys.- 1968.- V.49.- P. 445-450.
48. Funcy K-W., Begun G. Ms. Mamontov G.A. Raman Spectra of molten Bismute threchloride and antimony threchloride and of their Mixtures with Potassium Chloride on Aluminium chloride. // J. Inorg. Chem.- 1973. V. 12.- P. 53-57.
49. Кудяков В.Я., Смирнов М.В. Термодинамика фторидных комплексов алюминия в расплаве KCl – NaCl. V Всесоюзный симпозиум по химии неорганических фторидов. Днепропетровск. 1978.- М.1978. с.153.
50. Кудяков В.Я., Смирнов М.В., Росохин Ю.В. Фторидные комплексы алюминия в расплаве KCl – NaCl. // Координационная химия.- 1975.- 5.- с.821-823.
51. Мельников Б.В., Сальников В.И., ЛебедевВ.А., Ничков И.Ф., Роспопин С.П. Равновесные потенциалы алюминия и термодинамика образования его фторидных комплексов в расплавленной эквимольной смеси хлоридов натрия и калия. Деп. в ВИНИТИ 20.07.76г. № 2807-76.
52. Багрий В.А., Городыский А.В. Делимарский Ю.К. Потенциометрическое изучение комплексообразования в расплавленных хлоралюминатах. // Укр.хим.ж.- 1978.- т.44.- с. 563-570.
53. Rutter E., Ratkje S.K. Raman Spectra of molten mixtures containing Aluminium fluoride. Dissolving of AlF63- // Acta Chem. Scand.- 1975. V. 29.- P. 565-560.
54. Rollein M. Connaissence aotnelle de la Structure des millenx fondus a bass de cryolite // Rev. Sht. Tempset nefract.- 1976.- V.13.- P. 83-88.
55. Нарышкин И.И., Могилев В.М. Полярография расплавов на фоне хлоридов калия и натрия с применением свинцового капельного электрода. // Журн. Прикл.химия. – 1961. Т.34.- с.2353-2356.
56. Делимарский Ю.К., Макагон В.Ф., Грищенко О.П. Исследование разряда ионов алюминия из высокотемпературного хлоралюминатного расплава. // Укр.хим.ж.- 1980.- т.46.- с.115-118.
57. Saito M., Suzuki S, Coto H. Polarography of some metals ions in molten evtectic using dipping molibdenum electrode.// J. Electroanalytical Chem.- 1963.- V.84.- P. 332-334.
58. Tremillon B., Letisse G. Proprietes en Solution dans le tetrachloalyminate Sodium fondu. Systems “acidе-bese” // J. Electroanalytical Chem.- 1968.- V.17.- P. 371-386.
59. Городыский А.В., Багрий В.А., Делимарский Ю.К. Хронопотенциометрическое исследование восстановления алюминия из хлоралюминатных расплавов. // Укр.хим.ж.- 1979.- т.45.- с.579-582.
60. Демидов А.И., Симонов И.А., Морачевский А.Г. Катодные поляризации алюминия в расплавах MeCl – AlCl3 (Me – K, Na). Изв. вуз. цвет. металлургии.- 1985. № 2.- с.72-76.
61. Polland P., Mamontov G.A. Electrochemical reduction of Al2Cl7- ions in Chloraluminate melts // J. Electrjchemical Soc.- 1976.- V.123.- P. 1299-1303.
62. Делимарский Ю.К. Макагон В.Ф. Особенности электровосстановления алюминия из высокотемпературных хлоралюминатных расплавов.// Электрохимия.- 1982.- т.28.- с.1386-1390.
63. Делимарский Ю.К., Макагон В.Ф., Грищенко О.П. Природа остаточных токов при электровосстановлении хлорида алюминия из хлоридных расплавов. // Электрохимия.- 1985.- т.21.- с.1225-1227.
64. Диаграммы состояния металлических систем, опубликованные в 1965 году. Выпуск 11 под редакцией Н.В.Агеева, М., 1968г.
Похожие работы
... H2O + Cl2 NaOH + CeO2 = Na2CeO3 + H2O а соединения со степенью окисления II (Eu, Sm, Yb) – восстановительные, причем окисляются даже водой: 2SmCl2 + 2H2O = 2SmOHCl2 + H2 Лантаноиды очень реакционноспособны и легко взаимодействуют со многими элементами периодической системы: в кислороде сгорают при 200–400 °С с образованием Э2O3, а в атмосфере азота при 750–1000 °С образуют ...
0 комментариев