Навигация
Сухомлинский В.А. О воспитании. М., 1973
1 Сухомлинский В.А. О воспитании. М., 1973.
Приложение № …
Описание некоторых лабораторно-практических работ, используемых при апробации спецкурса „Белок – основа жизни“.
Выделение белков из тканей и биологических жидкостей.
Цель: выявить содержание белков в тканях и биологических жидкостях.
Выделение казеина из молока.
Вариант I.
В химический стакан вместимостью 50 мл отмеривают цилиндром 3 мл молока и добавляют 7 мл дистиллированной воды. Смесь перемешивают и добавляют 10-15 капель 1%-ного раствора соляной кислоты. Кислоту приливают аккуратно, по каплям, так как в избытке кислоты осадок растворяется. Суспензию перемешивают, через 3-5 минут образуется рыхлый осадок.
Для удаления соляной кислоты в стакан добавляют 10 мл дистиллированной воды, перемешивают и оставляют ещё на 5 минут. Жидкость осторожно сливают с осадка. К осадку ещё раз добавляют 10 мл дистиллированной воды, осторожно перемешивают содержимое стакана и через 5 минут фильтруют смесь через бумажный фильтр.
Доказательством того, что в состав казеина входит фосфор: осадок с фильтром переносят в широкую пробирку с обратным холодильником и добавляют 6 мл 10%-ного раствора гидроксида натрия. Пробирку нагревают на песчаной бане в течение 1 часа. Жидкости дают остыть и нейтрализуют её концентрированной азотной кислотой до слабокислой реакции на лакмус. При нейтрализации выпадает осадок высокомолекулярных продуктов неполного гидролиза белка.
После отстаивания жидкость фильтруют и с фильтратом проделывают биуретовую реакцию и молибденовую пробу на фосфорную кислоту. К 5 каплям гидролизата добавляют 10%-ый раствор NaOH и 2 капли 1%-ого раствора CuSO4. Наблюдается фиолетовое окрашивание. К 10 каплям молибденового реактива добавляют 5 капель гидролизата и кипятят несколько минут. В присутствии H3PO4 жидкость окрашивается в лимонно-жёлтый цвет. При охлаждении выпадает жёлтый кристаллический осадок комплексного соединения (NH4)3PO412MoO3.
Вариант II.
К 50-ти мл свежего молока добавляют равный объём насыщенного раствора сульфата аммония. При этом выпадают в осадок альбумины и казеин. Отфильтровывают через складчатый бумажный фильтр раствор альбуминов.
Получение раствора яичного альбумина.
Осторожно проделывают отверстие в скорлупе яйца с двух концов и выливают белок в стакан вместимостью 500 мл. В тот же стакан добавляют 250 мл дистиллированной воды и содержимое стакана тщательно перемешивают стеклянной палочкой с резиновым наконечником.
Затем раствор переносят в мерный цилиндр, и объём раствора доводят до 300 мл добавлением дистиллированной воды. Раствор оставляют на 30 минут при комнатной температуре для образования хлопьевидного осадка глобулинов, затем разливают в пробирки по 20 мл.
20 мл полученной суспензии дважды фильтруют через складчатый фильтр. Фильтрат, содержащий яичный альбумин, используют для дальнейшей работы.
Выделение белков мяса.
Помещают в стакан 40-50 г пропущенного через мясорубку обезжиренного мяса, добавляют 80-100 мл 10%-го раствора NaCl и оставляют смесь стоять 15-20 минут при частом помешивании. Отфильтровывают через бумажный складчатый фильтр или через двойной слой марли окрашенную в красный цвет жидкость. В растворе содержатся главным образом, мышечный альбумин и глобулин.
Выделение растительных альбуминов.
25 грамм пшеничной муки смешивают со 100 мл дистиллированной воды, и смесь стряхивают в течение одного часа с помощью встряхивателя. Взвесь муки центрифугируют и надосадочную жидкость фильтруют через складчатый фильтр. Отфильтрованный прозрачный раствор содержит преимущественно альбумин пшеничных зёрен.
Реакции осаждения белков.
Цель: выявить влияние различных органических и неорганических веществ на осаждение белков. Изучить физические свойства белков.
Осаждение белков концентрированными минеральными кислотами.
В три сухие пробирки наливают по 1-2 мл концентрированной HNO3, H2SO4, HCl. Затем, наклонив каждую пробирку, осторожно по стенке добавляют из пипетки по 0,5 мл исследуемого раствора белка, так чтобы он не смешивался с кислотой. Вместе соприкосновения двух жидкостей появляется белый аморфный осадок белка. При встряхивании осадок, выпавший при действии HNO3, увеличивается, а осадки выпавшие при действии HCl и H2SO4, растворяются в их избытке.
Концентрированные минеральные кислоты вызывают необратимые осаждения белков. Это связано как с дегидратацией белковых молекул, так и с денатурацией белка.
Осаждение белков органическими кислотами.
В две пробирки добавляют по 2-3 мл раствора белка и добавляют в одну из них несколько капель 5%-го раствора трихлоруксусной кислоты (ТХУ), а в другую – несколько капель 20%-го раствора сульфосалициловой кислоты. В обоих случаях наблюдается выпадение осадка белка. Сульфосалициловая и ТХУ кислоты являются чувствительными и специфическими реактивами на белок.
ТХУ кислота осаждает только белки и не осаждает продукты распада белка и аминокислоты, поэтому ею пользуются часто для полного удаления белков из биологических жидкостей (например, сыворотки крови).
Осаждение белков солями тяжелых металлов.
В две пробирки добавляют по 1-1,5 мл исследуемого пастора белка, по каплям при встряхивании, добавляют в одну из них раствор CuSO4, а другую –
Pb(CH3COO)2.Выпадает хлопьевидный осадок вследствие образования малорастворимого солеобразного соединения (с солью меди – голубого цвета). При избытке реактива осадок снова растворяется.
Соли тяжелых металлов (Hg, Ag, Cu, Pb и др.) вызывают необратимое осаждение белков, образуя с ними нерастворимые в воде соединения. Потому что белки применяют в качестве противоядия при отравлении, например, ртутными солями (сулема).
Гидролиз белка.
Цель: дать учащимся представление о кислотном, щелочном и ферментативном гидролизе белка. Опытным путём установить продукты распада белковой молекулы.
Кислотный гидролиз простого белка.
При гидролизе белки распадаются сначала на высокомолекулярные продукты – пептоны, затем на полипептиды и, наконец, на аминокислоты.
Для гидролиза отмеривают в круглодонную колбу 20 мл раствора яичного белка и 5 мл концентрированной HCl. Колбу закрывают пробкой с длинной стеклянной трубкой. Кипятят содержимое колбы под тягой в течение 45 или 90 минут.
Открытие промежуточных продуктов распада белка в гидролизате при помощи биуретовой реакции. Промежуточные продукты распада белка – пептоны – при проведении биуретовой реакции дают розовое или красное окрашивание, а белки – сине-фиолетовое.
Ферментативный гидролиз белка.
Подготовительный этап: белок куринового яйца развести 1:1 водой и раствор белка влить в кипящую воду (V=100 мл) при помешивании.
В две пробирки налить по 2 мл приготовленного раствора белка. В первую добавить 1 мл дистиллированной воды, во вторую – 1 мл 1%-го раствора пепсина. Обе пробирки поставить в водяную баню при t=37-40 0C на 15 минут. Проделать биуретовую реакцию с содержимым обеих пробирок.
В воде окраска более интенсивная (фиолетовая с синим оттенком), так как при гидролизе осталось больше пептидных связей, чем в случае с пепсином (окраска менее интенсивная – фиолетовая с розовым оттенком) – меньше пептидных связей.
В присутствии пепсина гидролиз идёт интенсивнее, чем в присутствии воды.
Денатурация белков.
Цель: определить факторы, вызывающие денатурацию белка.
Похожие работы
... космического пространства с уверенностью, что не существует угрозы необратимого загрязнения планет, то есть до времени, пока результаты исследований космического пространства не подтвердят возможности снятия карантина. Практический обзор поиска и исследований внеземных форм жизни. В предыдущих главах рассмотрены теоретические аспекты проблемы поиска и исследований внеземных форм жизни, теперь ...
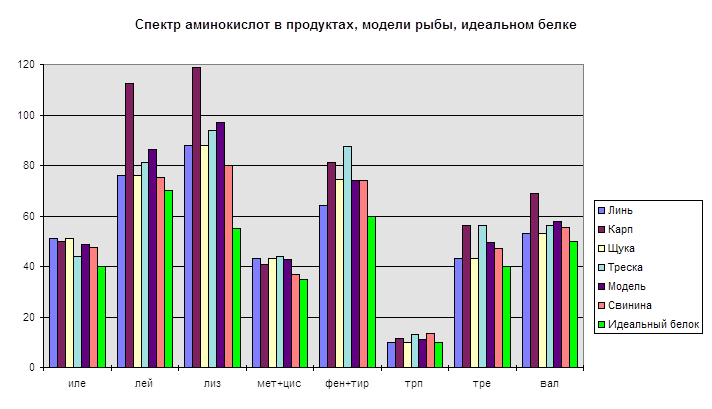
... [5; 7]. Таким образом, получается эффект истинного обогащения двух продуктов, что может быть полезным, а значит положительным аргументом оценивания мяса рыбы [7]. 3.3. Степень усвоения и термическая обработка белков пищи. Поступивший с пищей белок должен в начале усвоиться, и степень эффективности этого процесса зависит от ферментной атакуемости пептидных связей протеина. Ряд белковых веществ ( ...
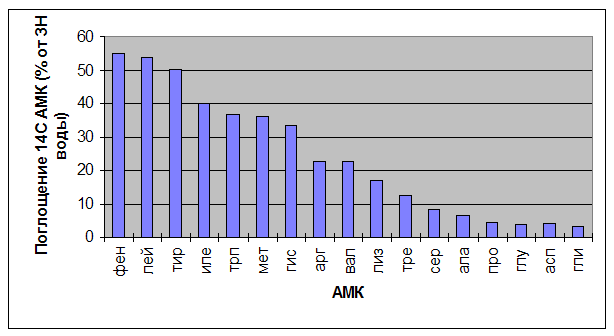
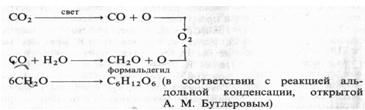
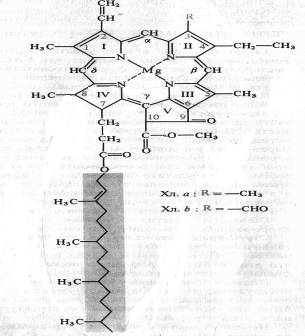
чительно большем количестве, если метка была у кислорода воды. 2 Фотосинтез как основа энергетики биосферы. Космическая роль фотосинтеза. Роль фотосинтеза в процессах энергетического и пластического обмена растительного организма К.А.Тимирязев, который первым начал изучать космическую роль зеленых растений, в публичной лекции, прочитанной в 1875 г., следующим образом представил эту проблему ...
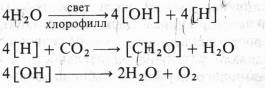
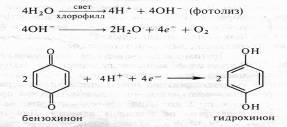
0 комментариев