Навигация
2.3 Задачи
2-1. Определите тепловой эффект реакции:
Al2Oкорунд + 3SO3 = Al2(SO4)3 кр +DUC, если реакция протекает при 298 К в автоклаве при постоянном объеме, а тепловой эффект реакции при р = const равен –573,4 кДж. (-566,0*103кДж)
2-2. Стандартная энтальпия реакции:
СаСО3(тв) = СаО(тв) + СО2(г),
протекающей в открытом сосуде при температуре 1000 К, равна 169 кДж моль-1. Чему равна теплота этой реакции, протекающей при той же температуре, но в закрытом сосуде? (160,7 кДж*моль-1)
2-3. Рассчитайте энтальпию образования N2О5(г) при Т = 298 К на основании следующих данных: 2 NО(г) + О2(г) = 2NО2(г), DН10 = -114,2 кДж моль-1, 4NО2(г) + О2(г) = 2N2О5(г), DН20 = -110,2 кДж моль-1, N2(г)+ О2(г) = 2NО(г), DН30 = 182,6 кДж моль-1.(13,3 кДж*моль-1)
2-4. Реакция горения ацетилена при стандартных условиях выражается уравнением: С2Н2+2,5О2=2СО2+Н2Ож –1300кДж. Определите теплоту образования ацетилена при постоянном давлении (226,5 кДж).2-5. Стандартные энтальпии образования жидкой и газообразной воды при 298 К равны -285,8 и -241,8 кДж моль-1 соответственно. Рассчитайте энтальпию испарения воды при этой температуре. (44,0 кДж моль-1)
2-6. Рассчитайте стандартный тепловой эффект реакции:
CаSO4(ТВ) + Na2CO3(aq) = CaCO3(ТВ) + Na2CO3(aq) при 298 К, если DfН0298 (CаSO4(ТВ)) = -1434 кДж моль-1(-5,0 кДж моль-1)
2-7. Известны тепловые эффекты следующих реакций:
СН3СООC2Н5(ж)+ОН¯(aq)=СН3СОО¯(aq)+C2Н5ОН(ж),DrН0298=-54,7кДжмоль-1;
Н3СООН(ж)+ОН¯(aq)=СН3СОО¯(aq)+Н2О(ж);DrН0298=-57,3кДжмоль-1;
СН3СООC2Н5(ж)+2Н2(г)=2C2Н5ОН(ж),
DrН0298=-76,4кДжмоль-1.
Рассчитайте тепловой эффект реакции:
C2Н5ОН(ж) + О2(г) = СН3СООН(ж) + Н2О(ж), если энтальпия образования жидкой воды равна -285,8 кДж моль-1.(-492,6 кДж моль-1)
2-8. На сколько градусов повысится температура при растворении 0,5 моль серной кислоты в 400 г воды, если теплота растворения серной кислоты равна -74,94 кДж, а удельная теплоемкость раствора равна 3,77 Дж/г·град? (22,14°С)
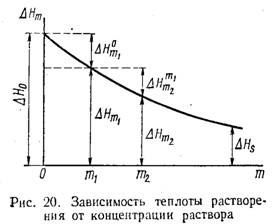
Тепловой эффект растворения безводного сульфата лития равен –26,71 кДж моль-1. Тепловой эффект растворения кристаллогидрата Li2SO4*H2O равен –14,31 кДж моль-1 при
298 К. Вычислите тепловой эффект образования Li2SO4*H2O из безводной соли и воды. Определите процентное содержание воды в частично выветренном кристаллогидрате сульфата лития, если тепловой эффект растворения 1 кг этой соли равен –0,146*103 кДж. (-12,40 кДж·моль-1)
Рассчитайте изменение энтальпии при нагревании 2 кг
a-SiO2 от 298 до 800 К, если зависимость теплоемкости от температуры выражается уравнением:
С0р = 46,94 +34,31*10-3Т – 11,3*105 /Т2.
(1,0212·106 Дж)
Зависимость теплового эффекта реакции Н2(г) + ½ О2(г) = Н2О(г) от температуры выражается уравнением:
DrH°Т (Дж/моль) = -237,65*103 – 13,01Т + 2,88*10-3Т2 –1,71. Рассчитайте изменение теплоемкости DСр DСVдля этой реакции при 800 К. (DСр = -8,14 Дж моль-1К-1, DСV= -3,98 Дж моль-1К-1)
Определите тепловой эффект химической реакции СН3ОН(г) + 3/2О2 = СО2 + 2Н2О(г) при 500 К и стандартном давлении. При расчете воспользуйтесь средними теплоемкостями веществ в интервале температур от 298 до 500 К. (-673,29 кДж)
Стандартная энтальпия образования формальдегида при 25°С равна –108,6 кДж/моль. Рассчитайте стандартную энтальпию образования формальдегида при 150°С, если известны теплоемкости: (-110,7 кДж моль-1)
| Вещество | С(графит) | Н2(г) | N2(г) | С2Н5N(г) |
| Ср,Дж*моль-1*К-1 | 8,53 | 28,82 | 29,13 | 53,10 |
Глава3. Второй закон термодинамики
Похожие работы
... и химическим процессам, происходящим в веществе, в различных системах. Важным достижением на пути этого процесса интеграции знаний было открытие фундаментального закона природы - закона сохранения и превращения энергии. Основатель термодинамики С. Карно в своем труде "Размышления о движущей силе огня и о машинах, способах развивать эту силу" пишет: "Тепло - это не что иное, как движущая сила, ...
... газов в результате реакции. Величина Δn может иметь положительное и отрицательное значения, в зависимости от того, увеличивается или уменьшается число молей газов во время процесса. Применение первого начала термодинамики к процессам в любых системах. Закон Гесса Примем, что единственным видом работы, которая совершается системой, является работа расширения. Подставляя уравнение (II, 5) в ...
... , или термодинамическое равновесие, при котором движение частиц хаотично. Максимальная энтропия означает полное термодинамическое равновесие, что эквивалентно хаосу. Часто второе начало термодинамики преподносится как объединенный принцип существования и возрастания энтропии. Принцип существования энтропии формулируется как математическое выражение энтропии термодинамических систем в условиях ...
... в ходе реакции мало, т.е. , тогда ; . При термомеханическом описании реакции опускают , , говорят только об изменении энтальпии : Закон Гесса: тепловой эффект химической реакции протекающий или при или при не зависит от числа промежуточных стадий, а определяется лишь конечным и начальным состоянием системы. Тепловой ...
0 комментариев