Навигация
Определение устойчивости к гипоксии крыс и адаптация к ней низкоустойчивых крыс
2.8. Определение устойчивости к гипоксии крыс и адаптация к ней низкоустойчивых крыс
Группу самцов линии Вистар, поместив в барокамеру и снизив давление до 22 кПа, подвергли острой гипобарической гипоксии, соответствующей подъему на высоту 11500 м. Те животные, что выдерживали гипоксию в течение 10-15 минут, считались высокоустойчивыми. Низкоустойчивые крысы выдерживали эту высоту только в течение полутора минут. Среднеустойчивых крыс в эксперимент не брали. Адаптация низкоустойчивых крыс проводилась методом интервальной нормобарической гипоксии. Для этого животные помещались в камеру с контролируемой подачей воздуха. В течение двенадцати дней животным ежедневно по пять раз в день подавался воздух с вдвое сниженной концентрацией кислорода в течение 10 минут с трехминутными перерывами, во время которых животным подавался воздух с нормальной концентрацией кислорода.
3. Результаты и обсуждение
3.1. Выделение белка с молекулярной массой 55 кДа
|

Рисунок 3. SDS-электрофорез фракций после повторной хроматографии. На треке 1 – маркер. На треках 2,3 – белок с Мr 55 кДа (фракции с 250 мМ КСl)
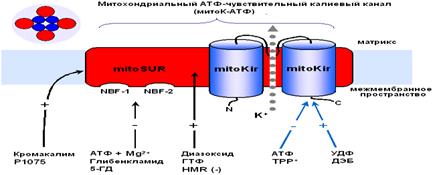
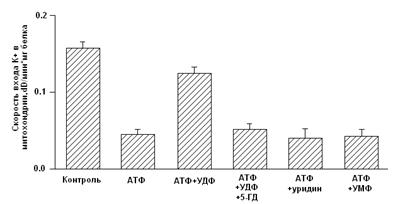
Дополнительная проверка фракций проводилась на приборе для определения проводимости искусственных бислойных мембран. При встраивании белка фракции, содержащих канальную субъединицу мито-К+АТФ обнаруживалась проводимость мембран, ингибируемая АТФ (рис 4).
Для дополнительной очистки проводили повторную хроматографию активной фракции. Для окончательной очистки белка до электрофоретически гомогенного состояния проводился нативный электрофорез активной фракции с последующей элюцией белка с геля.
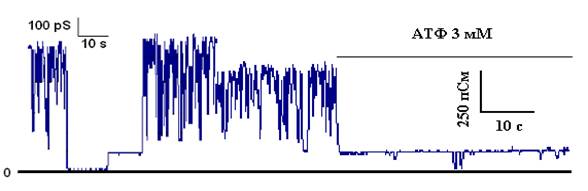 Рисунок 4. К+-транспортирующая АТФ-ингибируемая активность белка с молекулярной массой 55 кДа, реконструированного в искусственную мембрану.
Рисунок 4. К+-транспортирующая АТФ-ингибируемая активность белка с молекулярной массой 55 кДа, реконструированного в искусственную мембрану.
Электрофоретически гомогенный АТФ-ингибируемый К+-транспортирующий белок с Mr 55 кДа замораживали и накапливали для иммунизации. При выделении вышеописанным методом из 100 г печени крыс получали 30-70 мкг очищенного белка. Иммунизацию кроликов проводили при накоплении 0.2-0.4 мг белка.
3.2. Определение параметров дыхания у крыс с различной устойчивостью к гипоксии и адаптированных к ней
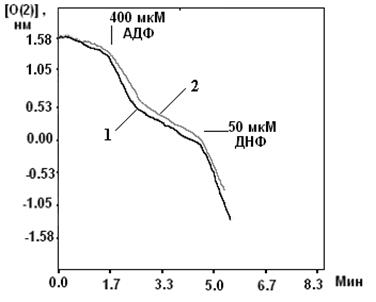
Определение проводилось с помощью кислородного электрода Кларка. Определялась скорость дыхания (V3) и скорость фосфорилирования АДФ (V2) в митохондриях печени и сердца трех групп крыс. Полученные данные представлены в таблице 5.
Как видно из таблицы 5, митохондрии печени высокоустойчивых к гипоксии крыс скорости дыхания во всех метаболических состояниях, а также в присутствии разобщителя ниже по сравнению с этими скоростями у низкоустойчивых животных. Этот эффект не зависел от наличия К+ в среде
| Среда | Группы крыс | V2, нмоль О2/мин*мг белка | V3, нмоль О2/мин*мг белка | V4, нмоль О2/мин*мг белка | VДНФ, нмоль О2/мин*мг белка | ДК |
| С ионами К+ | ВУ | 8.38±1.14 | 87.9±3.54 | 23.24±2.88 | 179.5±4.88 | 3.78±0.12 |
| НУ | 14.54±1.68 | 110.76±4.95 | 32.9±3.25 | 181.0±4.27 | 3.36±0.33 | |
| А | 11.46±1.32 | 68.03±4.76 | 24.7±2.65 | 94.4±4.12 | 2.75±0.21 | |
| Без ионов К+ | ВУ | 8.46±0.93 | 35.01±3.87 | 11.61±2.54 | 112±5.21 | 3.1±0.26 |
| НУ | 14.6±2.05 | 64.01±3.24 | 26.58±3.44 | 166.78±5.8 | 2.4±0.19 | |
| А | 8.76±1.39 | 45.95±4.77 | 19.92±1.76 | 79.55±4.22 | 2.3±0.14 |
Таблица 5. Скорость дыхания в митохондриях печени крыс с различной устойчивостью и адаптированных к гипоксии с использованием двух сред и сукцината в качестве дыхательного субстрата.
инкубации митохондрий. Адаптация к гипоксии низкоустойчивых животных ведет также к снижению всех скоростей, однако, в присутствии ионов калия,
эти скорости дыхания снижаются не столь значительно. Последнее может указывать на активацию транспорта ионов К+ в митохондриях при адаптации животных к гипоксии. Следует отметить, что эти эффекты больше проявляются по отношению к скорости дыхания в присутствии субстрата (V2, V4) по сравнению со скоростью АДФ-стимулируемого дыхания (V3). Это может быть связано с увеличением концентрации АТФ в митохондриях после фосфорилирования добавленного АДФ. Как известно, АТФ ингибирует вход катионов К+ в митохондрии.
Обнаружено также, что у адаптированных к гипоксии животных дыхательный контроль в среде с ионами К+ снижен по сравнению с этим показателем у низкоустойчивых к гипоксии животных. Это снижение наблюдается только в среде, содержащей катионы К+, что может указывать на активацию энергозависимых процессов в митохондриях.
Совокупность полученных данных указывает на то, что 1) адаптация к гипоксии ведет к ингибированию работы фосфорилирующей дыхательной цепи, независимо от присутствия или отсутствия ионов К+ в среде, вероятно, за счет активации гликолиза и 2) адаптация ведет также к активации знергозависимого входа К+ в митохондрии.
Для подтверждения полученных данных у этих же животных были определены параметры АТФ-зависимого транспорта ионов К+ в митохондриях, а также количество катионов К+ в них.
Похожие работы
... м, в течение 10-15 мин. Группа низкоустойчивых (НУ) животных выдерживала эту высоту только в течение 1-1.5 мин. Глава 5. Результаты и обсуждения 5.1 Параметры функционирования митоКАТФ канала у крыс с различной резистентностью, а также у животных, адаптированных к гипоксии В этом разделе работы исследовались такие показатели, как дыхание МХ, скорость АТФ-зависимого К+ транспорта, ...
0 комментариев