Навигация
Расчет расходных коэффициентов
1. Расчет расходных коэффициентов
Это параметры, характеризующие расход различных видов сырья на единицу полученной продукции. Различают теоретические и практические расходные коэффициенты. Теоретические расходные коэффициенты учитывают расход исходящего сырья с учетом стехиометрии реакции. Практические расходные коэффициенты учитывают селективность процесса, выход продукта, степень превращения (и рассчитываются на базе теоретических). Задание: Рассчитать теоретические и практические расходные коэффициенты для реагентов по основной реакции на 1 тонну целевого продукта.
![]()
Найдем молярные массы веществ участвующих в реакциях:
![]()
![]()
![]()
![]()
1.1 Рассчитаем теоретические расчетные расходные коэффициенты
![]()
![]()
![]()
![]()
1.2 Рассчитаем практические расходные коэффициенты для циклогексана
![]()
![]()
1.3 Рассчитаем практические расходные коэффициенты для циклогексана в смеси с бензолом
![]()
![]()
1.4 Рассчитаем практические расходные коэффициенты для примеси (бензол)
![]()
![]()
1.5 Исходя из мольного соотношения исходных реагентов, рассчитаем практические расходные коэффициенты для кислорода
![]()
![]()
![]()
![]()
![]()
![]()
![]()
Рассчитаем практические расходные коэффициенты для кислорода в смеси с азотом:
![]()
![]()
Рассчитаем практические расходные коэффициенты для примеси (азот):
![]()
![]()
Вывод: Таким образом, для получения 1 т циклогексанона необходимо взять 857,14 кг циклогексана и 326,53 кг кислорода, но с учетом состава вещества, а также технико-экономических показателей практические расходные коэффициенты составляют:
по циклогексану – 1177,86 кг
по кислороду – 3888,76 кг.
II. Расчет материального баланса
Составление материального баланса – основное звено в оценке технико-экономической эффективности химического процесса.
На основании данных материального баланса определяют основные технико-экономические показатели, такие как выход, селективность, степень превращения, расходные коэффициенты. Данные материального баланса используются при составлении энергетического или теплового баланса, при термодинамических и кинетических расчетах, расчетах реакторов.
Материальный баланс химико-технологического процесса – это вещественное выражение закона сохранения вещества, левую часть которого составляет масса всех вступивших в реакцию веществ (приход), а правую – масса полученных продуктов (расход) и производственные потери.
2.1 Расчет теоретического материального баланса
Задание: Рассчитать на основании вышеприведенных данных материальный баланс реакции получения циклогексанона:
![]()
Молярные массы веществ участвующих в реакциях:
![]()
![]()
![]()
![]()
Рассчитаем количество циклогесканона в кмолях:
![]()
![]()
Рассчитаем количество кмоль/час циклогексана, необходимого для получения 10,20 кмоль/час циклогексанона:
![]()
![]()
Рассчитаем количество кмоль/час кислорода, необходимого для получения 10,20 кмоль/час циклогексанона:
![]()
![]()
Рассчитаем количество образовавшейся воды:
![]()
![]()
Результаты расчетов сводим в таблицу:
Таблица 2. Теоретический материальный баланс
| Приход | Расход | ||||||||
| вещество |
| % мольн. |
| % масс. | вещество |
| % мольн. |
| % масс. |
| С6Н12 | 10,20 | 50 | 856,8 | 72,4 | С6Н10О | 10,20 | 50 | 999,6 | 84,5 |
| О2 | 10,20 | 50 | 326,4 | 27,6 | Н2О | 10,20 | 50 | 183,6 | 15,5 |
| Итого: | 20,40 | 100 | 1183,2 | 100 | Итого: | 20,40 | 100 | 1183,2 | 100 |
Вывод: Таким образом, в результате расчета установили, что при получении 1 тонны циклогексанона необходимо взять 856,8 кг циклогексана и 326,4 кг кислорода. При этом выделяется 183,6 кг воды.
Похожие работы
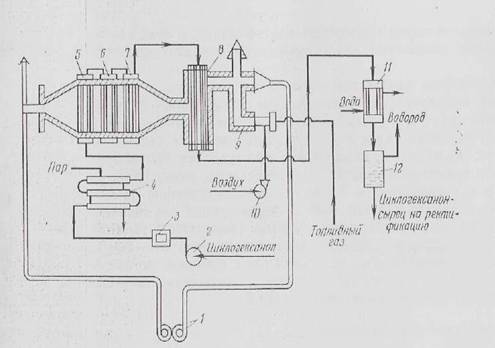
... 80-81 Продукты уплотнения 1 - 1,1 Циклогексанол 17--18 Циклогексен 0,5-0,6Вода 0,2-0,3 Рисунок 1. Технологическая схема процесса получения циклогексанона дегидрированием циклогексанола: 1 - ротационная газодувка; 2 - насос; 3 - фильтр; 4 - подогреватель; 5, 6 - испарители; 7 - перегреватель; 8 - контактный аппарат; 9 - тонка; 10 - воздуходувка; 11 - конденсатор; 12 - сепаратор. ...
... и электротехнической промышленности, в производстве дезинфицирующих средств, в пищевой и химико-фармацевтической промышленности, в получении лаков и эмалей, растворителей, самоотверждающихся составов. 1.3. Синтез адипиновой кислоты В 5-литровую круглодонную колбу, снабженную механической мешалкой, термометром и делительной воронкой емк. В 1л, помещают 2100г (16,6мол) 50%-ной азотной ...
... кристаллы отсасывают, промывают небольшим количеством ледяной воды и сушат при 110оС. Соли можно перекристаллизовывать из воды. NH3 + HReO4 = NH4ReO4 [12] По этой методике был проведен синтез перрената аммония. К 7 мл. концентрированной рениевой кислоты прилили 11 мл. раствора аммиака. В качестве индикатора использовался метилрот ( pH 6.2 - 6.4 ). Белый осадок перрената аммония ...
... из нафты (температура кипения 80 – 160оС) высокооктановых бензинов и ароматических соединений, которые экстрагируют из бензинов и используют в качестве сырья для гидрокрекинга или для органического синтеза. Процесс проводят в интервале 380 – 520оС при давлении 10 – 40 атм на гетерогенных бифункциональных катализаторах – металлических и кислотных – Pt на промотированном Cl– или F– оксиде алюминия ...

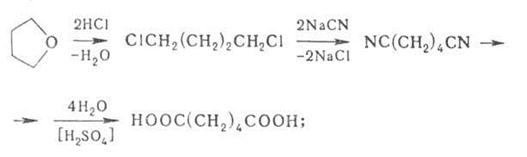

0 комментариев