Навигация
Задачи с решениями
6.2 Задачи с решениями
1. Для обратимой реакции первого порядка 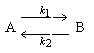
Кр = 8, а k1 = 0,4 c-1. Вычислите время, при котором концентрации веществ А и В станут равными, если начальная концентрация вещества В равна 0.
Решение. Из константы равновесия находим константу скорости обратной реакции: k-1 = k1/К = 0,4/8 = 0,05 с-1. По условию мы должны найти время, за которое прореагирует ровно половина вещества А. Для этого надо подставить значение х(t) = а/2 в решение кинетического уравнения для обратимых реакций:
t![]() .
.
Ответ: t = 1,84 с.
2. В параллельных реакциях первого порядка С ¬ А ® В выход вещества В равен 63%, а время превращения а на 1/3 равно 7 мин. Найдите k1 и k2.
Решение. Кинетическое уравнение для разложения вещества в параллельных реакциях имеет вид уравнения первого порядка![]() , в которое вместо одной константы входит сумма констант скорости отдельных стадий. Следовательно, по аналогии с реакциями первого порядка, по времени превращения А на 1/3 (х(t) = a/3) можно определить сумму констант k1 + k2:
, в которое вместо одной константы входит сумма констант скорости отдельных стадий. Следовательно, по аналогии с реакциями первого порядка, по времени превращения А на 1/3 (х(t) = a/3) можно определить сумму констант k1 + k2:
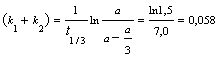 мин-1.
мин-1.
Выход вещества В равен 63%, а вещества D – 37%. Отношение этих выходов равно отношению конечных концентраций веществ В и D, следовательно оно равно отношению соответствующих констант скоростей
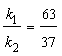 . Решая это уравнение совместно с предыдущим, находим: k1 = 0,037, k2 = 0,021.
. Решая это уравнение совместно с предыдущим, находим: k1 = 0,037, k2 = 0,021.
Ответ: k1 = 0,037 мин-1, k2 = 0,021 мин-1.
3. В системе протекают две параллельные реакции А + 2В→ → продукты (k1) и A +2C → продукты (k2). Отношение k1/ k2 = 5. Начальные концентрации веществ В и С одинаковы. К моменту времени t прореагировало 50% вещества В. Какая часть вещества С прореагировала к этому моменту?
Решение. Запишем кинетические уравнения для первой и второй реакций: ![]() . Поделив одно кинетическое уравнение на другое, избавимся от временной зависимости и получим дифференциальное уравнение, описывающее фазовый портрет системы, т. е. зависимость концентрации одного из веществ от концентрации другого:
. Поделив одно кинетическое уравнение на другое, избавимся от временной зависимости и получим дифференциальное уравнение, описывающее фазовый портрет системы, т. е. зависимость концентрации одного из веществ от концентрации другого: ![]() с начальным условием [В]0 = [С]0. Это уравнение решается методом разделения переменных:
с начальным условием [В]0 = [С]0. Это уравнение решается методом разделения переменных: ![]() , где константа находится из начального условия
, где константа находится из начального условия ![]() . Подставляя в это решение [В] = [В]0/2, находим [С]= 5[В]/6 = 5[С]0/6, т.е. к моменту времени t прореагирует 1/6 вещества С.
. Подставляя в это решение [В] = [В]0/2, находим [С]= 5[В]/6 = 5[С]0/6, т.е. к моменту времени t прореагирует 1/6 вещества С.
4. Реакция разложения изопропилового спирта протекает в присутствии катализатора триоксида ванадия при 588 К с образованием ацетона, пропилена и пропана. Концентрации веществ реакции, измеренные через 4,3 с после начала опыта, следующие, ммоль: с![]() ; с
; с![]() ; с
; с![]() . Определите константу скорости каждой реакции, если в начальный момент в системе присутствовал только С3Н7ОН.
. Определите константу скорости каждой реакции, если в начальный момент в системе присутствовал только С3Н7ОН.
Решение: Определим начальное количество С3Н7ОН: [А]0 = с1 + с2 + с3 + с4 = 24,7 + 7,5 + 8,1 + 1,7 = 44,7 ммоль/л. Вычислим сумму констант скоростей реакций:
![]()
![]()
![]() ,
, ![]() c-1.
c-1.
Определим константу скорости каждой реакции:
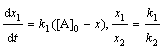 ;
; 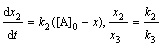 ;
; ![]()
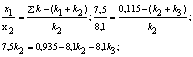
![]() ;
;
Так как х2/х3 = k2/k3, то 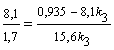 ;
;
![]() ;
;
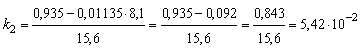 с-1;
с-1;
![]() .
.
Ответ: ![]() с-1.
с-1.
5. Последовательная реакция первого порядка протекает по схеме ![]()
![]() В. При 298 К имеет удельные скорости: k1 = 0,1 ч-1; k2 = 0,05 ч-1; начальная концентрация исходного вещества [А]0 = 1 моль/л. Вычислите: 1) координаты максимума кривой [Р] = f(t); 2) время достижения концентрации [А] = 0,001 моль/л, продолжительность tA реакции А→Р; 3) концентрации [Р] и [В] в момент окончания реакции А→Р; 4) время, за которое концентрация В достигнет значении 0,01 моль/л и продолжительность индукционного периода этой реакции, tинд; 5) координаты точки перегиба кривой [В] = f(t); 6) точку пересечения кривых [А] = f(t) и [Р] = f(t). Решение: Рассчитаем время, которому будет соответствовать максимальная концентрация промежуточного продукта, ч:
В. При 298 К имеет удельные скорости: k1 = 0,1 ч-1; k2 = 0,05 ч-1; начальная концентрация исходного вещества [А]0 = 1 моль/л. Вычислите: 1) координаты максимума кривой [Р] = f(t); 2) время достижения концентрации [А] = 0,001 моль/л, продолжительность tA реакции А→Р; 3) концентрации [Р] и [В] в момент окончания реакции А→Р; 4) время, за которое концентрация В достигнет значении 0,01 моль/л и продолжительность индукционного периода этой реакции, tинд; 5) координаты точки перегиба кривой [В] = f(t); 6) точку пересечения кривых [А] = f(t) и [Р] = f(t). Решение: Рассчитаем время, которому будет соответствовать максимальная концентрация промежуточного продукта, ч:
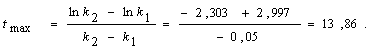
Обозначим концентрацию А при tmax через [А]max. Тогда [А]max = [А]![]() моль/л; максимальная концентрация промежуточного продукта будет [Р]max = (k1/k2).[А]max= (0,1/0,05).0,249=0,598 моль/л. Примем [А]0 = = 0,001 моль/л; тогда
моль/л; максимальная концентрация промежуточного продукта будет [Р]max = (k1/k2).[А]max= (0,1/0,05).0,249=0,598 моль/л. Примем [А]0 = = 0,001 моль/л; тогда ![]() ;
; ![]() ч. Рассчитаем концентрацию Р при t = 69 ч:
ч. Рассчитаем концентрацию Р при t = 69 ч:
[В]![]() ;
;![]() моль/л.
моль/л.
Рассчитаем концентрацию продукта [В] через 69 ч: [В] = = [А]0 - [Р] - [А] = = 1 – 0,061 – 0,001 = 0,938 моль/л. Вычислим время tинд, за которое устанавливается концентрация В, равная 0,01 моль/л, по уравнению
[В] = [А]0 ![]() ; [В]
; [В]![]() ;
;![]() (1)
(1)
Уравнение (1) решаем относительно tинд методом подбора на основании экспериментальных данных:
| tинд, ч | 1 | 2 | 2,5 | 3 | 4 |
| [В], моль/л | 0 | 0,008 | 0,014 | 0,018 | 0,032 |
Принимаем tинд = 2 ч. Точку перегиба кривой [В] = f(t) находим, используя условие ![]() . После дифференцирования и преобразований уравнения [В]=[А]0•
. После дифференцирования и преобразований уравнения [В]=[А]0•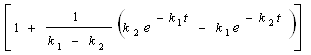 полу-чим точку перегиба:
полу-чим точку перегиба: ![]() или
или ![]() , где tП – координата точки перегиба, которую находим методом подбора для значений индукционных периодов tинд 5, 15, 10, 20 ч. Строим график зависимости х = f(t): х = 2е-0,1t – е-0,05t, откуда х = 0,05 при t = 13,6 ч. Концентрацию [В] в точке перегиба находим по уравнению (2): [В] = = 0,243 моль/л.
, где tП – координата точки перегиба, которую находим методом подбора для значений индукционных периодов tинд 5, 15, 10, 20 ч. Строим график зависимости х = f(t): х = 2е-0,1t – е-0,05t, откуда х = 0,05 при t = 13,6 ч. Концентрацию [В] в точке перегиба находим по уравнению (2): [В] = = 0,243 моль/л.
Похожие работы
... параметров ионного и электронного транспорта в переходных слоях интерфазы. 4. Принципы создания твердофазных электрохимических преобразователей энергии и информации. 5. Гипотеза о самоорганизации переходных ион-проводящих структур при протекании электрохимических и химических процессов на фазовых границах. Определяющую роль матричных структур в твердофазных электродных реакциях. ...
... устойчивость металлов и сплавов определяется их стойкостью к коррозии в водной среде. Лучшим способом представления термодинамической информации о химической и электрохимической устойчивости металлических систем в водных растворах являются диаграммы рН-потенциал. Впервые такие диаграммы в системе элемент-вода для чистых металлов при температуре 250С были построены Марселем Пурбе и использованы им ...
... агрессивных средах и при наличии различных сопутствующих физических факторов; 3. Определить методы применения противокоррозионных защитных покрытий, в первую очередь лакокрасочных. Обзорно-аналитическая часть Характеристика коррозионных процессов Коррозия металлов - разрушение металлов вследствие физико-химического воздействия внешней среды, при этом металл переходит в окисленное (ионное) ...
... не менее пяти циклов разряд – заряд глубиной 250 Кл/см2. Основные результаты и выводы Настоящая работа обобщает результаты комплексного исследования механизма и кинетики электродных процессов в ионной и электронной подсистемах в низкотемпературных твердых электролитах с использованием импульсных методов. Важнейшим результатом работы является получение новых и уточнение полученных другими исс

0 комментариев