Навигация
Расчет сушилки с кипящим слоем
3.5 Расчет сушилки с кипящим слоем
3.5.1 Материальный и тепловой баланс процесса горения
В сушильной установке с кипящим слоем подогрев сушильного агента осуществляется за счет сжигания газообразного топлива с высоким избытком воздуха в топке. При этом требуемая температура сушильного агента обеспечивается за счет дополнительного смешения продуктов сгорания и воздуха перед сушильной камерой.
Целью расчета является определение состава сушильного агента (смеси продуктов сгорания и воздуха), влагосодержания и энтальпии. Исходными данными являются элементарный состав топлива и температура газов перед сушилкой. Основой для расчета являются уравнения материального и теплового баланса процесса горения, учитывающие изменения теплоемкости газов в зависимости от температуры.
Требуемые для расчета параметры воздуха - энтальпия h0 и влагосодержание x0 определяем по h-x диаграмме влажного воздуха: h0 = 38 кДж/кг;x0 = 9∙10-3кг/кг.
Сжигание газообразного топлива
В качестве теплоносителя используем топочный газ, образующийся при горении газообразного топлива. В таблице 3.5.1.1.1 представлен состав используемого природного газа.
Таблица 3.5.1.1.1 Состав топлива
| Компонент газа | CH4 | C2H6 | C3H8 | C4H10 | CO2 | N2 |
| Объемное содержание данного компонента yi, % | 98,7 | 0,35 | 0,12 | 0,06 | 0,1 | 0,67 |
Теоретически необходимое количество воздуха для сжигания 1 м3 газа:
V0 = 0,0476 [yH2/2 + yCO/2 + yH2S + (3.5.1.1.1)
+ ∑(m+n/4)yCmHn - yO2],
где yi- объемное содержание данного компонента, %.
Так как используемый газ не содержит в себе H2, O2 и H2S, то в соответствии с уравнением (1) имеем:
V0 = 0,0476 [(1+4/4)98,7 + (2+6/4)0,35 + (3.5.1.1.2)
+ (3+8/4)0,12 + (4+10/4)0,06] = 9,5 м3/м3.
Находим объем дымовых газов. Теоретический объем азота:
V0N2 = 0,79V0 + 0,01yN2,(3.5.1.1.3)
V0N2 = 0,79∙9,5 + 0,01∙0,67 = 7,5 м3/м3. (3.5.1.1.4)
Объем трехатомных газов:
VRO2 = 0,01∙(yCO2 + yCO + yH2S +∑myCmHn), (3.5.1.1.5)
VRO2 = 0,01[(1∙98,7 + 2∙0,35 + 3∙0,12 +(3.5.1.1.6)
+ 4∙0,06 + 0,1)] = 1,0 м3/м3.
Теоретический объем водяных паров:
V0H2O = 0,01(yH2S+∑(n/2)yCmHn) + 1,61V0∙x0, (3.5.1.1.7)
где V0 - теоретически необходимое количество воздуха для сжигания 1 м3 газа, равное 9,5 м3/м3,
x0 - влагосодержание воздуха, равное 9∙10-3 кг/кг.
V0H2O = 0,01(2∙98,7 + 3∙0,35 + 4∙0,12 + 5∙0,06) +(3.5.1.1.8)
+ 1,61∙9,5∙9∙10-3 = 2,13 м3/м3.
Низшая теплота сгорания газового топлива определяется на 1м3 газа при нормальных условиях через теплоты сгорания составляющих его компонентов:
Qcн = 358,2∙yCH4 + 637,5∙yC2H5 + 912,5∙yC3H8 + (3.5.1.1.9)
+ 711,7∙yC4H10 + 126,4∙yCO,
Qcн = 358,2∙98,7 + 637,5∙0,35 + 912,5 ∙0,12 +(3.5.1.1.10)
+ 711,7∙0,06 + 126,4∙0,1 = 35742,31 кДж/м3.
Определение избытка воздуха и параметров смеси
Коэффициент избытка воздуха α определяется из уравнения теплового баланса, записанного для условий адиабатного сжигания:
Qφв + Qcн = hг,(3.5.1.2.1)
Qcн + α∙ V0∙cв∙t0 = hг0 + (α-1)∙h0в,(3.5.1.2.2)
где cв - теплоемкость воздуха, кДж/м3К,
h0в - энтальпия теоретически необходимого количества воздуха при температуре t = t1, °С.
Здесь энтальпия газов hг0 при α = 1 и температуре газов t = t1 определяется выражением:
hг0 = VRO2∙ сRO2∙ t1 + V0H2O∙ cH2O ∙ t1 +(3.5.1.2.3)
+ V0N2∙ cN2∙ t1, кДж/м3.
При расчете необходимо учитывать зависимость теплоемкости от температуры для газовых компонентов в следующем виде:
Теплоемкость сухих трехатомных газов
сRO2 = 1,6 + 0,00088∙ t1,(3.5.1.2.4)
где t1- температура теплоносителя на входе в сушилку, равная 330°С,
сRO2 = 1,6 + 0, 00088∙330 = 1,89 кДж/м3К.(3.5.1.2.5)
Теплоемкость азота
cN2 = 1,29 + 0,000202∙ t1,(3.5.1.2.6)
cN2 = 1,29 + 0,000202∙ 330 = 1,36 кДж/м3К. (3.5.1.2.7)
Теплоемкость водяных паров
cH2O= 1,49+0,00016∙ t1,(3.5.1.2.8)
cH2O= 1,49+0,00016∙ 330 = 1,54 кДж/м3К.(3.5.1.2.9)
Теплоемкость воздуха
cв = 1, 319 + 0, 000078∙ t1,(3.5.1.2.10)
cв = 1, 319 + 0, 000078∙ 330 = 1, 34 кДж/м3К.(3.5.1.2.11)
Энтальпия теоретически необходимого количества воздуха при температуре t = t1, °С:
h0в = V0∙ cв ∙ t1,(3.5.1.2.12)
h0в = 9,5∙1,34∙330 = 4200 кДж/м3.(3.5.1.2.13)
Таким образом, уравнение (3.5.1.2.3) принимает вид:
hг0 = 1,0∙1,89∙330 + 2, 13∙1,54∙330 + (3.5.1.2.14)
+ 7,5∙1,36∙330 = 5072 кДж/м3.
Физическая теплота воздуха:
Qφв = α∙V0∙ cв∙t0,(3.5.1.2.15)
где V0 - теоретически необходимое количество воздуха для сжигания 1 м3 газа, равное 9,5 м3/м3 (3.5.1.1.2).
Qφв = α∙9,5∙1,34∙20 = 255∙α кДж/м3.(3.5.1.2.16)
Определяем избыток воздуха из уравнения (3.5.1.2.2):
α = (Qcн - hг0 + h0в )/(h0в - V0∙ cв∙t0),(3.5.1.2.17)
где Qcн - низшая теплота сгорания газового топлива определяется на 1м3 газа при нормальных условиях, равная 35742,31 кДж/м3 (3.5.1.1.10).
α = (35742,31 - 5072 + 4200)/(4200 - 255) = 8,84. (3.5.1.2.18)
Тогда действительный объем водяных паров при избытке воздуха будет равен:
VH2O = V0H2O + 1, 61(α - 1) V0∙x0,(3.5.1.2.19)
где x0 - влагосодержание определяемое по h-x диаграмме влажного воздуха, равное 9∙10-3 кг/кг.
VH2O = 2, 13 + 1, 61(8,84 - 1)*(3.5.1.2.20)
*9,5∙9∙10-3 = 3,2 м3/м3.
Объем сухих дымовых газов:
Vс.г. = VRO2 + V0N2 +(α - 1) V0,(3.5.1.2.21)
где VRO2 - объем трехатомных газов, м3/м3; V0N2 - теоретический объем азота, м3/м3.
Vс.г. = 1,0 + 7,5 + (8,84 - 1)∙ 9,5 = 82,98 м3/м3. (3.5.1.2.22)
Найдем плотность отдельных компонентов при данном давлении (Р = 101, 325 кПа) и температуре из уравнения состояния идеального газа:
ρi = (P∙μi)/[R∙( t1 + 273)],(3.5.1.2.23)
где μi - молярная масса компонентов газа.
Плотность воздуха:
ρв = (P∙μв)/[R∙( t1 + 273)],(3.5.1.2.24)
ρв = (101325∙28,8)/[8314∙(330+ 273)] = 0, 582 кг/м3. (3.5.1.2.25)
Плотность азота:
ρN2 = (P∙μN2)/[R∙( t1 + 273)],(3.5.1.2.26)
ρN2 = (101325∙28)/[8314∙(330+ 273)] = 0, 566 кг/м3. (3.5.1.2.27)
Плотность сухих трехатомных газов:
ρRO2 = (P∙μRO2)/[R∙( t1 + 273)],(3.5.1.2.28)
ρRO2 = (101325∙44)/[8314∙(330+ 273)] = 0, 889 кг/м3. (3.5.1.2.29)
Плотность сухих дымовых газов:
ρ с.г. = (∑ρi∙Vi)/Vс.г.,(3.5.1.2.30)
ρ с.г. = [(0, 889∙1,0) + (0, 566∙7,5) + (3.5.1.2.31)
+ (0, 582∙(8, 84 - 1)∙ 9,5)]/82, 98 = 0, 584 кг/м3.
Плотность водяных паров:
ρH2O = (P∙μH2O)/[R∙( t1 + 273)], (3.5.1.2.32)
ρH2O = (101325∙18)/[8314∙(330+ 273)] = 0, 364 кг/м3. (3.5.1.2.33)
Влагосодержание теплоносителя на входе в сушильную камеру при заданной температуре t1 определяем из выражения:
x1 = (VH2O/Vс.г.)∙( ρH2O/ρ с.г.),(3.5.1.2.34)
где VH2O - действительный объем водяных паров при избытке воздуха, равный 3,2 м3/м3,
Vс.г. - объем сухих дымовых газов, равный 82,98 м3/м3 (3.5.1.2.22).
x1 = (3,2 / 82, 98)∙( 0, 364 / 0, 584) = 0, 024 кг/кг. (3.5.1.2.35)
По h-x диаграмме влажного воздуха (рисунок 3.5.1.2.1) при известных температуре t1, равной 330°, и влагосодержании x1, равному 0, 024,определяем энтальпию газов перед сушильной установкой: h1 = 400 кДж/кг.
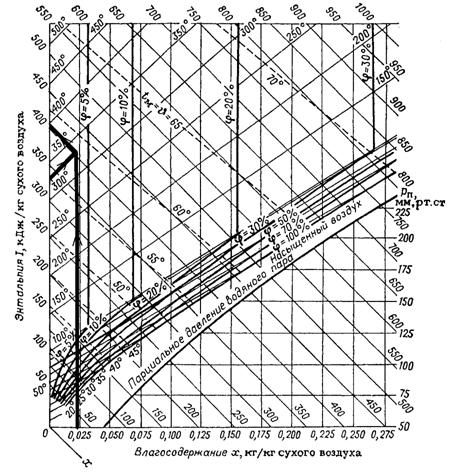
Рисунок 3.5.1.2.1. Нахождение энтальпии по h-x диаграмме влажного воздуха
0 комментариев